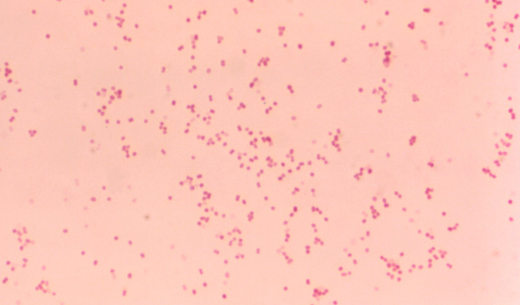
Бранхамелла катаралис что это такое
Moraxella catarrhalis
Сегодня мы поговорим о крайне интересном, с нашей точки зрения, микробе — моракселле. Этот разговор актуален особенно сейчас, когда может оказаться, что в постковидную эпоху именно этот зверек потенциально сможет понаделать много бед.
Автор: Трубачева Е.С., врач – клинический фармаколог
Сегодня мы поговорим о крайне интересном, с нашей точки зрения, микробе — моракселле, тем более этот разговор был обещан в предыдущей статье, посвященной эмпирической терапии заболеваний верхних дыхательных путей, а обещания принято выполнять. Этот разговор актуален особенно сейчас, когда может оказаться, что в постковидную эпоху именно этот зверек потенциально сможет понаделать много бед.
Микробиологические аспекты
Итак, Moraxella catarrhalis относится к грамотрицательным бактериям и входит в состав нормальной микрофлоры человека. Точнее будет сказать, что нормой она будет у маленьких обитателей планеты, то есть у детей. В холодное время года частота нормального носительства в этой возрастной группе достигает 75%. У взрослых же, напротив, моракселл мало, и определяются они у 1–5%.
Норма и норма, скажете вы, не первый раз уже обсуждаем, как нормальная микрофлора начинает бросаться на своих хозяев. Поэтому теперь обещанное интересное — дело в том, что носительство у взрослых сопряжено с наличием у них хронических заболеваний верхних и нижних дыхательных путей, вызванных другими патогенами. Ключевое слово — «другими». И тут начинается самое интересное. Помните, как в самом начале мы договорились не считать микробов статичными и аморфными существами? Например, в этой статье мы выяснили, что образование биопленок является результатом бурной социальной жизни микробов. Так вот, микробы бурно общаются не только в рамках своего штамма или вида, существует и межвидовое общение, чему моракселла наглядный пример. Поэтому поговорим об этом подробнее.
Одним из факторов патогенности Moraxella catarrhalis является пресловутая биопленка, которая помогает выживать колонии в достаточно агрессивных условиях нашего организма, одна иммунная система которого, с которой уже год активно воюют практически во всех ковидных госпиталях мира, чего стоит. Как вы помните, одним из компонентов нашей иммунки является система комплемента, и именно моракселла умеет ему противостоять. Причем у здоровых носителей комплемент уничтожить M. catarrhalis может, а у больных нет. Причина этого давно известна — это белок Usp2, связывающийся с человеческим вибронектином, но это даже не то что не тема данной статьи, это вообще только для тех, кого крепко укусила микробиологическая муха и кому хочется покопать тему поглубже. Мы просто примем как факт, что у больного человека система комплемента против моракселлы бессильна. И отсюда вытекает задумчивый первый вопрос — интересно, а сколько моракселл сейчас по ковидариям скачет?
Ну и что, что биопленка, опять спросите вы? Где вся глубина социальной коммуникации? Сейчас расскажем. Дело в том, что сама по себе Moraxella catarrhalis крайне редко вызывает хоть какое-то заболевание. Для этого надо иметь хорошо прибитый иммунитет (второй задумчивый вопрос — а сколько мораксельных пневмоний мы будем видеть у повторно заболевших, перенесших ранее ковид?) или тяжелое основное заболевание, либо травму, к которым в условиях стационарного лечения в качестве ВБИ присоединилась пневмония, вызванная Moraxella catarrhalis. В обычной стандартной ситуации моракселла если что и вызывает, то только оказывая содействие другим возбудителям заболеваний верхних и нижних дыхательный путей:
Как моракселла это делает? Дело в том, что она умеет формировать специальные агреганты, тем самым увеличивая прилипание на поверхности эпителия, например, пиогенного стептококка, в 10–20 раз. Сама M.catarrhalis, прилипая к эпителию дыхательных путей одной своей стороной, создает как бы посадочную площадку для стрептококков на другой, свободной своей стороне. Но в этом есть и хорошая новость — стрептококку перестает быть доступным эпителий, и процесс начинает носить более поверхностный характер, чем мог бы быть.
Но это еще не все, M.catarrhalis умеет передавать свои факторы устойчивости, например, пенициллиназы, не только в рамках своего вида, но еще и штаммам пневмококков и гемофилл. Притом, что пневмококк — грам-плюс возбудитель, а моракселла — грам-минус. Интересная зверюшка, правда? Поэтому, если обнаружили микст-инфекцию с M.catarrhalis, про пенициллины и незащищенные аминопенициллины нужно сразу забыть.
Клинические аспекты
Когда нужно думать о моракселле? Тогда, когда мы имеем дело с детьми, престарелыми и пациентами с предрасполагающими факторами, такими как:
Что еще? Если помните, то в уже упомянутой статье мы говорили о том, что в абсолютном большинстве случаев инфекции верхних дыхательных путей вызваны вирусами. Так вот, пришло время сказать, что именно M.catarrhalis умеет их бактериально осложнять чуть ли не лучше всех, особенно у маленьких детей. У взрослых такое встречается редко, но опять же, если микроб и выделяют, то при лечении ларингитов и трахеобронхитов, которые тоже в большинстве своем начинаются как вирусные. Но при этом надо помнить, что у моракселлы почетное третье место после пневмококка и гемофилы как возбудителя инфекций дыхательных путей, особенно верхних, притом что клиническая картина вообще никак на зверя не намекнет, так как абсолютно неспецифическая. Но на всякий случай проговорим, что
Диагностические аспекты
M.catarrhalis — это еще один пример, когда мы ни в коем случае не будем лечить анализ, он же посев. При отсутствии какой-либо клиники, как и в случае со всеми остальными представителями нормальной микрофлоры, «руки прочь от антибиотиков!». А если какая-либо клиника присутствует, сначала исключаем вирусную этиологию, и только тогда, еще раз подумав, хватаемся за антибиотик.
Терапевтические аспекты или чем будем геноцидить
Что необходимо запомнить раз и навсегда — в случае заболевания, вызванного M.catarrhalis, об антибиотиках пенициллинового ряда надо забыть сразу и навсегда, так как еще в 80-х годах прошлого века эта зверюшка перестала быть к ним чувствительна на 100% и, как упомянуто выше, начала довольно щедро делиться своими пенициллиназами с пневмококками и гемофиллами. Это не микроб, а какой-то гений микробного общения.
Моракселлы устойчивы в окружающей среде, находясь в капельках слюны и мокроты, но чувствительны ко всем дезинфектантам. Ничего не напоминает? SARS-CoV-2, например. Автор очень надеется, что ошибается, и эта сладкая парочка не «поженится» ни в ближайшем, ни в отдаленном будущем.
M.catarrhalis изначально природно устойчива к триметоприму (он же ко-тримоксазол), ванкомицину и линкомицину, которые являются бактериостатиками, так что можно ответственно заявить, что «контрацепция» не подействует, необходим тотальный геноцид, то есть антибиотики с бактерицидным эффектом. Пенициллины, как мы помним, уже потеряны, поэтому остаются:
В заключение, повторимся еще раз, M.catarrhalis — зверек крайне интересный, и дай нам всем бог или кто там вместо него есть, чтобы после многомесячного, если не сказать уже годичного, антибиотикового безумия в лечении COVID-19, этот интерес оставался сугубо академическим.
Моракселла катаралис – кто это такая?
5.00 (Проголосовало: 2)
Наиболее встречающимися ЛОР-заболеваниями являются средний отит и синусит. Особенно часто эти воспаления возникают в раннем возрасте. По статистике до пяти лет ими страдают до 60% детей. Одним из возбудителей этих заболеваний является бактерия моракселла. Моракселла катаралис или Moraxella catarrhalis или Branchamella catarrhalis была выделена в начале прошлого века и не считалась патогенной до 70-х годов.
Где обитает?
В норме она живет на слизистой оболочке носа, глаз и в мочеполовой системе. Обычно никаких неприятностей эта бактерия не доставляет. Но, как любая условно патогенная флора при ослаблении иммунитета, она может стать причиной заболевания. Моракселла в 50% случаев обнаруживается у детей и в десятки раз реже у взрослых. Именно поэтому чаще всего эта бактерия встречается в посеве у детей.
Для чего необходимо взять мазок?
Обычно этот микроорганизм живет у большинства людей и никаких неприятностей не доставляет, и избавляться от него заранее, в целях профилактики, смысла нет. Однако, если именно моракселла стала причиной постоянных болезней, то без антибиотиков, скорее всего, не обойтись.
Несмотря на то, что по агрессивности воспаления моракселла уступает другим возбудителям, опасна она в основном тем, что плохо распознается и часто может лечиться неправильно. Именно поэтому не стоит пренебрегать сдачей мазка на флору. Собранный материал от пациента высеивают на специальную среду и диагностируют бактерию с помощью микроскопа.
Если лечиться, то как?
Являясь бактерией, способной продуцировать фермент β-лактамазу, моракселла устойчива к определенным видам антибиотиков, которые при ЛОР-заболеваниях назначаются чаще всего. Поэтому лабораторные исследования и консультация врача необходимы для своевременного, правильного лечения и благополучного исхода заболевания.
Помимо этого, применяется и симптоматическое лечение, которое назначит врач, учитывая течение заболевания. Только врач на основе анализов сможет правильно установить возбудителя болезни и назначить тот препарат, который вам необходим.
В филиалах «ЛОР клиники №1» высококвалифицированные специалисты-оториноларингологи проведут полный осмотр ЛОР-органов, назначат необходимые обследования и лечение, соответствующее вашему заболеванию.
АНТИБАКТЕРИАЛЬНАЯ ТЕРАПИЯ
ИНФЕКЦИЙ В ОТОРИНОЛАРИНГОЛОГИИ
Л.С. Страчунский, Е.И. Каманин
«Русский медицинский журнал», 1998; т.6, №11, стр.684-693
Эпидемиология
В доступной литературе мы не нашли современных данных о распространенности инфекций ЛОР-органов в России. Для того чтобы получить представление об их распространенности, мы экстраполировали данные, полученные в США и Западной Европе [1]. Основываясь на данных зарубежных коллег, можно считать, что ежегодно в России 10 млн человек переносят острый синусит, развившийся во внебольничных условиях.
Инфекции ЛОР-органов являются одним из ведущих показаний к назначению антибиотиков. Во Франции ежегодно выписывается более 3 млн [2], а в США около 30 млн рецептов на антибиотики по поводу ОСО [3].
Возбудители
Мы обсуждаем лечение так называемых ОРЗ или ОРВИ в связи с тем, что необоснованное назначение антибиотиков, особенно детям, при этих инфекциях является одним из ведущих факторов формирования антибиотикорезистентности.
В основе антибактериальной терапии в оториноларингологии лежит эмпирический выбор. Однако при этом надо помнить, что эмпирическая терапия должна базироваться на сведениях, полученных в проспективных исследованиях.
Планируя эмпирическую антибиотикотерапию, врач должен задать себе четыре главных вопроса:
Гемофильная палочка. Для многих оториноларингологов данный возбудитель представляется чем-то экзотическим, поскольку в большинстве микробиологических лабораторий его не выделяют. А в том случае, если это удается сделать, то результаты определения чувствительности очень часто вызывают большие сомнения. Так, из отечественных лабораторий поступают сообщения не просто о резистентности, а о высокой резистентности к цефалоспоринам III поколения. В мировой литературе такой феномен не описан. Причина ошибок заключается в высокой требовательности гемофильной палочки к агару и условиям инкубирования. Поэтому для получения достоверных данных и их воспроизводимости во всем мире принято пользоваться рекомендациями Национального комитета по клиническим лабораторным стандартам США (NCCLS). Как показано в нашей лаборатории, для определения чувствительности гемофильной палочки нельзя использовать отечественную среду АГВ.
По поводу назначения антибиотиков при ОСО полного единодушия среди специалистов нет, так как в 60 случаях из 100 выздоровление наступает без применения антибиотиков. Антибиотики действительно необходимы только одной трети детей с ОСО, у которых уничтожение (эрадикапия) возбудителя ведет к более быстрому выздоровлению, однако идентифицировать таких детей на основании клинических данных трудно, если не невозможно.
Тактика ведения детей с ОСО зависит от таких факторов, как возраст ребенка, наличие сопутствующих и фоновых заболеваний, ЛОР-анамнез, социально-культурный уровень родителей, доступность квалифицированной медицинской помощи.
Повторная оценка состояния проводится через 48-72 ч. При эффективности антибактериальной терапии все основные симптомы отита, кроме экссудации в среднем ухе, должны разрешиться. Если этого не происходит, то назначенное лечение неэффективно. В этом случае необходимо сменить антибиотик, например, вместо амоксициллина назначить aмоксициллин/клавуланат или цефтриаксон внутримышечно. При наличии показаний проводят тимпанопункцию с обязательным бактериологическим исследованием полученного материала. При гладком течении ОСО ребенка осматривают на 10-14-й день, т.е. после окончания антибактериальной терапии. Примерно у половины детей к этому времени сохраняется выпот в среднем ухе, однако это не требует продолжения антибактериальной терапии.
Как уже было сказано, ОСО является одним из основных показаний для назначения антибиотиков [7]. Однако происходит постоянная переоценка эффективности антибиотиков при этом заболевании. В настоящее время достаточно четко сформулированы три условия эффективности антибиотиков при ОСО: чувствительность возбудителя к антибиотику; концентрация антибиотика в жидкости среднего уха и сыворотке крови выше МПК для данного возбудителя; сохранение концентрации в сыворотке крови выше МПК в течение 40-50% времени между приемами препарата, что обеспечивает 80-85% эффективность [8]. Если принято решение о назначении антибиотика, препаратом выбора является амоксициллин внутрь. Из всех доступных оральных пенициллинов и цефалоспоринов, включая препараты II-III поколения, амоксициллин наиболее активен против пенициллинрезистентных пневмококков и, например, в 4 раза превосходит ампициллин. Вследствие этого нельзя распространять на амоксициллин данные о резистентности к пенициллину и ампициллину. Дополнительными его преимуществами являются в 2 раза более высокий, чем у ампициллина, уровень в крови, значительно меньшая частота нежелательных побочных реакций со стороны желудочно-кишечного тракта и удобство приема. Амоксициллин принимают 3 раза в сутки независимо от времени приема пиши, тогда как ампициллин следует принимать 4 раза в сутки, за 1 ч до или через 2 ч после еды, так как пища в 2 раза снижает биодоступность этого антибиотика.
Экссудативный (выпотной) средний отит
При хроническом среднем отите антибактериальная терапия играет вторичную роль по сравнению с местной санацией и применением ототопических препаратов. Антибиотики целесообразно применять при неэффективности местной терапии, развитии яркой картины обострения и, что чрезвычайно важно, под контролем микробиологических данных, т.е. системная терапия должна быть этиотропной [10].
Наружный отит
При локализованных формах наружного отита основным возбудителем является золотистый стафилококк. В отдельных случаях может отмечаться рожистое воспаление с вовлечением ушной раковины и наружного слухового прохода, вызванное БГСА. От этих форм следует отличать острый диффузный наружный отит («ухо пловца») и злокачественный наружный отит, которые почти всегда вызваны грамотрицательной микрофлорой и прежде всего синегнойной палочкой. При хроническом наружном отите обычно отмечается сопутствующий хронический средний отит. У таких пациентов необходимо исключить грибковую инфекцию (аспергиллы, кандида).
При злокачественной форме назначают препарат с антисинегнойной активностью. Учитывая необходимость длительных курсов терапии (4-6 нед), обосновано назначение ступенчатой терапии ципрофлоксацином (первоначально внутривенно по 400 мг 2-3 раза в день с дальнейшим переходом на пероральный прием по 500-750 мг 2 раза в день).
Тонзиллофарингит
Эпиглоттит
Острый синусит
В данной статье мы коснемся только внебольничного острого синусита, другими словами, острого синусита, развившегося у амбулаторных больных, лечение которого может осуществляться как в поликлинических, так и в стационарных условиях. Важность отграничения этой формы синусита от хронического синусита и нозокомиального синусита у больных, находящихся на искусственной вентиляции легких, связана как с высокой частотой инфекции, так и с принципиальными различиями в этиологии, патогенезе и антибактериальной терапии.
Целью антибактериальной терапии острого синусита является подавление симптомов и сокращение продолжительности заболевания, уничтожение возбудителей, что уменьшает повреждение слизистой, ведущее к хронизации заболевания. Адекватная антибиотикотерапия также предупреждает развитие внутричерепных и орбитальных осложнений.
Хронический синусит
При хроническом синусите антибиотики играют меньшую роль, чем при остром, так как основной задачей является восстановление нормальной вентиляции придаточных пазух. Антибиотики применяются при обострении хронического синусита, однако с учетом частого выделения неспорообразующих анаэробов возрастает значение препаратов с антианаэробной активностью (например, амоксициллин/клавуланат). В целом весьма желательно проводить терапию под контролем данных бактериологического исследования, особенно у пациентов, у которых отмечалась неэффективность антибактериальной терапии. При применении антибиотиков, недостаточно активных против анаэробов (например, ко-тримоксазол, фторхинолоны), их целесообразно сочетать с метронидазолом [14].
Сопутствующая терапия
Сосудосуживающие препараты, которые в зарубежной литературе называют деконгестантами, играют важную роль в устранении отека слизистой, обеспечивая тем самым улучшение дренирования и восстановление функции евстахиевой трубы и придаточных пазух носа. На протяжении десятилетий в России наиболее популярны были местные деконгестанты в связи с отсутствием на рынке препаратов для приема внутрь; кроме того, считалось, что местные средства более безопасны. Однако в последние годы взгляды на применение местных препаратов изменились.
При использовании местных деконгестантов более 5 дней развивается медикаментозный ринит. В этом отношении наиболее опасен ксилометазолин. Эффективность назальных капель снижается в связи с тем, что пациенты не владеют правильной техникой их применения, которая состоит в том, что пациент должен вводить эти капли в нос в позе Мекки и оставаться в ней в течение 2-3 мин после инстилляции капель. Очевидно, что это очень неудобно для пациентов, особенно для работающих, пожилых, инвалидов [15].
Ошибки антибактериальной терапии инфекций ЛОР-органов можно разделить на три группы.
2. Неправильный выбор препарата, доз, путей введения.
К сожалению, антибиотики нередко назначают, не задумываясь о наиболее вероятном возбудителе, его чувствительности к антибактериальным препаратам, не учитывая результаты, полученные в контролированных клинических исследованиях. Даже в амбулаторных картах можно встретить назначение типа «антибиотик внутрь». Из-за недостатка знаний многие врачи нередко отождествляют генерики ципрофлоксацина с оральными цефалоспоринами, излюбленными препаратами продолжают оставаться сульфаниламиды, в том числе «стрептоцид под язык» (!), гентамицин или линкомицин внутримышечно у амбулаторных больных.
3. Недостаточное внимание к бактериологическому исследованию.
Несмотря на то что эмпирический выбор антибиотиков составляет основу их назначения, так как за исключением стрептококкового тонзиллофарингита нельзя быстро идентифицировать возбудитель, бактериологическое исследование должно обязательно проводиться. Помимо прямой пользы для данного пациента, например, при неэффективности стартовой терапии и необходимости смены антибиотиков, ее значение состоит в получении и накоплении эпидемиологических данных о структуре возбудителей и, что наиболее важно, их чувствительности к антибиотикам. Опора на локальные данные об антибиотикорезистентности позволяет сделать эмпирическую антибиотикотерапию максимально эффективной и поставить ее на научные основы.
При лечении инфекций ЛОР-органов важно преодолеть нигилизм по отношению к применению антибиотиков, который нередко встречается среди врачей и связан с высокой частотой спонтанного выздоровления. Предпочтение следует отдавать препаратам с наиболее высокой клинической и бактериологической эффективностью, ибо инфекциями ЛОР-органов болеют многие миллионы пациентов и небольшие различия в эффективности на практике оборачиваются тысячами случаев неэффективной терапии.
Первичная (природная) активность антибиотиков против основных возбудителей инфекций ЛОР-органов
|
Дозы антибиотиков при амбулаторных инфекциях ЛОР-органов
|
* Нельзя сочетать с алюминий-, магнийсодержащими антацидами. препаратами железа, цинка.
** Не применяется.
Резистентность к антибиотикам основных возбудителей инфекций ЛОР-органов
|
Резистентность к антибиотикам основных возбудителей инфекций ЛОР-органов
|
* исключение составляет однократная инъекция цефтриаксоиа (50 мг/кг) внутримышечно.