дгэа при беременности для чего
Гормональные исследования во время беременности / Няня.ru
Нона Овсепян, врач-консультант Независимой лаборатории ИНВИТРО
Зачем необходимо контролировать уровень гормонов?
Гормоны – удивительные биологически активные вещества, которые влияют не только на состояние здоровья, но и на внутренний мир человека. Природой предусмотрено, что в женском организме сразу после зачатия активизируются специальные гормоны беременности, которые не только помогают малышу полноценно развиваться, но также настраивают будущую маму на желанное материнство, учат любить растущего внутри кроху и привыкать заботиться о нем.
В период ожидания малыша происходят серьезные изменения во всем организме женщины — особенно это касается ее гормонального фона. Изменения происходят во всей эндокринной системе. Организм будущей мамы, полностью перестраиваясь, создает условия для вынашивания и нормального развития малыша и уже с первых дней беременности начинает готовиться к родам.
Все гормональные показатели организма будущей мамы играют огромную роль — а именно, являются важнейшими показателями развития плода. Поэтому уровень гормонов в обязательном порядке контролируется лечащим врачом с помощью специальных обследований — пренатальных скринингов, которые женщине необходимо пройти как минимум 2 раза: в первом триместре (11-12 недель) и во втором триместре (16-19 недель). Разберемся, какие показатели входят в это обязательное обследование, о чем говорит повышение или понижение уровня того или иного гормона и в чем состоит их роль.
Гормоны, которые «производит» организм будущего малыша
ХГЧ. Это хорионический гонадотропин человека, гормон, который активно вырабатывается клетками хориона (оболочки плода) сразу после того, как он прикрепляется к стенке матки. «Производство» этого гормона жизненно необходимо для сохранения и поддержания беременности! Именно ХГЧ контролирует выработку основных гормонов беременности — эстрогенов и прогестерона. При серьезном недостатке ХГЧ оплодотворенная яйцеклетка отсоединяется от матки, и снова наступает менструация — иными словами, происходит самопроизвольный выкидыш. В норме концентрация ХГЧ в крови будущей мамы постоянно растет, достигая максимума к 10-11 неделе беременности, затем концентрация ХГЧ постепенно уменьшается, чтобы остаться неизменной уже до самых родов.
Тест на ХГЧ во время беременности играет огромную роль.
Во-первых, анализ на уровень ХГЧ в крови способен подтвердить, что вы станете мамой, уже на 5-6 день после зачатия. Это намного раньше и, главное, намного надежнее, чем использование обычных экспресс-тестов.
Во-вторых, тест необходим, чтобы определить точный срок беременности. Очень часто будущая мама не может назвать точную дату зачатия или же называет ее, но неправильно. Вместе с тем каждому сроку соответствуют определенные показатели роста и развития, отклонения от нормы могут свидетельствовать о возникновении осложнений.
В-третьих, уровень ХГЧ в крови способен довольно точно «рассказать» о том, правильно ли развивается ваш малыш.
Внеплановое повышение уровня ХГЧ обычно происходит при многоплодии, гестозе, приеме синтетических гестагенов, сахарном диабете у будущей мамы, а также может говорить о некоторых наследственных заболеваниях у малыша (например, о синдроме Дауна) и множественных пороках развития. Ненормально низкий уровень ХГЧ может стать признаком внематочной и неразвивающейся беременности, задержки в развитии плода, угрозы самопроизвольного аборта, хронической плацентарной недостаточности.
Однако не спешите бить тревогу: повышенные или пониженные значения также могут говорить о том, что срок беременности был изначально установлен неправильно. Правильно интерпретировать результаты анализов поможет ваш лечащий врач.
Плацентарный лактоген и свободный эстриол. Контроль уровня этих гормонов крайне важен для оценки риска развития наследственных хромосомных аномалий у будущего малыша (это синдромы Дауна, Эдвардса, Тернера, Патау, дефект нервной трубки и т.д.)
Эстрадиол вырабатывается яичниками, а во время беременности еще и плацентой. Во время беременности уровень гормона резко возрастает, и неудивительно – эстрадиол «отвечает» за нормальное течение беременности. На ранних сроках по концентрации этого гормона оценивают функционирование плаценты. Снижение уровня эстрадиола говорит о серьезной угрозе прерывания беременности.
Кстати, именно под влиянием этого гормона женщина испытывает естественное желание «свить гнездо», все обустроить и подготовить к рождению малыша. Перед родами концентрация гормона в организме будущей мамы достигает своего «пика», что также объясняется естественными причинами — эстрадиол, действуя, как сильнейшее природное обезболивающее, помогает сделать процесс рождения малыша менее болезненным.
Прогестерон — это также основной «гормон беременности», основная задача которого — сохранить беременность и создать необходимые условия для развития плода. Нормальный уровень прогестерона необходим для того, чтобы произошло само зачатие. Совместно с эстрогенами гормон способствует прикреплению оплодотворенной яйцеклетки к эндометрию и заботливо снижает повышенный тонус матки, предупреждая выкидыш. Во время вынашивания малыша прогестерон стимулирует рост и созревание молочных желез, «готовя» организм будущей мамы к грудному вскармливанию, а в психологическом плане — успокаивает ее и морально поддерживает. К сожалению, у этого гормона есть и «побочные» эффекты, знакомые каждой беременной, — это повышенная сонливость, тошнота, частое мочеиспускание, болезненность и набухание груди.
При недостатке прогестерона беременность может протекать с серьезными осложнениями. Дефицит гормона необходимо срочно восполнить, иначе увеличивается риск неразвивающейся беременности и выкидыша.
Важно! Анализ на уровень эстрадиола и прогестерона проводится как во время беременности, так и при подготовке к рождению ребенка, особенно это необходимо в тех случаях, когда у женщины уже были случаи выкидыша.
Гормоны щитовидной железы
Большую роль для развития малыша играет нормальное функционирование щитовидной железы будущей мамы. О наличии гипо- или гиперфункции железы способны также «рассказать» соответствующие гормоны (ТТГ, Т3 и Т4).
Незаменимую роль во время ожидания малыша играют также гормоны гипофиза (это эндокринная железа, расположенная в гипоталамическом отделе головного мозга). Во время родов гипофиз высвобождает в кровь гормон окситацин, который стимулирует маточные сокращения. А после родов начинается активный синтез гормона пролактина, который «отвечает» за лактацию. При недостатке пролактина женщина просто не смогла бы полноценно кормить своего малыша грудным молоком.
Кроме того, пролактин и окситацин еще называют «гормонами материнства», потому что благодаря им сердце мамы наполняется нежностью, она чувствует удовольствие от кормления и общения с ребенком, что еще больше привязывает ее к малышу. Эти гормоны, по сути, и обеспечивают волшебное «превращение» женщины в маму — под их влиянием приоритеты резко меняются, учеба, работа, карьера и личный успех отходят на второй план, а главное место в сердце женщины занимает маленькое родное существо. Считается, что чем больше у женщины этих самых «гормонов материнства», тем сильнее ее желание постоянно быть рядом с малышом, чувствовать его тепло, заботиться о нем. Однако не стоит ожидать, что это «превращение» произойдет словно по мановению волшебной палочки: в норме уровень гормонов в организме женщины меняется постепенно, так, чтобы ее психика успела без стресса подготовиться к происходящим изменениям. Главное во время беременности — приложить все усилия для того, чтобы выносить крепкого и здорового малыша.
Главный «антистрессовый» гормон организма
Дегидроэпиандростерон или ДГЭА — является гормоном с андрогенной активностью. ДГЭА отвечает за развитие вторичных половых признаков, поддержание половой функции, а также обладает анаболическим действием. 90% гормона образуется в коре надпочечников, остальные 10% синтезируется у мужчин в семенниках, у женщин в яичниках.
Предшественником ДГЭА является холестерин. В свою очередь, ДГЭА преобразуется в другие стероидные гормоны. В организме мужчин ДГЭА конвертируется в более сильные андрогены: тестостерон и андростендион; у женщин — эстроген и прогестерон. Производство гормона происходит под контролем АКТГ.
Уровни ДГЭА достигают пика в юношеском возрасте, а затем постепенно снижаются. В 70–80 лет значения ДГЭА составляют лишь 10–20% от пикового значения в пубертатном периоде.
ДГЭА во многом работает как синергетический близнец другого гормона стресса — кортизола. Это помогает организму более эффективно адаптироваться к стрессовому воздействию. Стресс может быть любым: физическим, психическим и эмоциональным, но его воздействие всегда происходит длительно. Например, учеба, которая дается человеку с трудом или изнуряющие условия на работе — могут стать источником серьезных проблем для здоровья.
Исследования показали, что снижение уровня ДГЭА связано с аллергией, воспалением, усталостью, аутоиммунными проблемами, сексуальной дисфункцией, инфекциями, бессонницей, снижением когнитивных функций, сердечно-сосудистыми заболеваниями, потерей массы костной ткани, депрессией и раком.
ДГЭА и кардиоваскулярная патология
ДГЭА оказывает защитное действие по отношению к заболеваниям сердечно-сосудистой системы. Результаты исследования, опубликованные в 2014 г в журнале Американского колледжа кардиологов, показали, что низкий уровень ДГЭА в крови связан с риском развития коронарной болезни сердца у пожилых мужчин. Ученые из Гарвардской школы общественного здравоохранения обнаружили связь между низкими уровнями ДГЭА и высоким риском развития инсульта у пожилых женщин.
ДГЭА и остеопороз
ДГЭА улучшает минеральную плотность костной ткани и тормозит остеопороз. Особенно это важно для женщин, которые находится в постменопаузе и страдают от дефицита женских половых гормонов.
ДГЭА и сексуальное поведение
Здоровые уровни ДГЭА поддерживают здоровую сексуальную жизнь. ДГЭА улучшает либидо у мужчин и женщин в равной степени.
ДГЭА и когнитивные функции
Исследования показали, что ДГЭА поддерживает здоровые когнитивные функции и настроение. Гормон поддерживает производство и функционирование нейротрансмиттеров в мозге — химических веществ, которые влияют на память и настроение.
Было обнаружено, что ДГЭА обладает регенеративной активностью по отношению к тканям мозга. Люди, страдающие от болезни Альцгеймера, имеют низкий уровень факторов роста, жизненно необходимых для нервной ткани. ДГЭА может защитить тонкие ткани мозга, сохранив их.
Люди с низким уровнем ДГЭА более восприимчивы к тревоге и депрессии.
ДГЭА и метаболический ответ на инсулин
ДГЭА предотвращает развитие сахарного диабета. Гормон позволяет клеткам более эффективно усваивать глюкозу, тем самым снижая резистентность тканей к инсулину. Как известно, это ведущая причина развития сахарного диабета 2-го типа.
ДГЭА и здоровье иммунной системы
ДГЭА имеет решающее значение для укрепления иммунной системы. При хроническом стрессе уровень кортизола падает, и иммунная система оказывается подавленной. Но здоровые уровни ДГЭА могут уравновесить это состояние.
Некоторыми исследователями было продемонстрировано, что ДГЭА играет определенную роль в борьбе с аутоиммунными состояниями, особенно с красной волчанкой.
Недостаток ДГЭА способствует ряду заболеваний и состояний, поэтому для поддержания оптимального сердечно-сосудистого здоровья и жизнеспособности на протяжении всей жизни важно следить за уровнем ДГЭА. Возможно определение гормона в образцах крови, а также в образцах слюны.
Поскольку для хорошего здоровья имеет значение правильный баланс гормонов, поэтому уровень ДГЭА сопоставляют с уровнем кортизола.
Тестирование уровня ДГЭА и сохранение гормонального баланса между стресс-гормонами является ключом успеха на пути к долголетию. Хороший уровень ДГЭА поможет почувствовать себя моложе, сильнее и увереннее.
Тестостерон при беременности. Андрогены: их образование и метаболизм при нормальной беременности. Гиперандрогения при беременности. «Мужские» гормоны при беременности.
Краткое содержание статьи
Несмотря на рост концентрации общих и свободных андрогенов у беременных женщин, большинство женщин и их младенцев женского пола не вирилизованы. Четырьмя факторами, которые могут защитить от вирилизации, являются: высокие концентрации в сыворотке SHBG, влияние прогестерона на рецепторы к андрогенам, воздействие прогестерона на активацию андрогенов в тканях-мишенях, и плацентарная ароматизация андрогенов. (См. «Защитные механизмы против вирилизации матери и плода»).
Уровень андрогенов в крови беременных женщин
Во время нормальной беременности концентрация в сыворотке крови некоторых, но не всех, андрогенов увеличивается.
Тестостерон при беременности («Мужской» гормон при беременности)
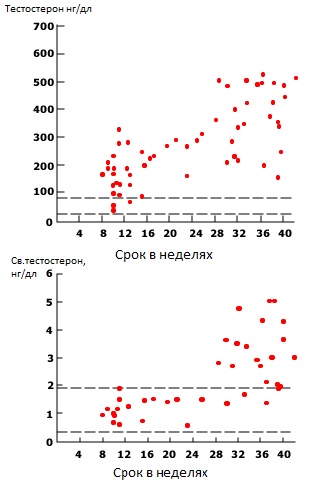
Есть несколько исследований посвященных продукции и распаду андрогенов у здоровых беременных женщин. В одном из них при обследовании пяти беременных женщин было выявлено, что темпы продукции тестостерона и дигидротестостерона у беременных и небеременных женщин совпадают. Однако преобразование тестостерона в дигидротестостерон и метаболический клиренс этих гормонов во время беременности были ниже, чего и следовало ожидать при повышенной концентрации в сыворотке SHBG.
При другом исследовании, включавшем в себя обследование 1343 женщин с одноплодной беременностью, был выявлен более низкий уровень андрогенов у женщин старше 30 лет, а так же повторнородящих (двое и более родов). В то время как с курением был связан более высокий уровень андрогенов в первой половине беременности по сравнению с более молодыми женщинами, нерожавшими и некурящими женщинами, соответственно.
Во время беременности концентрация тестостерона в сыворотке крови в три-четыре раза выше, чем в сыворотке пуповинной крови. Концентрация тестостерона в крови беременной женщины может колебаться от 100 до 140 нг/дл (от 3,5 до 4,8 нмоль/л), а в пуповинной крови средние значение 33,5 нг/мл (1,2 нмоль/л).
Свободный тестостерон при беременности
Концентрация в сыворотке свободного тестостерона во время беременности изменяется незначительно, вплоть до третьего триместра, когда она увеличивается примерно в два раза. Данное увеличение концентрации свободного тестостерона не может быть объяснено изменением концентрации SHBG и, скорее всего, может быть следствием увеличения продукции тестостерона. Источник повышенного образования тестостерона в данной ситуации не известен. Одной из возможных причин может являться то, что человеческий хорионический гонадотропин (ХГЧ) может стимулировать тека-интерстициальные клетки яичников синтезировать тестостерон, однако, концентрация ХГЧ в сыворотке крови достигает своего пика в конце первого триместра беременности и далее постепенно снижается, а концентрация свободного тестостерона увеличивается. Как показали исследования у человекообразных обезьян, одним из возможных источников тестостерона является желтое тело. Наконец, тестостерон может продуцироваться в коре надпочечников беременных женщин, параллельно с увеличением секреции материнского кортизола в конце беременности.
ДЭА-С при беременности
Концентрация дегидроэпиандростерон сульфата (ДГЭА-С) в крови матери во время беременности снижается, несмотря на увеличение его продукции в крови плода. Наибольшее снижение происходит в начале второго триместра, когда метаболический клиренс ДГЭА-С резко возрастает. У беременных женщин ДГЭА-С метаболизируется в печени, путем превращения в 16-альфа-гидрокси-ДЭА, и в плаценте, путем превращения в эстрогены.
Андростендион при беременности
Концентрация андростендиона в крови матери увеличивается во второй половине беременности.
Андростандиол глюкуронид при беременности
Концентрация в сыворотке крови у беременной женщины 3-альфа-17-бета-андростандиол глюкуронида (3а-диол-G), продукта метаболизма дигидротестостерона в волосяных фолликулах кожи, повышается во время беременности. До конца неизвестно, связано ли это с повышением активности 5-альфа-редуктазы и других андроген-метаболизирующих ферментов, или с увеличением доступности субстрата.
Уровень андрогенов в амниотической жидкости
Концентрация в амниотической жидкости тестостерона и андростендиона, в среднем, примерно в два-три раза выше, если плод мужского пола. Медиана вероятного отклонения у мальчиков составляет от 17,3 до 33,7 нг/дл (0,60 до 1,17 нмоль/л) и 5,05 до 12,98 нг/дл (0,175 до 0,45 нмоль/л) у девочек. Эта разница показателей у плодов мужского и женского пола указывает на то, что по крайней мере часть андростендиона и тестостерона в амниотической жидкости продуцируется яичками плода. Концентрация же ДГЭА-С в амниотической жидкости одинакова у плодов женского и мужского пола. Вероятно, это связано с тем, что данный гормон надпочечникового происхождения.
Уровень андрогенов в крови плода
Мало что известно о регуляции фетального тестостерона, однако предполагается, что он больше зависит от уровня материнского ХГЧ, чем от лютеинизирующего гормона (ЛГ) гипофиза плода. Концентрация ХГЧ в крови матери и плода достигает своего пика в период с 9 до 12 недель беременности, а затем постепенно снижается (концентрация материнского ХГЧ в сыворотке плода значительно ниже, чем в сыворотке самой матери: показатели плода могут варьироваться от едва уловимых до 2,5 мМЕ/мл).
Появление материнского ХГЧ в сыворотки плода совпадает с появлением клеток Лейдига (источник выработки тестостерона в яичках), что происходит на сроке около 8 недель беременности. Предполагается, что материнский ХГЧ играет существенную роль в развитии клеток Лейдига у плода и в продукции тестостерона. Пик формирования клеток Лейдига приходится на сроки от 14 до 18 недель беременности.
Гонадотропины обнаруживаются в гипофизе плода примерно в 10 недель беременности, а в фетальной сыворотке приблизительно еще через неделю. Проведенное исследование на трансгенных мышах мужского пола, а так же позднее начало выработки гонадотропина у плода подтверждает теорию, того что развитие клеток Лейдига и продукция тестостерона инициируется основном материнским ХГЧ. Кроме того, функция клеток Лейдига оказалась нормальной у мышей, лишенных ЛГ или его рецепторов.
У плодов женского полаконцентрация тестостерона в сыворотке крови низкая (около 50 нг/дл [1,7 нмоль/л] ) и на протяжении большей части беременности имеет тенденцию к снижению. Источником тестостерона, вероятнее всего, являются яичники плода, т.к. гонадотропин может стимулировать продукцию андрогенов в яичниках плода, которые в дальнейшем преобразуются в эстрогены.
Уровень андрогенов у новорожденных
У новорожденных мальчиков уровень концентрации тестостерона в пупочной артерии лишь немного выше, чем у девочек. Тем не менее, концентрация тестостерона (и андростендиона) в крови значительно увеличивается в течение первых суток жизни, особенно у мальчиков, а затем снижается в течение следующих шести дней.
Увеличение андрогенов в первый день жизни может быть ответом на выработку свободного ХГЧ.
Во время беременности другие стероиды, вырабатываемые плацентой, могут частично ингибировать действие ХГЧ на клетки плода. Снижение концентрации сывороточных андрогенов в течение первой недели жизни происходит одновременно со снижением концентрации в сыворотке крови ХГЧ.
Уровень андрогенов в плаценте
Исследования показывают, что плацента может самостоятельно синтезировать андрогены, большинство из которых превращается в эстрогены под воздействием плацентарной CYP17. Значение плацентарного синтеза андрогенов неизвестно.
Защитные механизмы против вирилизации матери и плода
Несмотря на увеличение в сыворотке крови беременных женщин концентрации общих и свободных андрогенов, большинство женщин и их детей не вирилизованы. Причинами этого являются:
Эти результаты показывают, что воздействие андрогенов плода может быть уменьшено плацентарной ароматизацией андрогенов и производством эстрогенов. Также подтверждением этой гипотезы является обнаружение вирилизации у плодов женского пола при недостаточности плацентарной ароматазы. У одного из таких младенцев, концентрация тестостерона, дигидротестостерона и андростендиона в пуповинной крови были в 26, 26 и 207 раз выше нормы, а концентрация эстрона, эстрадиола и эстриола составляли всего 0,6, 0,9 и 0,2 процента от нормы.
Тем не менее, ароматизации, как правило, недостаточно, чтобы полностью защитить плод от передачи тестостерона, и это не в полной мере объясняет отсутствие вирилизации плода. Есть доклады о беременных с лютеомами яичников, у которых выявлялись высокие концентрации дигидротестостерона в сыворотки крови, но родились здоровые девочки. Поскольку дигидротестостерон не подвергается ароматизации до эстрогенов, то при физиологически протекающей беременности плоды женского пола должны быть защищены от вирилизации снижением действия андрогенов.
Пренатальное воздействие андрогенов, находящихся в пределах нормы для беременности, скорее всего, не вызывает изменений яичников, ведущих к синдрому поликистозных яичников (СПКЯ) в подростковом возрасте.
Референтные значения 17-гидроксипрогестерона и дегидроэпиандростерон-сульфата в период гестации
Полный текст:
Аннотация
Гиперандрогения оказывает существенное негативное влияние на течение беременности. Определение уровня 17-гидрокси-прогестерона и дегидроэпиандростерон-сулъфата в качестве маркеров адреналовой гиперандрогении у беременных без учета особенностей метаболизма гормонов в период гестации способствует гипердиагностике неклассических форм врожденной дисфункции коры надпочечников и влечет за собой неадекватную терапевтическую тактику. Изолированное повышение дегидроэпиандростерон-сулъфата не сопровождается увеличением частоты андрогензависимых осложнений беременности.
Ключевые слова
Для цитирования:
Суплотова Л.А., Храмова Е.Б., Старкова О.Б., Суплотов С.H., Южакова Н.Ю., Фомина С.В. Референтные значения 17-гидроксипрогестерона и дегидроэпиандростерон-сульфата в период гестации. Проблемы Эндокринологии. 2007;53(4):19-21. https://doi.org/10.14341/probl200753419-21
For citation:
Suplotova L.A., Khramova E.В., Starkova О.В., Supbtov S.N., Yuzhakova N.Yu., Fomina S.V. The reference values of 17-hydroxyprogesterone and dehydroepiandrosterone in the gestational period. Problems of Endocrinology. 2007;53(4):19-21. (In Russ.) https://doi.org/10.14341/probl200753419-21
В последние годы в России отмечаются устойчивая тенденция снижения рождаемости и высокая частота невынашивания беременности, что усугубляет демографическую ситуацию, характеризующуюся отрицательным коэффициентом естественного прироста. Таким образом, проблема репродуктивных потерь приобретает не только медицинское, но и социально-демографическое значение. В этой связи актуальными представляются вопросы диагностики и коррекции состояний, препятствующих зачатию и вынашиванию беременности.
В спектре гормональных нарушений, приводящих к невынашиванию беременности, значительное место занимает гиперандрогения. Одной из наиболее частых причин гиперандрогении надпочечникового генеза является врожденная дисфункция коры надпочечников (ВДК.Н), распространенность неклассической формы заболевания достигает 4% в общей популяции. При неклассических формах врожденной ферментопатии клинические симптомы минимальны, а наступившая беременность становится сильнейшим провоцирующим фактором, впервые выявляющим скрытую дисфункцию стероидогенеза [1]. В этом случае обследование женщины и верификация диагноза проводятся не на этапе планирования беременности, а уже в I триместре. Своевременная диагностика заболевания и патогенетическая терапия позволяют сократить репродуктивные потери на ранних сроках гестации [2, 5].
Гормональными маркерами адреналовой гиперандрогении являются повышенные уровни 17- гидроксипрогестерона (17-ОНР) и дегидроэпиандростерон-сульфата (ДЭГА-С). В справочной литературе представлены нормативы концентрации ДГЭА-С в зависимости от возраста и 17-ОНР в зависимости от фазы менструального цикла. Сложность в адекватной оценке уровней ДГЭА-С и 17- ОНР во время беременности возникает ввиду особенностей гормональной секреции плаценты и высокой активности адреналового стероидогенеза матери и плода. Так, продукция ДГЭА-С надпочечниками плода на порядок превышает материнскую секрецию гормона (200 и 30 мг/сут соответственно) [3]. Существенное влияние на концентрацию ДГЭА-С у беременной оказывает активность фето- плацентарного комплекса, использующего гормон в качестве субстрата для синтеза эстриола [5]. Возрастающая концентрация 17-ОНР в период гестации отражает физиологическую активацию стероидогенеза во 2-й половине беременности [6]. Однако производители лабораторных тест-систем предлагают единые референтные интервалы (РИ) маркеров гиперандрогении для всего периода гестации, не учитывающие также возрастные особенности гормональной секреции. Неверная интерпретация биохимических маркеров адреналовой гиперандрогении в период гестации приводит к гипердиагностике неклассической формы ВДК.Н и влечет за собой необоснованное широкое применение глюкокортикостероидной терапии у беременных.
Цель исследования: разработать и обосновать РИ уровней 17-ОНР и ДГЭА-С у беременных и оценить предикторную роль высокого уровня гормонов в диагностике андрогензависимых осложнений беременности.
Материалы и методы
Согласно рекомендациям кафедры акушерства и гинекологии Тюменской государственной медицинской академии при поддержке Управления здравоохранения Тюмени с 2002 г. всем беременным женщинам, имеющим отягощенный репродуктивный анамнез и угрозу прерывания беременности, выполняется исследование уровней ДГЭА-С и 17-ОНР для исключения гиперандрогении надпочечникового генеза. За период с 2002 по 2004 г. концентрация ДГЭА-С определена у 3869, а концентрация 17-ОНР — у 424 из 11 260 беременных. На наш взгляд, столь значительные материальные и интеллектуальные затраты на скрининг требуют клинического обоснования. У 72% обследованных беременных концентрация ДГЭА-С превышала рекомендованный лабораторный норматив.
Возможность диагностики неклассической формы ВДКН в период гестации с учетом существующих и разработанных в исследовании референтных уровней метаболитов стероидного синтеза рассматривалась при ретроспективном анализе течения беременности у 460 женщин, отобранных методом случайной выборки из группы обследованных на сывороточные маркеры гиперандрогении. Критерий исключения — наступление беременности вследствие экстракорпорального оплодотворения или стимуляции овуляции. Средний возраст женщин в группе составил 26,8 ± 4,6 года. Большинство из них (89,6%) русские. При клиническом осмотре все беременные имели женский фенотип без признаков маскулинизации. Наиболее частыми ан- дрогензависимыми осложнениями гестации в исследуемой группе женщин были хроническая маточно-плацентарная недостаточность (ХМПН — 91,7%), угроза прерывания беременности (80,7%) и истмико-цервикальная недостаточность (ИЦН — 15,7%).
С целью определения РИ ДГЭА-С и 17-ОНР для периода гестации одномоментно обследовано 234 женщины в различные сроки беременности — от 5 до 36 нед. Исследование проводили методом случайной выборки, забор крови осуществляли согласно Хельсинкской декларации 1975 г. при условии получения информированного согласия. Критерии исключения: отягощенный репродуктивный анамнез, наличие угрозы прерывания беременности, клинические признаки гиперандрогении при объективном осмотре, прием гормональных препаратов, а также хроническая соматическая патология.
Результаты и их обсуждение
Рассматривая беременность как провоцирующий фактор, впервые выявляющий скрытую дисфункцию стероидогенеза, а гиперандрогению как фактор риска репродуктивных потерь, в исследовании предпринята попытка оценить значимость изменений уровней ДГЭА-С и 17-ОНР в формировании андрогензависимых осложнений периода гестации.
У 86,5% из 460 обследованных женщин уровень ДГЭА-С превысил предлагаемые нормативные значения (0,2—1,2 мкг/мл), что отражает общую тенденцию высокой концентрации аналита среди беременных. Выявлена обратная пропорциональная зависимость между уровнем гормона и сроком беременности, что не учитывается в инструкциях к лабораторным тест-системам. Различие уровня ДГЭА-С в I—III триместрах беременности оказалось статистически значимо: 2,3—1,7 и 1,5 мкг/мл соответственно (р 0,05). Референтный уровень 17-ОНР в III триместре соответствует лабораторной норме для данного срока гестации. Верхние границы РИ ДГЭА-С и 17-ОНР (97 персентили) использовали в качестве лабораторной нормы.
Для подтверждения обоснованности предложенных изменений референтных значений ДГЭА-С для беременных, проведен сравнительный анализ частоты осложнений в период гестации в 3 группах женщин в возрасте до 30 лет: 1-я (п = 21) — беременные с ДГЭА-С в I триместре от 0,2 до 1,2 мкг/мл (лабораторная норма, используемая в настоящее время); 2-я (л = 196) — беременные с ДГЭА-С в I триместре от 1,21 до 3,2 мкг/мл (интервал между верхней границей существующей лабораторной нормы и верхней границей РИ гормона в I триместре, определенного для здоровой популяции беременных женщин Тюмени); 3-я (л = 94) — беременные с ДГЭА-С крови в I триместре более 3,21 мкг/мл (гормональные показатели, превышающие РИ для I триместра, определенный для здоровой популяции беременных женщин Тюмени).
В исследовании не установлены достоверные различия в клинических особенностях течения беременности у женщин 1-й и 2-й групп (р > 0,05). Это свидетельствует о возможности увеличения референтного уровня ДГЭА-С до 3,2 мкг/мл и использовании его в качестве лабораторной нормы у женщин до 30 лет (табл. 2).
Смещение верхней границы нормы до 3,2 мкг/мл позволяет исключить адреналовую гиперандроге- нию у наиболее многочисленной 2-й группы обследованных женщин и избежать таким образом необоснованного назначения глюкокортикоидной терапии.
Аналогичные результаты получены при сравнительном анализе течения беременности и родов у женщин в возрасте старше 31 года (табл. 3) Повышение верхней границы нормы ДГЭА-С до референтного уровня, определенного для данного возраста (2,5 мкг/мл), также не сопровождалось возрастанием частоты андрогензависимых осложнений беременности и родов.
Полученные результаты подтверждаются путем построения математической модели по оценке вероятности развития осложнений гестационного периода в зависимости от уровня ДГЭА-С в I триместре беременности. Изолированное повышение уровня ДГЭА-С до 3,2 мкг/мл и более не увеличивает шансы развития андрогензависимых осложнений у беременных в возрасте до 30 лет. У женщин старше 31 года уровень ДГЭА-С более 2,5 мкг/мл лишь незначительно повышает шансы развития ИЦН (х 2 = 5,71; р = 0,017; ОШ = 3,94).
Особенности течения беременности в 3 группах женщин до 30 лет

