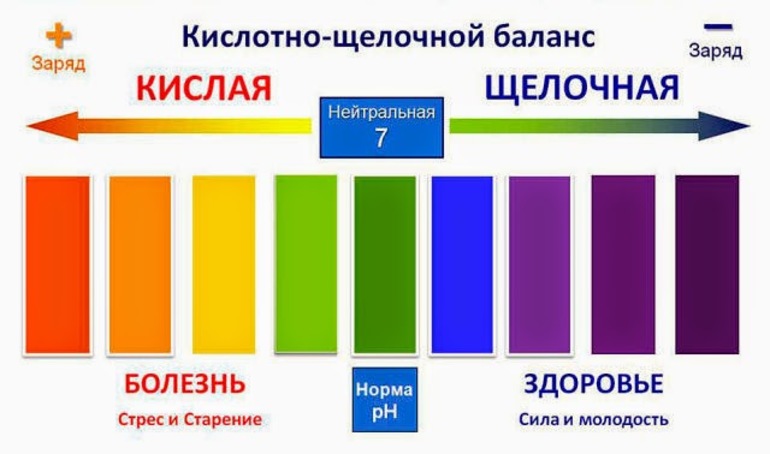
для чего нужен водородный показатель
Теоретические основы
Вода является средой, в которой растворяются органические и неорганические химические вещества, и обладает способностью распадаться на ионы. Одна молекула отдает свой протон другой, поэтому в воде постоянно находится некоторое количество положительно заряженных ионов водорода H и отрицательно заряженных гидроксид-ионов OH. Этот процесс называется электролитической диссоциацией.
Говоря об ионе водорода, делается упрощение, так как на самом деле положительно заряженный ион в воде — это ион гидроксония H3O. Он образуется из целой молекулы воды и протона, оторванного от другой молекулы. Чем больше таких ионов в воде, тем больше и ее кислотность.
Ионы очень подвижны и постоянно переходят от одной молекулы к другой. Таким образом, процесс распада и процесс соединения в новую молекулу идут постоянно и уравновешивают друг друга, т. е. диссоциация воды находится в равновесии.
С. Сёренсен руководил химико-физиологической лабораторией при пивоваренном заводе Carlsberg, где разработал шкалу для измерения показателя pH. На ее основе были созданы специальные приборы: pH-метры, которые применяются для измерения кислотности растворов и жидкостей в промышленности, и ацидогастрометры для диагностики желудочно-кишечных заболеваний в медицине.
Важно не путать pH с понятиями кислотности и щелочности. Главное различие заключается в том, что pH — это показатель не количества, а активности.
Он отражает степень кислотности или щелочности среды, а не количественное содержание в воде химических веществ. В разбавленных растворах мера активности эквивалентна концентрации, поэтому при определенном допущении один термин заменяют другим.
Влияние pH на свойства среды
При попадании в воду многих химических соединений происходит их гидролиз. Растворяемое вещество распадается на катионы и анионы, которые могут соединяться с ионами, получившимися в результате диссоциации воды. При этом получается смещение равновесия диссоциации воды. Показатель pH определяет, в какую сторону оно произошло. Если pH 7 — щелочная.
Показатель pH влияет на протекание химических реакций как на производстве, так и в природе и является универсальным показателем состояния среды. С помощью его контроля производят все виды горючего, краски, удобрения, средства личной гигиены и косметику. В пищевой промышленности проверяется качество изготовления напитков, молокопродуктов, изделий из злаков. Все живые обитатели природных почв и вод могут жить только при определенных значениях водородного показателя, от него же зависит и урожайность многих растений, поэтому ведется наблюдение за pH в почвоведении и земледелии, особенно в гидропонике.
При этом обычно необходимо поддерживать постоянное значение pH в течение длительного времени. Для этого используют так называемые буферные растворы. Они представляют собой смеси слабого основания и его соли или слабой кислоты и ее соли, в которых мера активности ионов водорода постоянна и устойчива.
Измерение водородного показателя
Формулы для расчета pH зависят от того, к какому классу относится химическое вещество, входящее в исследуемый раствор, и приведены в специальных справочниках. Более точное значение получают другими методами. Цели и условия проведения исследований определяют, как будет измеряться водородный показатель.
Индикаторные способы
Приблизительно оценить меру активности ионов водорода можно с помощью кислотно-основных индикаторов. Такие вещества обычно относятся к органическим соединениям и имеют свойство изменять свой цвет в разных средах:
Изменение происходит для каждого индикатора в своём диапазоне кислотности, обычно составляющем 1—2 единицы. При этом методе результат можно получить быстрый и наглядный при небольших затратах, но недостаточно точный, с большой погрешностью при исследовании очень слабых растворов, окрашенных или мутных вод. Используется, когда нужно найти предварительное определение pH.
Более широкий диапазон и выше точность у универсального индикатора. Он соединяет в себе несколько индикаторов и градуируется в соответствии со значениями pH от единицы до десяти. Соответствие значения водородного показателя и цвета:
Аналитический объемный метод
Кислотно-основное титрирование — метод определения водородного показателя среды с помощью так называемых титрантов. В основном для этого используются сильные кислоты (серная, соляная) и сильные щелочи (едкий калий, каустическая сода).
Раствор-титрант добавляют в исследуемую жидкость по каплям. При этом они вступают в химическую реакцию. Когда она завершается, наступает точка эквивалентности, т. е. момент отчетливого изменения окраски исследуемого раствора. По установленному в результате опыта объему титранта, необходимому для получения точки эквивалентности, и известному значению его концентрации можно рассчитать pH с высокой точностью.
Измерительный прибор pH-метр
Ионометрический метод, при котором кислотный показатель можно измерить с помощью специализированного прибора — pH-метра, является наиболее точным (до сотых от единицы pH), удобным и имеет широкий диапазон измерения. PH-метр представляет собой милливольтметр, способный измерять разность потенциалов со стеклянных электродов. У него также есть система пересчета напряжения в pH.
В исследуемый раствор погружают индикаторный электрод и электрод сравнения, замыкая таким образом гальваническую цепь. Величина электродвижущей силы в ней зависит от активности ионов H+ в растворе, т. е. является функцией только его pH. Индикаторный электрод состоит из стеклянной трубки, заполненной специальной суспензией в растворе соляной кислоты, и погруженной в нее серебряной проволоки.
Полезный сигнал возникает на границе соприкосновения раствора и индикаторного электрода и передается через металлический проводник на вход pH-метра. Таким способом можно измерять pH любых жидкостей, в том числе непрозрачных и цветных.
Специализированный прибор, применяемый в медицине для исследований pH жидкостей желудочно-кишечного тракта, называется ацидогастрометром. Включает в себя регистрирующий блок и один или несколько зондов. Для измерения уровня pH таких биологических жидкостей, как слюна и моча, применяются электронные pH-метры.
Кислотно-щелочной баланс человека
Организмом человека вырабатываются разные жидкости, каждая из которых должна иметь определенное значение pH. Отклонение в ту или иную сторону может привести к развитию множества серьезных заболеваний. Вовремя обнаруженные изменения можно исправить, если повысить или понизить кислотность потребляемых продуктов и питьевой воды. Механизм регулирования пропорционального соотношения кислот и щелочей в клеточных и межклеточных жидкостях называют кислотно-щелочным балансом (равновесием). По значению pH можно определить, в каком состоянии находятся многие органы человека.
На pH почек и печени оказывают влияние не только метаболические процессы в самом организме, но также пища и вода. Излишнюю кислотность потребленных продуктов организм выводит через мочу. Низкий уровень pH мочи говорит о том, что почки работают на пределе. Когда излишняя кислота не может быть выведена из организма естественным путем, она скапливается в подкожной жировой прослойке, имеющей кислотный pH. Это приводит к излишнему весу. В борьбе с этим явлением помогает щелочная вода, снижая нагрузку на почки.
В желудке среда резко кислая, в момент пищеварения pH равен 1,8−3. Вопреки распространненому мнению, причиной таких неприятных симптомов, как изжога и дискомфорт в желудке, является пониженная, а не повышенная кислотность желудочного сока. Нормальный уровень pH создает благоприятные условия для развития правильных бактерий и запускает механизм переваривания пищи, а болезнетворные микроорганизмы и гельминты расщепляются пищеварительными ферментами.
pH крови организм поддерживает в постоянном состоянии на уровне 7,4—7,45. Малейшее отклонение его от нормы может привести к тяжелым последствиям для человека. При понижении pH ниже 7,35 возникает ацидоз. При превышении нормы — алкалоз. Это не самостоятельные заболевания, они свидетельствуют о нарушениях в работе легких, почек, печении. Такие состояния сопровождаются очень опасными для здоровья симптомами, приводящими иногда даже к коме. По мнению врачей, ацидоз переносится легче алкалоза.
Кровеносные сосуды питают слюнные железы, поэтому за уровнем pH крови можно следить по pH слюны. Поддержание кислотно-щелочного баланса в кровеносной системе — это важнейшая функция организма человека. Внешние факторы не оказывают влияния на pH крови, он регулируется только внутренними механизмами тела человека:
Таким образом, хотя кислотный показатель крови совершенно не подвержен внешнему влиянию, механизмы его поддержания на нужном уровне имеют зависимость от того, чем человек питается и какую воду пьет. Мясо и молоко повышают общую кислотность организма, а зелень и зеленые овощи лучше всего нейтрализуют ее. Кислотность и щелочность различных пищевых продуктов можно узнать из специальных таблиц. Оптимальное значение pH для воды находится в пределах от 6 до 9.
Придерживаясь принципов правильного питания для поддержания кислотно-щелочного равновесия в своем организме, человек надолго сохранит молодость, красоту и здоровье.
Водородный показатель воды
Из этой статьи вы узнаете:
Про водородный показатель воды мало кто задумывается, а зря. Это основной параметр, на который нужно ориентироваться, если здоровье небезразлично. Вода с низким pH здорово влияет на кожу, состав крови, иммунитет и общее состояние человека. Можно даже ничем не болеть, но чувствовать себя разбитым – все это действие воды с низким водородным показателем.
Чтобы такого не допустить, мы подготовили для вас шпаргалку про норму pH, как его определить в домашних условиях без походов по лабораториям, а также как потом повысить. Не пренебрегайте описанными ниже советами и рекомендациям, это важно для вашего же здоровья.
Суть водородного показателя воды
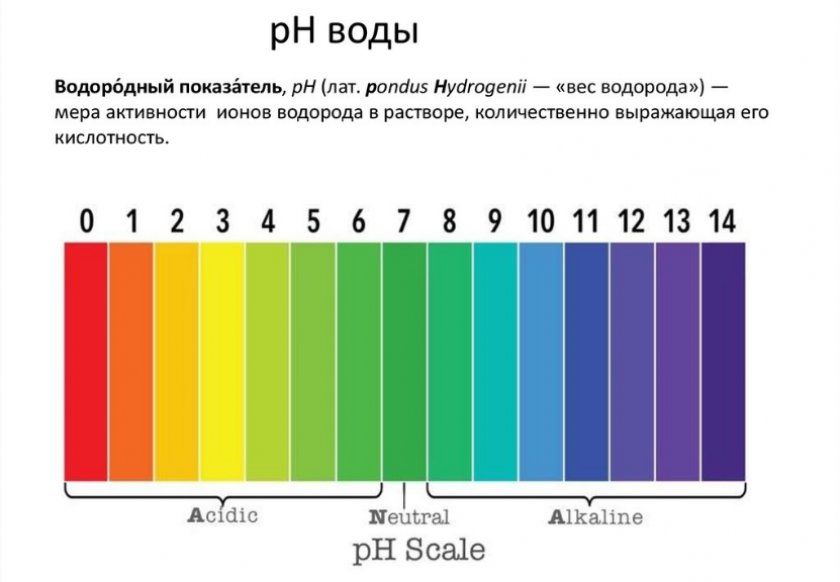
Для речной воды водородный показатель (pH) варьируется между значениями 6,5–8,5, в дождевой воде и талом снеге – 4,6–6,1, в болотной жидкости – 5,5–6,0, в морской воде – 7,9–8,3.
Согласно установленным требованиям к составу воды в пунктах питьевого водопользования, водных объектах, в зонах рекреакции и в водоемах рыбохозяйств величина водородного показателя (pH) не может выходить за пределы допустимого интервала значений 6,5–8,5.
Какую воду необходимо пить, чтобы быть здоровым?
практикующий врач терапевт-диетолог, натуропат
Сразу после регистрации вы получите подборку исследований:
Старение: остановить нельзя смириться К каким выводам пришли ученые 21 века, изучая воду и ее способность продлевать молодость
На самом деле, мы ничего не знаем о воде Важная информация для продления молодости, которую нам могли рассказать еще в школе
В зависимости от водородного показателя воды все природные источники влаги делят на семь групп.
Группы природных вод в зависимости от водородного показателя (рН):
Группа
Примечание

Постоянной величиной является водородный показатель (рН) крови человека – 7,41–7,45 – слабощелочная среда. Организм в течение всей жизни поддерживает константу крови с помощью бикарбонатов Са и Mg, что явно прослеживается исходя из данных вышеприведенной таблицы. При этом все выделения организма являются кислыми. Тело на протяжении всей жизни избавляется от кислот. Кислыми являются моча и пот. С выдохом мы выделяем углекислоту. Закисление жидкостей организма, таких как лимфа, межклеточное пространство и т. д., недопустимо. Однако щелочными напитками злоупотреблять не стоит. К таким относят жидкости, водородный показатель которых больше 8,5 (смотрите таблицу).
Что закисление организма (ацидоз), что защелачивание (алкалоз) одинаково опасны, а значит, необходимо поддерживать ту золотую середину, которая предопределена природой. Для достижения оптимальных показателей крови нам необходима вода с бикарбонатами Са и Mg. Эта вода имеет для нашего организма оптимальный водородный показатель.
Когда ионов Са и Mg поступает с водой больше, чем это необходимо на данный момент, организм их изымает и откладывает в запас, в кости (конечно, если минералы имеют органическое происхождение), а при первой необходимости достает. Однако организму непосильно откладывание в запас ионов Na (натрия). Поэтому длительное употребление щелочной воды на основе карбонатов и гидрокарбонатов натрия (пищевая сода) вредно для здоровья. Под щелочными водами подразумевают и те, которые получают на основе электроактивации.
Влияние низкого водородного показателя на организм человека
Система кровоснабжения
При закислении крови происходит слипание эритроцитов, их активность снижается, так же как способность доставлять кислород, на 20–30 %. Но даже повышение водородного показателя крови всего на 0,15 единицы рН увеличивает перенос кислорода кровью до 60 %.
Практикующий врач терапевт- диетолог, натуропат
Иммунная система

Для иммунитета оптимальными показателями кислотности признаны значения 7,41–7,45. При данных показателях иммунитет может функционировать полноценно. При таком значении кислотности максимально активно подавляется патогенная микрофлора. Все обменные процессы при поддержании подобных значений рН в организме протекают идеально.
Болевые ощущения
Боль – сигнализирует о том, что понижение уровня водородного показателя (рН) в конкретном месте в ближайшее время может обернуться клеткам кислотными ожогами. Если боль не вызвана травмой или инфекцией, это может быть сигналом недостатка щелочной воды в той области, где эта боль ощущается. Другими словами, при помощи боли организм подает сигналы о необходимости щелочной воды для нейтрализации и вымывания кислотных отходов из пораженного обезвоживанием места.
Остеопороз
Наш организм поддерживает необходимый уровень водородного показателя (рН) с помощью ионов кальция. Когда кальция не хватает, он начинает вымываться из костей и суставов, что провоцирует развитие остеопороза. Из-за этого разрушаются зубы, выпадают волосы, расслаиваются ногти. Но этот процесс обратимый и поддается лечению.
Состояние кожи
По величине водородного показателя и его воздействии на кожу различают воды: кислые (pH 3,5–6,8) вызывают свертывание белков, уплотняют эпидермис, оказывает дубящее действие на кожу; нейтральные (pH 6,8–7,2); щелочные (pH 7,2–8,5) способствуют набуханию кожных коллоидов (коллагена) и разглаживанию морщин, отторжению поверхностного ороговевшего эпителия, повышению эластичных свойств кожи.
3 метода определения водородного показателя
Вам необязательно проводить лабораторный анализ для определения водородного показателя питьевой воды. Достаточно пользоваться одним из распространенных индикаторов, чтобы понять, нуждается ли жидкость в дополнительной обработке.
1. Лакмусовая бумажка
Самый простой и дешевый способ определения водородного показателя pH воды – лакмусовая бумага. Если значение отличается от нейтрального в большую или меньшую сторону, индикатор при контакте с водой меняет цвет. Это возможно благодаря специальной пропитке красящими веществами, которые вступают с водой в реакцию. Лакмусовая бумага пропитана более полутора десятками разных красителей природного происхождения (вытяжки из растений и лишайников).
Если бумага контактирует с щелочной средой, ее цвет меняется на синий, попадая в кислотную среду, краснеет. Разработана специальная цветовая шкала для точного определения pH воды.
2. pН-метр
Когда необходимы точные данные водородного показателя жидкости, понадобится прибор под названием pH-метр. Его стоимость на порядок выше лакмусовых полосок, но он определяет значение кислотности воды с точностью до сотых долей.
Прибор может быть бытовым, а может лабораторным. Конечно, в условиях квартиры или офиса удобнее применять бытовой pН-метр. Они подразделяются на группы в зависимости от ряда параметров:
показателей точности получаемых значений;
наличия или отсутствия влагозащиты;
наличия автоматической калибровки.
Калибровка прибора осуществляется с помощью буферных растворов.
Рекомендация: при использовании прибора в домашних условиях имеет смысл приобретение измерителя с автоматической калибровкой.
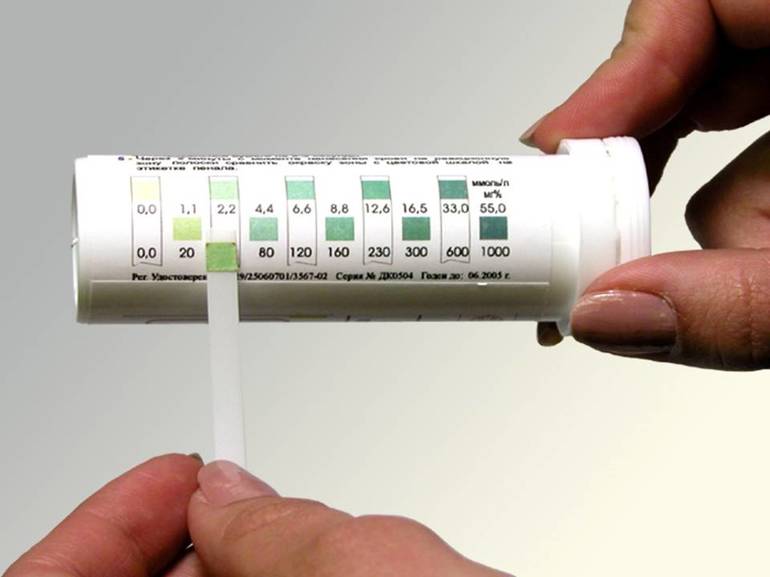
3. Тест-полоски для определения pH
Для быстроты и удобства определения водородного показателя воды можно пробрести специальные тест-полоски. Они есть в наличии в обычных зоомагазинах и предназначены для определения уровня кислотности в аквариумах.
С помощью тест-полоски можно за секунду получить результат уровня pH воды. Для этого полоску опускают в водопроводную воду, после чего влажная часть бумаги меняет цвет на глазах.
Более того, тест-полоски можно сделать своими руками. Вам достаточно в течение 30 минут отваривать краснокочанную капусту и около 10 минут вымачивать в полученном растворе принтерную бумагу. Когда бумага высохнет, нужно капнуть на нее кислотой, и цвет изменится на ярко-красный, если капнуть щелочью, бумага пожелтеет.
Способы повысить водородный показатель воды
Пищевая сода
Самый легкий способ сделать воду более щелочной – добавить в нее пищевую соду. Бикарбонат натрия – он же привычная нам пищевая сода – щелочной продукт с уровнем pH = 9. При необходимости подщелачивания воды, добавьте в нее пищевую соду и энергично встряхните до полного растворения бикарбоната натрия. Все, вода готова к употреблению, пищевая сода сделает свое дело. Некоторые специалисты утверждают, что увеличения эффективности соды для превращения воды в щелочную ее нужно прокалить.
Использование пищевой соды будет полезно тем, кто страдает изжогой и имеет другие нарушения функций желудка. Однако если у вас есть проблемы с почками, диабет или другие серьезные заболевания, перед употреблением воды с содой необходимо проконсультироваться с врачом. При ощелачивании воды и пищи с помощью бикарбоната натрия общее поступление натрия в организм увеличивается, что может быть опасным.
Лимон
Чтобы сделать воду щелочной, можно выжать в нее сок лимона. Да, лимоны кислые, но при этом они содержат анионы. Внутри организма, после обработки желудочным соком, лимонная вода становится щелочной.

Возьмите кувшин с водой и один лимон. Нарежьте фрукт на восемь частей и сложите в кувшин. Нет необходимости выжимать из кусочков сок, ведь вы их сложите в воду. Кувшин накройте салфеткой или крышкой и оставьте на 8–12 часов при комнатной температуре. Спустя определенное время вода будет готова. Она имеет освежающий вкус, калий в составе подпитает мозг, а кальций укрепит кости.
Лучший период для употребления лимонной воды – перед сном.
Капли рН
Можно пойти самым простым путем и купить в аптеке специальные капли pH. Они состоят из высококонцентрированных щелочных минералов. В комплекте с бутылочкой должна быть инструкция, где указано, сколько капель необходимо для ощелачивания определенного количества воды.
Капните нужное количество капель в вашу воду, хорошо встряхните или перемешайте, после чего используйте по назначению. Капли pH продают в интернет-магазинах или аптеках. Имейте в виду, что снижение pH обойдется дороже, в пределах 6–20 долларов.
Ощелачивание воды после фильтра обратного осмоса
Сделать водопроводную воду щелочной можно с помощью фильтра обратного осмоса, оснащенного модулем-минерализатором. Очистная конструкция может быть профессиональной, установленной в вашем доме, или подключенной к крану в квартире. Идеально подходит как тем, кто ищет хороший способ очищения и фильтрации воды, так и тем, кто желает установить в доме источник щелочной жидкости. Работа этого фильтра заключается в использовании осмотического давления и микроскопических фильтрующих мембран, через которые проходят только кислород и водород.
Протекая через эту систему под давлением, вода фильтруется через несколько мембран и из нее удаляются все загрязнения. Проходя через угольный фильтр, вода очищается от всех пигментов и запахов. В норме сама система обратного осмоса либо не меняет рН водопроводной воды, либо понижает. Именно с этой проблемой и справляется минерализатор, насыщающий жидкость солями кальция и магния, за счет чего она становится щелочной.
Наряду с ионизатором эта система очистки для воды имеет более высокую стоимость.
Ионизатор воды

Когда есть стремление к наличию в свободном доступе щелочной воды, лучший способ организовать это – установить ионизатор. Его необходимо закрепить к раковине, и он будет снабжать владельцев водой двух типов: ионизированной (щелочной) и окисленной (кислотной). Щелочная H2O используется для питья и приготовления пищи.
Окисленная H2O выходит из шланга отдельно и может быть использована для стерилизации посуды, рук или сантехники, обеззараживания поверхностей в ванной комнате.
Процесс разделения жидкости проходит в камере электролиза. В ней положительные ионы притягиваются к отрицательным электродам, в то время как анионы (отрицательные ионы) накапливаются около положительных электродов под действием электрического тока.
Вышеописанный процесс называется электролизом, и вода делится на живую и мертвую – щелочную и кислотную соответственно. Будьте готовы к тому, что устройство займет место у раковины, если это не будет профессиональная установка для всего дома.
От значений водородного показателя воды зависит самочувствие человека. Обращайте внимание на любые отклонения этой величины от нормы. Каждая из них указывает на наличие проблем в водопроводе. Определить pH питьевой воды можно с помощью простой лакмусовой бумажки или pH-метра. Полученный результат укажет на безопасность используемой жидкости.
Водородный показатель кислотности (рН)
Водородный показатель, pH (лат. pondus Hydrogenii — «вес водорода», произносится «пэ аш») — мера активности (в сильно разбавленных растворах эквивалентна концентрации) ионов водорода в растворе, которая количественно выражает его кислотность. Равен по модулю и противоположен по знаку десятичному логарифму активности водородных ионов, которая выражена в молях на один литр:

Понятие водородного показателя введено датским химиком Сёренсеном в 1909 году. Показатель называется pH (по первым буквам латинских слов potentia hydrogeni — сила водорода, либо pondus hydrogeni — вес водорода). В химии сочетанием pX обычно обозначают величину, которая равна lg X, а буквой H в этом случае обозначают концентрацию ионов водорода (H + ), либо, вернее, термодинамическую активность гидроксоний-ионов.
В чистой воде при 25 °C концентрации ионов водорода ([H + ]) и гидроксид-ионов ([OH − ]) оказываются одинаковыми и равняются 10 −7 моль/л, это четко следует из определения ионного произведения воды, равное [H + ] · [OH − ] и равно 10 −14 моль²/л² (при 25 °C).
Если концентрации двух видов ионов в растворе окажутся одинаковыми, в таком случае говорится, что у раствора нейтральная реакция. При добавлении кислоты к воде, концентрация ионов водорода возрастает, а концентрация гидроксид-ионов понижается, при добавлении основания — напротив, увеличивается содержание гидроксид-ионов, а концентрация ионов водорода уменьшается. Когда [H + ] > [OH − ] говорится, что раствор оказывается кислым, а при [OH − ] > [H + ] — щелочным.
Чтоб было удобнее представлять, для избавления от отрицательного показателя степени, вместо концентраций ионов водорода используют их десятичный логарифм, который берется с противоположным знаком, являющийся водородным показателем — pH.

Немного меньшую популяризацию имеет обратная pH величина — показатель основности раствора, pOH, которая равняется десятичному логарифму (отрицательному) концентрации в растворе ионов OH − :
как во всяком водном растворе при 25 °C 

Значения pH в растворах различной кислотности.
Существует несколько методов определения значения pH растворов. Водородный показатель приблизительно оценивают при помощи индикаторов, точно измерять при помощи pH-метра либо определять аналитическим путём, проводя кислотно-основное титрование.
0,001 моль/Л HCl при 20 °C имеет pH=3, при 30 °C pH=3,
0,001 моль/Л NaOH при 20 °C имеет pH=11,73, при 30 °C pH=10,83,
Влияние температуры на значения pH объясняют разчной диссоциацией ионов водорода (H + ) и не есть ошибкой эксперимента. Температурный эффект нельзя компенсировать за счет электроники pH-метра.
Роль pH в химии и биологии.
Кислотность среды имеет важное значение для большинства химических процессов, и возможность протекания либо результат той или иной реакции зачастую зависит от pH среды. Для поддержания определённого значения pH в реакционной системе при проведении лабораторных исследований либо на производстве применяют буферные растворы, позволяющие сохранять почти постоянное значение pH при разбавлении либо при добавлении в раствор маленьких количеств кислоты либо щёлочи.
Водородный показатель pH часто применяют для характеристики кислотно-основных свойств разных биологических сред.
Для биохимических реакций сильное значение имеет кислотность реакционной среды, протекающих в живых системах. Концентрация в растворе ионов водорода зачастую оказывает влияние на физико-химические свойства и биологическую активность белков и нуклеиновых кислот, поэтому для нормального функционирования организма поддержание кислотно-основного гомеостаза является задачей исключительной важности. Динамическое поддержание оптимального pH биологических жидкостей достигается под действием буферных систем организма.
В человеческом организме в разных органах водородный показатель оказывается разным.
Некоторые значения pH.