для чего нужна вулканическая сера
Для чего нужна вулканическая сера
Чистая желтая сера
Сера — минерал из класса самородных элементов. Сера представляет собой пример хорошо выраженного энантиоморфного полиморфизма. В природе образует 2 полиморфные модификации: a-сера ромбическая и b-сера моноклинная. При атмосферном давлении и температуре 95,6°С a-сера переходит в b-серу. Сера жизненно необходима для роста растений и животных, она входит в состав живых организмов и продуктов их разложения, ее много, например, в яйцах, капусте, хрене, чесноке, горчице, луке, волосах, шерсти и т.д. Она присутствует также в углях и нефти.
СТРУКТУРА
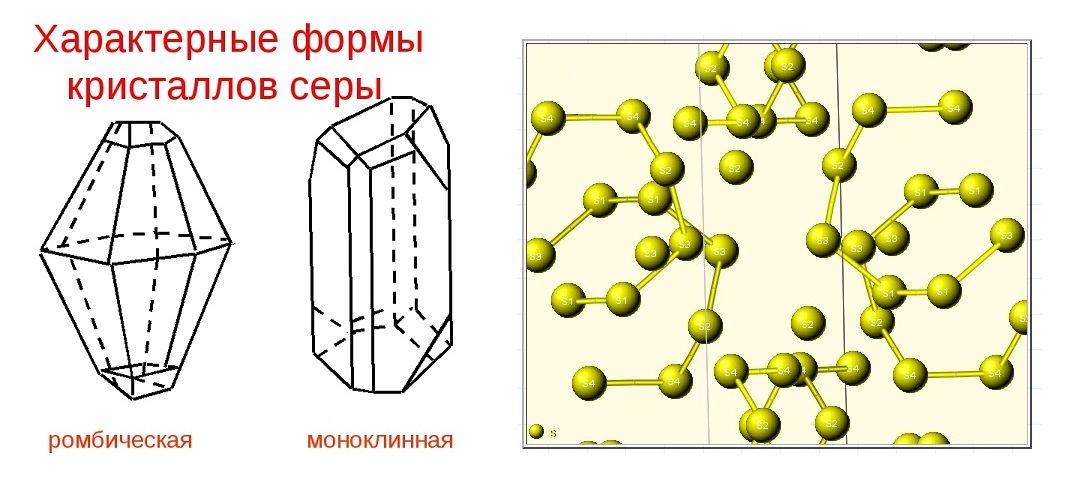
Кристаллическая структура и две сингонии серы
Самородная сера обычно представлена a-серой, которая кристаллизуется в ромбической сингонии, ромбо-дипирамидальный вид симметрии. Кристаллическая сера имеет две модификации; одну из них, ромбическую, получают из раствора серы в сероуглероде (CS2) испарением растворителя при комнатной температуре. При этом образуются ромбовидные просвечивающие кристаллы светложелтого цвета, легко растворимые в CS2. Эта модификация устойчива до 96° С, при более высокой температуре стабильна моноклинная форма. При естественном охлаждении расплавленной серы в цилиндрических тиглях вырастают крупные кристаллы ромбической модификации с искаженной формой (октаэдры, у которых частично «срезаны» углы или грани). Такой материал в промышленности называется комовая сера. Моноклинная модификация серы представляет собой длинные прозрачные темножелтые игольчатые кристаллы, также растворимые в CS2. При охлаждении моноклинной серы ниже 96° С образуется более стабильная желтая ромбическая сера.
СВОЙСТВА
МОРФОЛОГИЯ
Образует усечённо-дипирамидальные, реже дипирамидальные, пинакоидальные или толстопризматические кристаллы, а также плотные скрытокристаллические, сливные, зернистые, реже тонковолокнистые агрегаты. Главные формы на кристаллах: дипирамиды (111) и (113), призмы (011) и (101), пинакоид (001). Также сростки и друзы кристаллов, скелетные кристаллы, псевдосталактиты, порошковатые и землистые массы, налёты и примазки. Для кристаллов характерны множественные параллельные срастания.
ПРОИСХОЖДЕНИЕ
Сера образуется при вулканических извержениях, при выветривании сульфидов, при разложении гипсоносных осадочных толщ, а также в связи с деятельностью бактерий. Главные типы месторождений самородной серы — вулканогенные и экзогенные (хемогенно-осадочные). Экзогенные месторождения преобладают; они связаны с гипсо-ангидритами, которые под воздействием выделений углеводородов и сероводорода восстанавливаются и замещаются серно-кальцитовыми рудами. Такой инфильтрационно-метасоматический генезис имеют все крупнейшие месторождения. Самородная сера часто образуется (кроме крупных cкоплений) в результате окисления H2S. Геохимические процессы её образования существенно активизируются микроорганизмами (сульфатредуцирующими и тионовыми бактериями). Сопутствующие минералы — кальцит, арагонит, гипс, ангидрит, целестин, иногда битумы. Среди вулканогенных месторождений самородной серы главное значение имеют гидротермально-метасоматические (например, в Японии), образованные сероносными кварцитами и опалитами, и вулканогенно-осадочные сероносные илы кратерных озёр. Образуется также при фумарольной деятельности. Образуясь в условиях земной поверхности, самородная сера является всё же не очень устойчивой и, постепенно окисляясь, даёт начало сульфатам, гл. образом гипсу.
Используется в производстве серной кислоты (около 50% добываемого количества). В 1890 г. Герман Фраш предложил плавить серу под землёй и извлекать на поверхность через скважины, и в настоящее время месторождения серы разрабатывают главным образом путём выплавки самородной серы из пластов под землёй непосредственно в местах её залегания. Сера также в больших количествах содержится в природном газе (в виде сероводорода и сернистого ангидрида), при добыче газа она откладывается на стенках труб, выводя их из строя, поэтому её улавливают из газа как можно быстрее после добычи.
ПРИМЕНЕНИЕ
Сера входит в состав спичечной головки
Примерно половина производимой серы используется в производстве серной кислоты. Серу применяют для вулканизации каучука, как фунгицид в сельском хозяйстве и как сера коллоидная — лекарственный препарат. Также сера в составе серобитумных композиций применяется для получения сероасфальта, а в качестве заместителя портландцемента — для получения серобетона. Сера находит применение для производства пиротехнических составов, ранее использовалась в производстве пороха, применяется для производства спичек.
Самородная сера — применение, свойства, особенности
Впервые увидев изумительной красоты кристаллы ярко-жёлтого, лимонного или медового цвета, можно ошибочно принять их за янтарь. Но это не что иное, как самородная сера.
Открытие самородной серы
Сера самородная существует на Земле с момента рождения планеты. Можно сказать, что она имеет внеземное происхождение. Известно, что этот минерал присутствует в больших количествах и на других планетах. Ио — спутник Сатурна, покрытый извергающимися вулканами, похож на огромный яичный желток. Значительная часть поверхности Венеры также покрыта слоем жёлтой серы.
Люди начали использовать её ещё до нашей эры, но точная дата открытия неизвестна.
Неприятный удушающий запах, возникающий при горении, принёс этому веществу дурную славу. Чуть ли не во всех религиях мира расплавленная сера, источающая невыносимое зловоние, ассоциировалась с адской преисподней, где грешники принимали жуткие мучения.
Древние жрецы, совершая религиозные обряды, применяли горящий серный порошок для общения с подземными духами. Считалось, что сера – порождение тёмных сил из потустороннего мира.
Описание смертоносных испарений встречается у Гомера. А знаменитый самовоспламеняющийся «греческий огонь», повергавший противника в мистический ужас, также имел в своём составе серу.
Греки добывали самородную серу на Сицилии и с помощью едкого состава чернили металл, отбеливали кожу и ткани, боролись с паразитами и плесенью.
В VIII веке китайцы применяли горючие свойства самородной серы при изготовлении пороха.
Арабские алхимики называли серу «отцом всех металлов» и создали оригинальную ртутно-серную теорию. По их мнению, сера присутствует в составе любого металла.
Позже французский физик Лавуазье, после проведения серии опытов по горению серы, установил её элементарную природу.
После открытия пороха и его распространения в Европе начали добывать самородную серу и разработали метод получения вещества из пирита. Впрочем, этот способ широко использовался ещё в древней Руси.
Происхождение самородной серы
В недрах нашей планеты содержание природной серы не менее 0,5%. В самородном виде её крупные залежи встречаются редко и внешне похожи на сюрреалистический пейзаж с картин Сальвадора Дали.
В некоторых рудах присутствуют вкрапления чистой серы. Откуда и как давно они появились? До сих пор учёные не пришли к единому выводу. Существует несколько версий:
Места добычи самородной серы
На материке Евразия вся сера (самородная) находится в поверхностном слое. Крупное Водинское месторождение расположено в Самарской области. Отсюда широкая полоса серосодержащей породы тянется по левому берегу Волги до Казани. В Челябинской области добывают серу, которая образовалась после окисления пирита.
Курильские острова и Камчатка – кладовая серы, образовавшейся после извержения вулканов. За рубежом серу активно добывают в США, Италии, Испании, на Гавайских островах, Сербии. Богатые залежи самородных кристаллов находятся в Прикарпатье, Польше, Узбекистане, Туркмении.
Физические и химические свойства самородной серы
Антуан Лавуазье был первым естествоиспытателем, детально изучившим свойства самородной серы. Оказалось, что сера хорошо кристаллизуется. После расплавления образуются игольчатые кристаллики. Охлаждаясь, они изменяют форму и объём, превращаясь в полупрозрачные агрегаты лимонного или янтарного цвета.
«Самородная» необычно ведёт себя при нагревании. Расплавленная до 119°С, а затем вылитая в холодную воду, она принимает вид пластичной массы, похожей на резину. Кристаллизация серы начнётся только через несколько суток.
При нагревании до высоких температур вязкость серной массы увеличивается. После 155°С происходит уплотнение, а при 187°С природная сера становится твёрдой. При дальнейшем нагреве до 300°С к сере возвращается текучесть, а достигнув 445°С, она вскипает, а затем переходит в газообразное состояние.
Обычно формулу серы записывают как «S». В зависимости от строения молекул это может быть «S8», кристаллические жёлтые агрегаты, или «S4» и «S6», коричневая пластическая масса.
Свойства кристалла самородной серы:
Цвет серного порошка обычно очень светлый, почти белый или соломенного оттенка. Примесь селена придаёт самородному минералу тёмно-коричневый окрас, мышьяк делает его ярко-красным.
Область применения самородной серы
Более 50% добываемой самородной серы расходуется на производство серной кислоты.
Помимо химической промышленности сера находит применение:
Самородная сера имеет низкую электропроводность, может входить в состав материала при производстве электрических изоляторов. Известно применение минерала в качестве теплоизолятора при строительстве сооружений.
Лечение самородной серой
В тканях человеческого тела присутствует до 0,25% серы от общей массы. Особенно велико её содержание в костно-мышечной системе, нервной ткани, желчи, коже, волосах.
Поэтому применение препаратов на основе соединений серы показано при таких заболеваниях, как:
Кроме этого сера улучшает выработку желчи, стимулирует мозговую активность, снимает воспаление, оказывает противоглистное действие.
Недостаток серы в организме можно восполнить с помощью коррекции питания. Больше всего содержание серы в пище животного происхождения: говядина, все молочные продукты, перепелиные и куриные яйца. Полезно включить в свой рацион морепродукты, гречневую и овсяную кашу. Среди овощей и фруктов стоит обратить внимание на богатые серой чеснок, репчатый лук, бобовые культуры, капусту, крыжовник.
» alt=»»>
Видео на тему:Сера самородная
Магические свойства самородной серы
С древних времён самородная сера ассоциировалась с колдовством и магией. Резкий неприятный запах, возникавший при горении, применяли для отпугивания тёмных сил.
Сера обладает способностью впитывать отрицательную энергию и поглощать негативные эмоции. Небольшой кусочек самородной серы стоит держать на рабочем месте и в своей квартире. Она поможет избежать конфликтов с коллегами и ссор в семье.
Минерал окажет благотворное влияние на раздражительных людей, склонных к агрессии, разрешит давние споры и поможет найти компромиссное решение.
У астрологов самородный минирал считается одним из трёх первичных веществ и символизирует вездесущий дух жизни. Являясь «отцом всех металлов», серный самородок связан одновременно со всеми знаками зодиака.
Для любителей минералогии кристалл самородной серы станет достойным украшением коллекции.
Популярная библиотека химических элементов
Сера – одно из немногих веществ, которыми уже несколько тысяч лет назад оперировали первые «химики». Она стала служить человечеству задолго до того, как заняла в таблице Менделеева клетку под №16.
Об одном из самых древних (хотя и гипотетических!) применений серы рассказывают многие старинные книги. Как источник тепла при термообработке грешников серу живописуют и Новый и Ветхий заветы. И если книги такого рода не дают достаточных оснований для археологических раскопок в поисках остатков райских кущ или геенны огненной, то их свидетельство о том, что древние были знакомы с серой и некоторыми ее свойствами, можно принять на веру.
Одна из причин этой известности – распространенность самородной серы в странах древнейших цивилизаций. Месторождения этого желтого горючего вещества разрабатывались греками и римлянами, особенно в Сицилии, которая вплоть до конца прошлого века славилась в основном серой.
И сейчас пороховое производство потребляет часть добываемой серы, правда весьма незначительную. В наше время сера – один из важнейших видов сырья для многих химических производств. И в этом причина непрерывного роста мирового производства серы.
Происхождение серы
Большие скопления самородной серы встречаются не так уж часто. Чаще она присутствует в некоторых рудах. Руда самородной серы – это порода с вкраплениями серы.
Когда образовались эти вкрапления – одновременно с сопутствующими породами или позже? От ответа на этот вопрос зависит направление поисковых и разведочных работ. Но, несмотря на тысячелетия общения с серой, человечество до сих пор не имеет однозначного ответа. Существует несколько теорий, авторы которых придерживаются противоположных взглядов.
Теория сингенеза (т.е. одновременного образования серы и вмещающих пород) предполагает, что образование самородной серы происходило в мелководных бассейнах. Особые бактерии восстанавливали сульфаты, растворенные в воде, до сероводорода, который поднимался вверх, попадал в окислительную зону и здесь химическим путем или при участии других бактерий окислялся до элементарной серы. Сера осаждалась на дно, и впоследствии содержащий серу ид образовал руду.
Теория эпигенеза (вкрапления серы образовались позднее, чем основные породы) имеет несколько вариантов. Самый распространенный из них предполагает, что подземные воды, проникая сквозь толщи пород, обогащаются сульфатами. Если такие воды соприкасаются с месторождениями нефти или природного газа, то ионы сульфатов восстанавливаются углеводородами до сероводорода. Сероводород поднимается к поверхности и, окисляясь, выделяет чистую серу в пустотах и трещинах пород.
В последние десятилетия находит все новые подтверждения одна из разновидностей теории эпигенеза – теория метасоматоза (в переводе с греческого «метасоматоз» означает «замещение». Согласно ей в недрах постоянно происходит превращение гипса CaSO4 · 2H2O и ангидрита CaSO4 в серу и кальцит СаCO3. Эта теория создана в 1935 г. советскими учеными Л.М. Миропольским и Б.П. Кротовым. В ее пользу говорит, в частности, такой факт.
В 1961 г. в Ираке было открыто месторождение Мишрак. Сера здесь заключена в карбонатных породах, которые образуют свод, поддерживаемый уходящими вглубь опорами (в геологии их называют крыльями). Крылья эти состоят в основном из ангидрита и гипса. Такая же картина наблюдалась на отечественном месторождении Шор-Су.
Геологическое своеобразие этих месторождений можно объяснить только с позиций теории метасоматоза: первичные гипсы и ангидриты превратились во вторичные карбонатные руды с вкраплениями самородной серы. Важно не только соседство минералов – среднее содержание серы в руде этих месторождений равно содержанию химически связанной серы в ангидрите. А исследования изотопного состава серы и углерода в руде этих месторождений дали сторонникам теории метасоматоза дополнительные аргументы.
Но есть одно «но»: химизм процесса превращения гипса в серу и кальцит пока не ясен, и потому нет оснований считать теорию метасоматоза единственно правильной. На Земле и сейчас существуют озера (в частности, Серное озеро близ Серноводска), где происходит сингенетическое отложение серы и сероносный ил не содержит ни гипса, ни ангидрита.
Все это означает, что разнообразие теорий и гипотез о происхождении самородной серы – результат не только и не столько неполноты наших знаний, сколько сложности явлений, происходящих в недрах. Еще из элементарной школьной математики все мы знаем, что к одному результату могут привести разные пути. Этот закон распространяется и на геохимию.
Добыча серы
Серные руды добывают разными способами – в зависимости от условий залегания. Но в любом случае приходится уделять много внимания технике безопасности. Залежам серы почти всегда сопутствуют скопления ядовитых газов – соединений серы. К тому же нельзя забывать о возможности ее самовозгорания.
Добыча руды открытым способом происходит так. Шагающие экскаваторы снимают пласты пород, под которыми залегает руда. Взрывами рудный пласт дробят, после чего глыбы руды отправляют на обогатительную фабрику, а оттуда – на сероплавильный завод, где из концентрата извлекают серу. Методы извлечения различны. О некоторых из них будет рассказано ниже. А здесь уместно кратко описать скважинный метод добычи серы из-под земли, позволивший Соединенным Штатам Америки и Мексике стать крупнейшими поставщиками серы.
В конце прошлого века на юге Соединенных Штатов были открыты богатейшие месторождения серной руды. Но подступиться к пластам было непросто: в шахты (а именно шахтным способом предполагалось разрабатывать месторождение) просачивался сероводород и преграждал доступ к сере. Кроме того, пробиться к сероносным пластам мешали песчаные плавуны. Выход нашел химик Герман Фраш, предложивший плавить серу под землей и через скважины, подобные нефтяным, выкачивать ее на поверхность. Сравнительно невысокая (меньше 120°C) температура плавления серы подтверждала реальность идеи Фраша. В 1890 г. начались испытания, приведшие к успеху.
В принципе установка Фраша очень несложна: труба в трубе. В пространство между трубами подается перегретая вода и по нему идет в пласт. А по внутренней, обогреваемой со всех сторон, трубе поднимается расплавленная сера. Современный вариант установки Фраша дополнен третьей – самой узкой трубой. Через нее в скважину подается сжатый воздух, который помогает поднять расплавленную Серу на поверхность. Одно из основных достоинств метода Фраша – в том, что он позволяет уже на первой стадии добычи получить сравнительно чистую серу. При разработке богатых руд этот метод весьма эффективен.
Раньше считалось, что метод подземной выплавки серы применим только в специфических условиях «соляных куполов» тихоокеанского побережья США и Мексики. Однако опыты, проведенные в Польше и СССР, опровергли это мнение. В Польше этим методом уже добывают большое количество серы: в 1968 г. пущены первые серные скважины и в СССР.
А руду, полученную в карьерах и шахтах, приходится перерабатывать (часто с предварительным обогащением), используя для этого различные технологические приемы.
Известно несколько методов получения серы из серных руд: пароводяные, фильтрационные, термические, центрифугальные и экстракционные.
Термические методы извлечения серы – самые старые. Еще в XVIII в. в Неаполитанском королевстве выплавляли серу в кучах – «сольфатарах». До сих пор в Италии выплавляют серу в примитивных печах – «калькаронах». Тепло, необходимое для выплавления серы из руды, получают, сжигая часть добытой серы. Процесс этот малоэффективен, потери достигают 45%.
Италия стала родиной и пароводяных методов извлечения серы из руд. В 1859 г. Джузеппе Джилль получил патент на свой аппарат – предшественник нынешних автоклавов. Автоклавный метод (значительно усовершенствованный, конечно) используется и сейчас во многих странах.
В автоклавном процессе обогащенный концентрат серной руды, содержащий до 80% серы, в виде жидкой пульпы с реагентами подается насосами в автоклав. Туда же под давлением подается водяной пар. Пульпа нагревается до 130°C. Сера, содержащаяся в концентрате, плавится и отделяется от породы. После недолгого отстоя выплавленная сера сливается. Затем из автоклава выпускаются «хвосты» – взвесь пустой породы в воде. Хвосты содержат довольно много серы и вновь поступают на обогатительную фабрику.
В России автоклавный способ был впервые применен инженером К.Г. Паткановым в 1896 г.
Современные автоклавы – это огромные аппараты высотой с четырехэтажный дом. Такие автоклавы установлены, в частности, на сероплавильном заводе Роздольского горно-химического комбината в Прикарпатье.
На некоторых производствах, например на крупном серном комбинате в Тарнобжеге (Польша), пустую породу отделяют от расплавленной серы на специальных фильтрах. Метод разделения серы и пустой породы на центрифугах разработан в нашей стране. Словом, «руду золотую (точнее – золотистую) отделять от породы пустой» можно по-разному.
В последнее время все большее внимание уделяется скважинным геотехнологическим способам добычи серы. На Язовском месторождении в Прикарпатье серу – классический диэлектрик плавят под землей токами высокой частоты и выкачивают на поверхность через скважины, как в методе Фраша. Ученые Института горно-химического сырья предложили способ подземной газификации серы. По этому способу серу поджигают в пласте, а на поверхность выкачивают сернистый газ, который идет на производство серной кислоты и других полезных продуктов.
По-разному и удовлетворяют свои потребности в сере разные страны. Мексика и США используют в основном метод Фраша. Италия, занимающая по добыче серы третье место среди капиталистических государств, продолжает добывать и перерабатывать (разными методами) серные руды сицилийских месторождений и провинции Марке. У Японии есть значительные запасы серы вулканического происхождения. Франция и Канада, не имеющие самородной серы, развили крупное производство ее из газов. Нет собственных серных месторождений и в Англии и ФРГ. Свои потребности в серной кислоте они покрывают за счет переработки серусодержащего сырья (преимущественно пирита), а элементарную серу импортируют из других стран.
Советский Союз и социалистические страны полностью удовлетворяют свои потребности благодаря собственным источникам сырья. После открытия и освоения богатых Прикарпатских месторождений СССР и Польша значительно увеличили производство серы. Эта отрасль промышленности продолжает развиваться. В последние годы построены новые крупные предприятия на Украине, реконструированы старые комбинаты на Волге и в Туркмении, расширено производство серы из природного газа и отходящих газов.
Кристаллы и макромолекулы
В том, что сера – самостоятельный химический элемент, а не соединение, первым убедился великий французский химик Антуан Лоран Лавуазье в XVIII в.
С тех пор представления о сере как элементе изменились не очень сильно, но значительно углубились и дополнились.
Сейчас известно, что элемент №16 состоит из смеси четырех устойчивых изотопов с массовыми числами 32, 33, 34 и 36. Это типичный неметалл.
Лимонно-желтые кристаллы чистой серы полупрозрачны. Форма кристаллов не всегда одинакова. Чаще всего встречается ромбическая сера (наиболее устойчивая модификация) – кристаллы имеют вид октаэдров со срезанными углами. В эту модификацию при комнатной (или близкой к комнатной) температуре превращаются все прочие модификации. Известно, например, что при кристаллизации из расплава (температура плавления серы 119,5°C) сначала получаются игольчатые кристаллы (моноклинная форма). Но эта модификация неустойчива, и при температуре 95,6°C она переходит в ромбическую. Подобный процесс происходит и с другими модификациями серы.
Напомним известный опыт – получение пластической серы.
Если расплавленную серу вылить в холодную воду, образуется эластичная, во многом похожая на резину масса. Ее можно получить и в виде нитей. Но проходит несколько дней, и масса перекристаллизуется, становится жесткой и ломкой.
Молекулы кристаллов серы всегда состоят из восьми атомов (S8), а различие в свойствах модификаций серы объясняется полиморфизмом – неодинаковым строением кристаллов. Атомы в молекуле серы построены в замкнутый цикл, образующий своеобразный венец. При плавлении связи в цикле рвутся, и циклические молекулы превращаются в линейные.
Необычному поведению серы при плавлении даются различные толкования. Одно из них – такое. При температуре от 155 до 187°, по-видимому, происходит значительный рост молекулярного веса, это подтверждается многократным увеличением вязкости. При 187°C вязкость расплава достигает чуть ли не тысячи пуаз, получается почти твердое вещество. Дальнейший рост температуры приводит к уменьшению вязкости (молекулярный вес падает).
При 300°C сера вновь переходит в текучее состояние, а при 444,6°C закипает.
У паров серы с повышением температуры число атомов в молекуле постепенно уменьшается: S8 → S6 → S4 → (800°C) S2. При 1700°C пары серы одноатомны.
Коротко о соединениях серы
По распространенности элемент №16 занимает 15-е место. Содержание серы в земной коре составляет 0,05% по весу. Это немало.
К тому же сера химически активна и вступает в реакции с большинством элементов. Поэтому в природе сера встречается не только в свободном состоянии, но и в виде разнообразных неорганических соединений. Особенно распространены сульфаты (главным образом щелочных и щелочноземельных металлов) и сульфиды (железа, меди, цинка, свинца). Сера есть и в углях, сланцах, нефти, природных газах, в организмах животных и растений.
При взаимодействии серы с металлами, как правило, выделяется довольно много тепла. В реакциях с кислородом сера дает несколько окислов, из них самые важные SO2 и SO3 – ангидриды сернистой H2SO3 и серной Н2SO4 кислот. Соединение серы с водородом – сероводород H2S – очень ядовитый зловонный газ, всегда присутствующий в местах гниения органических остатков. Земная кора в местах, расположенных близ месторождений серы, часто содержит довольно значительные количества сероводорода. В водном растворе этот газ обладает кислотными свойствами. Хранить его растворы на воздухе нельзя, он окисляется с выделением серы:
Сероводород – сильный восстановитель. Этим его свойством пользуются во многих химических производствах.
Для чего нужна сера
Значительную часть мировой добычи серы поглощает бумажная промышленность (соединения серы помогают выделить целлюлозу). Для того чтобы произвести 1 т целлюлозы, нужно затратить более 100 кг серы. Много элементарной серы потребляет и резиновая промышленность – для вулканизации каучуков.
В сельском хозяйстве сера применяется как в элементарном виде, так и в различных соединениях. Она входит в состав минеральных удобрений и препаратов для борьбы с вредителями. Наряду с фосфором, калием и другими элементами сера необходима растениям. Впрочем, большая часть вносимой в почву серы не усваивается ими, но помогает усваивать фосфор. Серу вводят в почву вместе с фосфоритной мукой. Имеющиеся в почве бактерии окисляют ее, образующиеся серная и сернистая кислоты реагируют с фосфоритами, и в результате получаются фосфорные соединения, хорошо усваиваемые растениями.
Однако основной потребитель серы – химическая промышленность. Примерно половина добываемой в мире серы идет на производство серной кислоты. Чтобы получить 1 т H2SО4, нужно сжечь около 300 кг серы. А роль серной кислоты в химической промышленности сравнима с ролью хлеба в нашем питании.
Значительное количество серы (и серной кислоты) расходуется при производстве взрывчатых веществ и спичек. Чистая, освобожденная от примесей сера нужна для производства красителей и светящихся составов.
Соединения серы находят применение в нефтехимической промышленности. В частности, они необходимы при производстве антидетонаторов, смазочных веществ для аппаратуры сверхвысоких давлений; в охлаждающих маслах, ускоряющих обработку металла, содержится иногда до 18% серы.
Перечисление примеров, подтверждающих первостепенную важность элемента №16, можно было бы продолжить, но «нельзя объять необъятное». Поэтому вскользь упомянем, что сера необходима и таким отраслям промышленности, как горнодобывающая, пищевая, текстильная, и – поставим точку.
Наш век считается веком «экзотических» материалов – трансурановых элементов, титана, полупроводников и так далее. Но внешне непритязательный, давно известный элемент №16 продолжает оставаться абсолютно необходимым. Подсчитано, что в производстве 88 из 150 важнейших химических продуктов используют либо саму серу, либо ее соединения.
Из древних и средневековых книг
«Сера применяется для очищения жилищ, так как многие держатся мнения, что запах и горение серы могут предохранить от всяких чародейств и прогнать всякую нечистую силу».
Плиний Старший, «Естественная история» I в. н.э.
«Если травы чахлы, бедны соками, а ветви и листва деревьев имеют окраску тусклую, грязную, темноватую вместо блестящего зеленого цвета, это признак, что подпочва изобилует минералами, в которых господствует сера».
«Если руда очень богата серой, ее зажигают на широком железном листе с множеством отверстий, через которые сера вытекает в горшки, наполненные доверху водой».
«Сера входит также в состав ужасного изобретения – порошка, который может метать далеко вперед куски железа, бронзы или камня – орудие войны нового тина».
Агрикола, «О царстве минералов», XVI в.
Как испытывали серу в XIV веке
«Если ты хочешь испытать серу, хороша она или нет, то возьми кусок серы в руку и поднеси к уху. Если сера трещит так, что ты слышишь ее треск, значит она хороша; если же сера молчит и не трещит, то она нехороша. »
Этот своеобразный метод определения качества материала на слух (применительно к сере) может быть использован и сейчас. Экспериментально подтвердилось, что «трещит» только сера, содержащая не больше одного процента примесей. Иногда дело не ограничивается только треском – кусок серы раскалывается на части.
Удушающий серный газ
Как известно, выдающийся естествоиспытатель древности Плиний Старший погиб в 79 г. н.э. при извержении вулкана. Его племянник в письме историку Тациту писал: «. Вдруг раздались раскаты грома, и от горного пламени покатились вниз черные серные пары. Все разбежались. Плиний поднялся и, опираясь на двух рабов, думал тоже уйти; но смертоносный пар окружил его со всех сторон, его колени подогнулись, он снова упал и задохся».
«Черные серные пары», погубившие Плиния, состояли, конечно, не только из парообразной серы. В состав вулканических газов входят и сероводород, и двуокись серы. Эти газы обладают не только резким запахом, но и большой токсичностью. Особенно опасен сероводород. В чистом виде он убивает человека почти мгновенно. Опасность велика даже при незначительном (порядка 0,01%) содержании сероводорода в воздухе. Сероводород тем более опасен, что он может накапливаться в организме. Он соединяется с железом, входящим в состав гемоглобина, что может привести к тяжелейшему кислородному голоданию и смерти. Сернистый газ (двуокись серы) менее токсичен, однако выпуск его в атмосферу приводил к тому, что вокруг металлургических заводов гибла вся растительность. Поэтому на всех предприятиях, производящих или использующих эти газы; вопросам техники безопасности уделяется особое внимание.
Сернистый газ и соломенная шляпка
Соединяясь с водой, сернистый газ образует слабую сернистую кислоту Н2SO3, существующую только в растворах. В присутствии влаги сернистый газ обесцвечивает многие красители. Это свойство используется для отбелки шерсти, шелка, соломы. Но такие соединения, как правило, не обладают большой стойкостью, и белые соломенные шляпки со временем приобретают первоначальную грязно-желтую окраску.
Не асбест, хотя и похож
Сернистый ангидрид SO3 в обычных условиях представляет собой бесцветную очень летучую жидкость, кипящую при 44,8°C. Твердеет он при –16,8°C и становится очень похожим на обыкновенный лед. Но есть и другая – полимерная модификация твердого серного ангидрида (формулу его в этом случае следовало бы писать (SO3)n). Внешне она очень похожа на асбест, ее волокнистую структуру подтверждают рентгенограммы. Строго определенной точки плавления эта модификация не имеет, что свидетельствует о ее неоднородности.
Гипс и алебастр
Гипс CaSO4 · 2Н2O – один из самых распространенных минералов. Но распространенные в медицинской практике «гипсовые шины» делаются не из природного гипса, а из алебастра. Алебастр отличается от гипса только количеством кристаллизационной воды в молекуле, его формула 2CaSO4 · Н2O. При «варке» алебастра (процесс идет при 160. 170°C в течение 1,5. 2 часов) гипс теряет три четверти кристаллизационной воды, и материал приобретает вяжущие свойства. Алебастр жадно захватывает воду, при этом происходит быстрая беспорядочная кристаллизация. Разрастись кристаллики не успевают, но сплетаются друг с другом; масса, образованная ими, в мельчайших подробностях воспроизводит форму, в которой происходит твердение. Химизм происходящего в это время процесса обратен происходящему при варке: алебастр превращается в гипс. Поэтому отливка – гипсовая, маска – гипсовая, повязка – тоже гипсовая, а делаются они из алебастра.
Глауберова соль
Минерал глауберовой соли называется мирабилитом (от латинского «mirabilis» – удивительный). Название происходит от имени, которое дал Глаубер открытой им соли; он назвал ее чудесной. Крупнейшие в мире разработки этого вещества находятся в нашей стране, чрезвычайно богата глауберовой солью вода знаменитого залива Кара-Богаз-Гол. Дно залива буквально устлано ею.
Сульфиты, сульфаты, тиосульфаты.
Если вы фотолюбитель, вам необходим фиксаж, т.е. натриевая соль серноватистой (тиосерной) кислоты Н2S2O3. Тиосульфат натрия Na2S2O3 (он же гипосульфит) служил поглотителем хлора в первых противогазах.
Если вы порезались во время бритья, кровь можно остановить кристаллом алюмокалиевых квасцов KAl(SO4)2 · 12H2O.
Если вы хотите побелить потолки, покрыть медью какой-либо предмет или уничтожить вредителей в саду – вам не обойтись без темно-синих кристаллов медного купороса CuSO4 · 5Н2О.
Если врачи порекомендовали вам очистить желудок, воспользуйтесь горькой солью MgSО4. (Она же придает горький вкус морской воде.)
Бумага, на которой напечатана эта книга, сделана с помощью гидросульфита кальция Са(НSO3)2.
Широко используются также железный купорос FeSO4 · 7H2O, хромовые квасцы K2SO4 · Cr2(SO4)3 · 2Н2O и многие другие соли серной, сернистой и тиосерной кислот.
Киноварь
Если в лаборатории разлили ртуть (возникла опасность отравления ртутными парами!), ее первым делом собирают, а те места, из которых серебристые капли не извлекаются, засыпают порошкообразной серой. Ртуть и сера вступают в реакцию даже в твердом состоянии – при простом соприкосновении. Образуется кирпично-красная киноварь – сульфид ртути – химически крайне инертное и безвредное вещество.
Выделить ртуть из киновари несложно. Многие другие металлы, в частности железо, вытесняют ртуть из киновари.
Серобактерии
В природе постепенно происходит круговорот серы, подобный круговороту азота или углерода. Растения потребляют серу – ведь ее атомы входят в состав белка. Растения берут серу из растворимых сульфатов, а гнилостные бактерии превращают серу белков в сероводород (отсюда – отвратительный запах гниения).
Но есть так называемые серобактерии, которым вообще не нужна органическая пища. Они питаются сероводородом, и в их организмах в результате реакции между H2S, CO2 и О2 образуются углеводы и элементарная сера. Серобактерии нередко оказываются переполнены крупинками серы – почти всю их массу составляет сера с очень небольшой «добавкой» органических веществ.
Сера – фармацевтам
Все сульфамидные препараты – сульфидин, сульфазол, норсульфазол, сульгин, сульфодимезин, стрептоцид и другие подавляют активность многочисленных микробов. И все эти лекарства – органические соединения серы. Вот структурные формулы некоторых из них:
После появления антибиотиков роль сульфамидных препаратов несколько уменьшилась. Впрочем, и многие антибиотики можно рассматривать как органические производные серы. В частности, она обязательно входит в состав пенициллина.
Мелкодисперсная элементарная сера – основа мазей, применяемых при лечении грибковых заболеваний кожи.
Нитрид серы проводит ток
В 1975 г. журнал «Кэмикл энд инжениринг ньюс» сообщил о получении нового неорганического полимера, у которого многие свойства – как у металла. Полимерный нитрид серы – политиазил (SN)n легко прессуется и куется, его электропроводность близка к электропроводности ртути. При этом пленки из политиазила не одинаково проводят ток в продольном и поперечном направлении. Это объясняется тем, что пленка построена из упорядоченных, расположенных параллельно друг другу полимерных волокон.
Что можно построить из серы
В 70-х годах в некоторых странах мира производство серы превысило потребности в ней. Поэтому сере стали искать новые применения, прежде всего в таких материалоемких областях, как строительство. В результате этих поисков появились серный пенопласт – как теплоизоляционный материал, бетонные смеси, в которых серой частично или полностью заменен портландцемент, покрытия для автострад, содержащие элементарную серу.