для чего определяют плотность газа
Плотность газа
Плотность газа и другие его физические свойства
Одной из важнейших физических свойств газообразных веществ является значение их плотности.
Зачастую, применительно к газам используют понятие «относительная плотность». Данная величина представляет собой отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму.
Например, при нормальных условиях масса диокисда углерода в объеме 1 л равна 1,98 г, а масса водорода в том же объеме и при тех же условиях – 0,09 г, откуда плотность диоксида углерода по водороду составит: 1,98 / 0,09 = 22.
Относительная плотность газа
Обозначим относительную плотность газа m1 / m2 буквой D. Тогда
Следовательно, молярная масса газа равна его плотности по отношению у другому газа, умноженной на молярную массу второго газа.
Часто плотности различных газов определяют по отношению к водороду, как самому легкому из всех газов. Поскольку молярная масса водорода равна 2,0158 г/моль, то в этом случае уравнение для расчета молярных масс принимает вид:
или, если округлить молярную массу водорода до 2:
Вычисляя, например, по этому уравнению молярную массу диоксида углерода, плотность которого по водороду, как указано выше равна 22, находим:
M(CO2) = 2 × 22 = 44 г/моль.
Плотность газа в лабораторных условиях самостоятельно можно определить следующим образом: необходимо взять стеклянную колбу с краном и взвесить её на аналитических весах. Первоначальный вес – вес колбы, из которой откачали весь воздух, конечный – вес колбы, наполненной до конкретного давления исследуемым газом. Разность полученных масс следует разделить на объем колбы. Вычисленное значение и есть плотность газа в данных условиях.
Чтобы рассчитать плотность газа при н.у. нужно воспользоваться уравнением состояния идеального газа:
В таблице ниже приведены значения плотностей некоторых газов.
Таблица 1. Плотность газов при нормальных условиях.
Химия. 10 класс
*§ 8-1. Закон Авогадро. Относительная плотность газов. Объёмная доля газа в смеси
Закон Авогадро. Относительная плотность газов. Объёмная доля газа в смеси
Как вам известно, вещества могут находиться в твёрдом, жидком и газообразном состоянии. Молекулы жидкости и твёрдого вещества располагаются близко друг к другу. Это возможно благодаря тому, что молекулы притягиваются друг к другу. То есть существуют силы, которые удерживают молекулы жидкости или твёрдого вещества вместе. Из курса химии 8-го класса вы знаете, что эти силы называются силами межмолекулярного взаимодействия. Молекулы газов находятся на значительно большем расстоянии друг от друга, чем в случае жидкостей и твёрдых веществ. На таком расстоянии молекулы практически не взаимодействуют друг с другом. Поэтому, чтобы превратить жидкость или твёрдое вещество в газ, необходимо преодолеть силы межмолекулярного взаимодействия, отдалив молекулы друг от друга.
Переход в газообразное состояние осуществляется в результате нагревания веществ, находящихся в твёрдом или жидком состоянии (кипение жидкостей, возгонка твёрдых веществ).
Так как расстояние между молекулами газов значительно больше размеров самих молекул, то объём, который занимает газ, — это, по существу, объём свободного пространства между хаотически движущимися молекулами газа. Величина этого пространства определяется условиями, при которых находится газ, т. е. температурой и давлением. Эта величина примерно одинакова для всех газов. При этом объёмом, занимаемым самими молекулами, можно пренебречь. Отсюда следует закон Авогадро — в равных объёмах различных газов при одинаковых условиях содержится одинаковое число молекул.
Интересно знать
Из закона Авогадро вытекают два основных следствия.
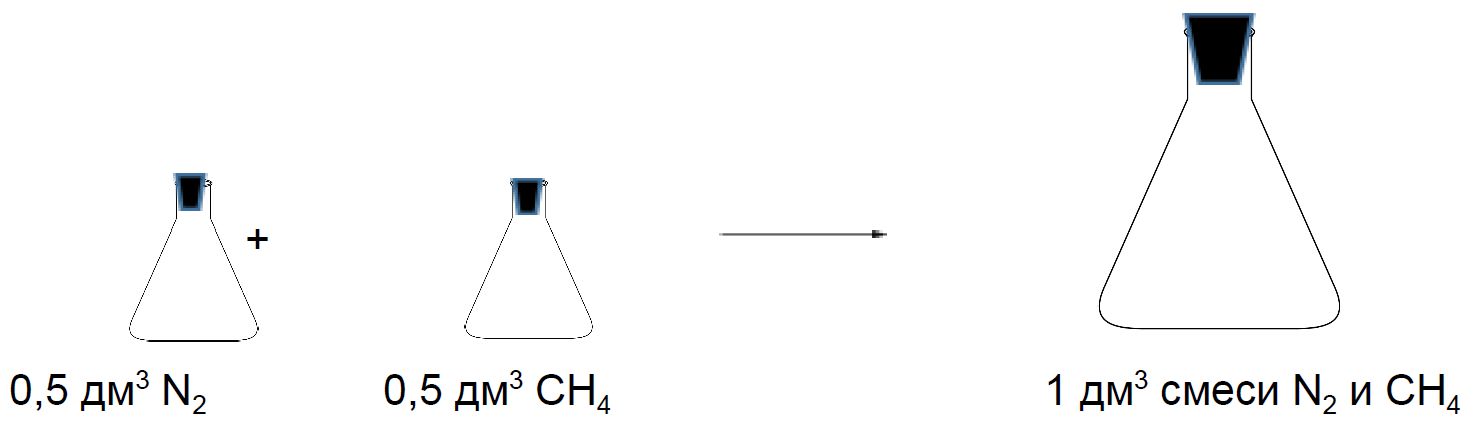
Таким образом, из закона Авогадро следует, что 22,4 дм 3 любого газа при нормальных условиях содержат 6,02 ∙ 10 23 молекул.
Второе следствие. Плотности газов относятся между собой как молярные массы газов.
Это видно из следующих соображений. Пусть имеется две порции различных газов. Рассчитаем их плотности:
газ 1: 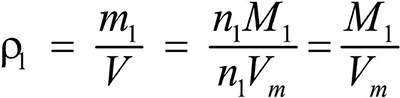
газ 2: 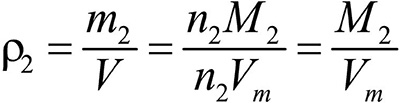
Разделив плотность первого газа на плотность второго, получим: 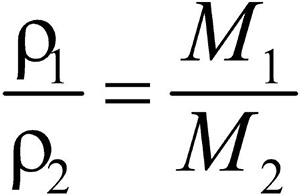
Зная D и молярную массу одного газа, легко найти молярную массу другого газа:
Пример 1. Относительная плотность газа по водороду равна 8. Определите молярную массу газа.
Пример 2. Относительная плотность некоторого газообразного углеводорода по воздуху равна 2. Определите молярную массу углеводорода.
Средняя молярная масса воздуха равна 29 г/моль ;
Следует отметить, что газы с молярной массой меньше 29 легче воздуха, больше 29 — тяжелее.
В расчётных задачах могут быть даны относительные плотности неизвестного газа по азоту, кислороду и другим газам. В этом случае для нахождения молярной массы неизвестного газа необходимо умножить относительную плотность на молярную массу соответственно азота (28 г/моль ), кислорода (32 г/моль ) и т. д.
Закон Авогадро широко применяется в химических расчётах. Поскольку для газов объёмы пропорциональны количествам (моль) веществ, то коэффициенты в уравнении реакции между газообразными веществами, отражающие количественное соотношение реагирующих веществ, пропорциональны объёмам взаимодействующих газов. Очевидно, что объёмы должны быть измерены при одинаковых условиях.
Пример 3. Какой объём кислорода потребуется для сжигания 2 дм 3 пропана? Объёмы измерены при н. у.
Уравнение реакции горения пропана:
С3Н8 + 5О2 
2 дм 3 С3Н8 — 10 дм 3 О2
Смеси газов
Состав смеси газов часто выражают в объёмных долях. Объёмная доля газа обозначается греческой буквой φ (фи) и равна отношению объёма данного газа к объёму смеси. Рассчитаем объёмную долю азота в полученной выше смеси газов:
φ = 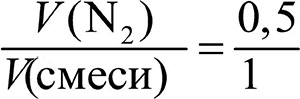
Пример 4. В результате пропускания 150 дм 3 (н. у.) воздуха через избыток известковой воды выпало 0,201 г осадка. Найдите объёмную долю (%) углекислого газа в данном образце воздуха.
Уравнение реакции взаимодействия углекислого газа с известковой водой:
СО2 + Са(ОН)2 = СаСО3 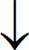
Найдём количество (моль) карбоната кальция, выпавшего в осадок (M(CaCO3) = 100 г/моль ):
По уравнению реакции:
Рассчитаем объёмную долю углекислого газа в воздухе:
V(CO2) = 0,00201 ∙ 22,4 = 0,045 дм 3 ;
φ(СО2) = 0,045/150 = 0,0003, или 0,03 %.
Уравнение реакции взаимодействия водорода с хлором:
H2 + Cl2 
Поскольку после взаимодействия осталось 10 см 3 хлора, то 40 см 3 исходной смеси прореагировало. Хлор и водород реагируют между собой в равных объёмных отношениях. Исходя из этих соображений, в реакцию вступили по 20 см 3 хлора и водорода. Поскольку осталось 10 см 3 хлора, то в первоначальной смеси было 20 см 3 водорода и 30 см 3 хлора.
Рассчитаем объёмные доли газов в исходной смеси:
φ(Cl2) = 30/50 = 0,6, или 60 %.
Согласно закону Авогадро, в равных объёмах различных газов при одинаковых условиях содержится одинаковое количество молекул.
Один моль любого газа при нормальных условиях (температура таяния льда, атмосферное давление) занимает объём
Плотности газов, измеренные при одинаковых условиях, относятся между собой как их молярные массы. Это отношение называется относительной плотностью одного газа по другому газу.
Объёмная доля газа в смеси равна отношению объёма данного газа к общему объёму смеси.
Для чего определяют плотность газа
ГАЗ ПРИРОДНЫЙ. МЕТОДЫ РАСЧЕТА ФИЗИЧЕСКИХ СВОЙСТВ
Определение физических свойств природного газа,
его компонентов и продуктов его переработки
Natural gas. Methods of calculation of physical properties.
Definition of physical properties of natural gas,
its components and processing products
Дата введения 1997-07-01
1 РАЗРАБОТАН Всероссийским научно-исследовательским центром стандартизации, информации и сертификации сырья, материалов и веществ (ВНИЦ СМВ) Госстандарта России; фирмой “Газприборавтоматика” акционерного общества “Газавтоматика” РАО “Газпром”
ВНЕСЕН Госстандартом Российской Федерации
2 ПРИНЯТ Межгосударственным Советом по стандартизации, метрологии и сертификации (протокол № 9-96 от 12 апреля 1996 г.)
За принятие проголосовали:
Наименование национального органа по стандартизации
Госстандарт Республики Казахстан
Таджикский государственный центр по стандартизации, метрологии и сертификации
3 Постановлением Государственного комитета Российской Федерации по стандартизации, метрологии и сертификации от 30 декабря 1996 г. N 723 межгосударственный стандарт ГОСТ 30319.1-96 введен в действие непосредственно в качестве государственного стандарта Российской Федерации с 1 июля 1997 г.
ВНЕСЕНО Изменение N 1, принятое Межгосударственным Советом по стандартизации, метрологии и сертификации (протокол N 22 от 06.11.2002). Государство-разработчик Россия. Постановлением Госстандарта России от 10.03.2004 N 167-ст введено в действие на территории РФ с 01.06.2004 и опубликовано в ИУС N 8, 2004 год
Изменение N 1 внесено изготовителем базы данных по тексту ИУС N 8, 2004 год
1 НАЗНАЧЕНИЕ И ОБЛАСТЬ ПРИМЕНЕНИЯ
Настоящий стандарт предназначен для практического применения при косвенном определении коэффициента сжимаемости, плотности, показателя адиабаты, скорости звука, динамической вязкости и объемной удельной теплоты сгорания природного газа, его компонентов и продуктов его переработки по измеренным значениям давления, температуры, компонентного состава и плотности при стандартных условиях.
Используемые в настоящем стандарте определения и обозначения приведены в соответствующих разделах ГОСТ 30319.0.
2 НОРМАТИВНЫЕ ССЫЛКИ
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ 22667-82 Газы горючие природные. Расчетный метод определения теплоты сгорания, относительной плотности и числа Воббе
ГОСТ 30319.0-96 Газ природный. Методы расчета физических свойств. Общие положения
ГОСТ 30319.2-96 Газ природный. Методы расчета физических свойств. Определение коэффициента сжимаемости
ГОСТ 30319.3-96 Газ природный. Методы расчета физических свойств. Определение физических свойств по уравнению состояния
ГСССД 4-78 Плотность, энтальпия, энтропия и изобарная теплоемкость жидкого и газообразного азота при температурах 70-1500 К и давлениях 0,1-1000 МПа
ГСССД 8-79 Плотность, энтальпия, энтропия и изобарная теплоемкость жидкого и газообразного воздуха при температурах 70-1500 К и давлениях 0,1-100 МПа
ГСССД 17-81 Динамическая вязкость и теплопроводность гелия, неона, аргона, криптона и ксенона при атмосферном давлении в интервале температур от нормальных точек кипения до 2500 К
ГСССД 19-81 Кислород жидкий и газообразный. Плотность, энтальпия, энтропия и изобарная теплоемкость при температурах 70-1000 К и давлениях 0,1-100 МПа
ГСССД 47-83 Этилен жидкий и газообразный. Плотность, энтальпия, энтропия и изобарная теплоемкость при температурах 130-450 К и давлениях 0,1-100 МПа
ГСССД 48-83 Этан жидкий и газообразный. Плотность, энтальпия, энтропия и изобарная теплоемкость при температурах 100-500 К и давлениях 0,1-70 МПа
ГСССД 70-84 Гелий-4 жидкий и газообразный. Плотность, энтальпия, энтропия и изобарная теплоемкость при температурах 2,4-450 К и давлениях 0,05-100 МПа
ГСССД 95-86 Криптон жидкий и газообразный. Плотность, энтальпия, энтропия, изобарная теплоемкость и скорость звука при температурах 120-1300 К и давлениях 0,1-100 МПа
ГСССД 96-86 Диоксид углерода жидкий и газообразный. Плотность, фактор сжимаемости, энтальпия, энтропия, изобарная теплоемкость, скорость звука и коэффициент объемного расширения при температурах 220-1300 К и давлениях 0,1-100 МПа
ГСССД 110-87 Диоксид углерода. Коэффициенты динамической вязкости и теплопроводности при температурах 220-1000 К и давлениях от соответствующих разреженному газу до 100 МПа
ГСССД 147-90 Пропан жидкий и газообразный. Плотность, энтальпия, энтропия и изобарная теплоемкость в диапазоне температур 100-700 К и давлений 0,1-100 МПа
3 ОПРЕДЕЛЕНИЕ ПЛОТНОСТИ
3.1 Общие положения
3.1.1 Плотность газа вычисляют по формуле
3.1.2 Плотность определяют с помощью плотномеров любого типа (пикнометрических, ареометрических, вибрационных, акустических, радиационных и др.) или косвенным методом (измерением параметров состояния среды, определения ее состава и проведения расчета).
3.1.3 В зависимости от технико-экономической целесообразности плотность контролируемых сред допускается рассчитывать: вручную, с помощью таблиц и графиков, c применением вычислительных машин и частично или полностью автоматизированных устройств.
3.2 Определение плотности чистых газов
3.2.1 Плотность газа в идеально газовом состоянии определяют по известным значениям давления и температуры по формуле
За молярную массу принимают массу одного киломоля вещества в килограммах.
Молярную массу определяют по формуле
3.2.3 Плотность газа при стандартных условиях определяется при 

Плотность газов



За относительную плотность газа принимается число, показывающее, во сколько раз масса данного газа, заключенная в определенном объеме при данном давлении и температуре, больше или меньше массы сухого воздуха, заключенного в том же объеме при нормальных условиях:
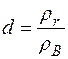
где ρr и ρв — плотности газа и воздуха в кг/м3. Чем жирнее газ, т. е. чем больше он содержит тяжелых компонентов, тем больше его плотность.
Плотность газа может быть также найдена по его относительной молекулярной массе. Для смеси газов их средняя (кажущаяся) молекулярная масса рассчитывается по известному Мольному компонентному составу газа по формуле
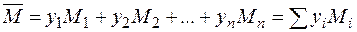
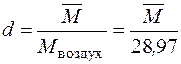
Кроме того, по известной плотности газа при нормальных условиях средняя молекулярная масса газа может быть найдена по формуле
В табл. 2.5 приведены величины относительной плотности (относительно воздуха) некоторых газов.
Таблица 2.5. Относительная плотность некоторых газов (относительно воздуха)
| Газ | Относительная плотность |
| Воздух | |
| Гелий | 0,138 |
| Азот | 0,97 |
| Углекислый газ | 0,518 |
| Сероводород | 1,191 |
| Метан | 0,55 |
| Этан | 1,038 |
| Пропан | 1,52 |
| Бутан | 2,0065 |
Плотности многих углеводородных газов и сероводорода больше плотности воздуха (табл. 2.5). Поэтому они могут накапливаться в помещениях насосных, в колодцах и т. д., где возможны пропуски газа в арматуре оборудования. Это необходимо учитывать при проектировании промыслового хозяйства, при проведении работ на промысле и принимать меры к устранению вредного влияния газов на здоровье персонала.
10.11. Измерение плотности и объема газов
Плотность газа В(рв, г/л) определяют взвешиванием (mв) небольшой стеклянной колбочки известного объема с газом (рис. 274,а) или газового пикнометра (см. рис. 77), применяя формулу
Для уменьшения поправки на потерю массы колбочки с газом в воздухе при ее взвешивании в качестве тары на Другом плече коромысла весов располагают запаянную колбочку точно, такого же объема.

Рис. 274. Приборы для определения плотности газа: колбочка (а) и жидкостной (б) и ртутный (в) эффуэиометры
Поверхность этой колбочки обрабатывают (очищают) каждый раз точно так же, как и взвешиваемой с газом.
В процессе вакуумирования колбочку немного нагревают, оставляя подключенной к вакуумной системе в течение нескольких часов, поскольку остатки воздуха и влаги удаляются с трудом. У вакуумированной колбочки может измениться объем из-за сжатия стенок атмосферным давлением. Погрешность определения плотности легких газов от такого сжатия может достигать 1%. В отдельных случаях для газа определяют и относительную плотность dв, т. е. отношение плотности данного газа рв к плотности другого газа, выбранного в качестве стандартного р0, взятого при тех же температуре и давлении:
Для водорода M0 = 2,016 г/моль, поэтому
Из этого соотношения можно определить молярную массу газа, если принять его за идеальный.
Быстрым методом определения плотности газа является метод измерения продолжительности его истечения из малого отверстия под давлением, которая пропорциональна скорости истечения.
время истечения газа В и воздуха соответственно.
Если для исследуемого газа нельзя подобрать жидкость, в которой он был бы малорастворим, применяют ртутный эффузионетр (рис. 274,в). Он состоит из стеклянного сосуда 4 с трехходовым краном 1 и уравнительного сосуда 5, наполненного ртутью. Сосуд 4 находится в стеклянном сосуде 3, выполняющем функции термостата. Через кран 1 в сосуд 4 вводят газ, вытесняя ртуть ниже метки М1. Выпускают исследуемый газ или воздух через капилляр 2, подняв уравнительный сосуд 5. Более чувствительными приборами для определения плотности газов являются газовый ареометр Штока (рис. 275,а) и газовые весы
Рис. 275. Ареометр Штока (а) и схема установки (б)
Острием Отрубка с шаром опирается на кварцевую или агатовую опору. Трубка с шаром помешены в кварцевый сосуд 5 с пришлифованной круглой пробкой. Вне сосуда расположен соленоид 6 с железным сердечником. При помощи тока различной силы, протекающего через соленоид, выравнивают положение коромысла с шаром так, чтобы волосок 7 указывал точно на индикатор нуля 8. За положением волоска наблюдают при помощи зрительной трубы или микроскопа.
Ареометр Штока приваривают к трубке 2 для устранения каких-либо вибраций.
Шар с трубкой находятся в равновесии при данной плотности окружающего их газа. Если в сосуде 5 один газ заменить на другой при постоянном давлении, то равновесие нарушится из-за изменения плотности газа. Для его восстановления необходимо либо притянуть стержень 3 электромагнитом 6 вниз при понижении плотности газа, либо дать ему подняться вверх при увеличении плотности. Сила тока, протекающего через соленоид, при достижении равновесия прямо пропорциональна изменению плотности.
Объем газа измеряют при помощи калиброванных газовых береток (см. рис. 84) с термостатируемой водяной рубашкой. Во избежание поправок на капиллярные явления газовую 3 и компенсационную 5 бюретки подбирают одинакового диаметра и располагают в термостатируемой рубашке 4 рядом (рис. 276). В качестве запирающих жидкостей применяют ртуть, глицерин и другие жидкости, плохо растворяющие исследуемый газ.
Оперируют этим прибором следующим образом. Сначала заполняют бюретки жидкостью до уровня выше крана 2, поднимая сосуд б. Затем газовую бюретку соединяют с источником газа и вводят его, опуская сосуд б, после чего кран 2 закрывают. Для уравнивания давления газа, находящегося в бюретке 3, с атмосферным давлением сосуд б подносят вплотную к бюретке и устанавливают на такой высоте, чтобы мениски ртути в компенсационной 5 и газовой 3 бюретках были на одном уровне. Поскольку компенсационная бюретка сообщается с атмосферой (ее верхний конец открыт), при таком положении менисков давление газа в газовой бюретке будет равно атмосферному.
Одновременно измеряют атмосферное давление по барометру и температуру воды в рубашке 4 при помощи термометра 7.
Найденный объем газа приводят к нормальным условиям (0 °С; 0,1 МПа), используя уравнение для идеального газа:
Если газ содержит пары воды или находился перед измерением объема в сосуде над водой или водным раствором, то его Oбъем приводят к нормальным условиям с учетом давления пара воды p1 при температуре опыта (см. табл. 37):
Уравнения применяют в том случае, если атмосферное давление при измерении объема газа было сравнительно близко к 760 торр. Давление реального газа всегда меньше, чем у идеального, из-за взаимодействия молекул. Поэтому в найденное значение объема газа вводят поправку на неидеальность газа, взятую из специальных справочников.