днк баррелей что такое
Паниковать не стоит, но лечиться надо. Что мы знаем о вирусе Эпштейна-Барр?
От него не скроешься. Рано или поздно с ним встречается каждый человек. Надо ли его бояться? А может, инфекция совсем безобидна? Паниковать не стоит, но и легкомысленное отношение – ошибка.
О вирусе Эпштейна-Барр рассказала врач-инфекционист «Клиники Эксперт» Тула Елена Геннадьевна Королёва.
— Елена Геннадьевна, что такое вирус Эпштейна-Барр?
— Среди герпес-вирусов насчитывают 8 типов, вызывающих патологии у вида Homo sapiens, то есть у людей. Вирус Эпштейна-Барр – герпес-вирус IV типа. После заражения вирусом Эпштейна-Барр инфекция остаётся в организме навсегда и никогда его не покидает.
Вирус Эпштейна-Барр – один из самых распространённых герпес-вирусов у людей. Восприимчивость к нему человека высока. Многие дети инфицируются до достижения годовалого возраста, а к 40-50 годам инфекция есть в организме практически у каждого.
— Как происходит заражение вирусом Эпштейна-Барр?
— Источник инфекции – вирусоносители, а также больные с типичными (манифестными) и стёртыми формами заболевания. Наиболее распространённый путь передачи – воздушно-капельный: с частицами слюны при разговоре, чихании, кашле. Возможна передача вируса при поцелуе (именно поэтому в некоторых источниках вызванный им инфекционный мононуклеоз называют «болезнью поцелуев»). Возможен и контактный путь заражения (например, через предметы домашнего обихода).
Вирус Эпштейна-Барр проникает в организм через верхние дыхательные пути, и уже оттуда распространяется в лимфоидную ткань, вызывая поражения лимфоузлов, миндалин, селезёнки и печени.
При размножении в организме вирус Эпштейна-Барр воздействует на иммунную систему. Механизм воздействия сложен, но в конечном результате за счёт поражения В-лимфоцитов и угнетения Т-клеточного иммунитета происходит подавление выработки интерферона – белка, отвечающего за противовирусную защиту организма.
В современном мире у детей отмечается всплеск заболеваемости, особенно в городах. Наиболее высока вероятность заразиться в местах скопления людей.
— А бессимптомный носитель может быть опасен?
— Чаще всего источником инфекции становится человек в острой стадии болезни. Но передача от бессимптомного носителя не исключена.
— Какую болезнь вызывает вирус Эпштейна-Барр?
— Классическое проявление – инфекционный мононуклеоз. Для него характерны общие интоксикационные симптомы: высокая температура тела, сонливость, вялость, головные боли, боль в горле, увеличение лимфоузлов (или лимфопролиферативный синдром).
Лимфопролиферативный синдром сочетает:
В общем анализе крови определяется наличие атипичных мононуклеаров. Что это такое? Атипичные мононуклеары (другое их название – «вироциты») – это изменённые одноядерные клетки крови. При течении инфекционного мононуклеоза количество атипичных мононуклеаров в крови повышается значительно (больше 10 %). Может снижаться общее количество тромбоцитов и лейкоцитов, что говорит о тяжести переносимой инфекции.
Есть особенности проявления вируса Эпштейна-Барр у детей. Инфицированные попадают в такую категорию, как «часто болеющие дети». Из-за ослабления иммунитета регулярно возникают заболевания ЛОР-органов, трудности при выздоровлении (подкашливание, постоянно красное горло), бывает храп (из-за разрастания миндалин). При таком течении к взрослому возрасту иммунитет учится противостоять инфекции, взрослые болеют уже не так часто. Показания к оперативному удалению аденоидов у детей практически всегда связаны с непролеченным вирусом Эпштейна-Барр. И это очень печально: ничего лишнего в организме нет, а при своевременном лечении удаления можно было бы избежать.
Читайте материалы по теме:
Знать, что ребёнок инфицирован, важно и по другой причине. Вирус Эпштейна-Барр может изменить реакцию на некоторые антибиотики, спровоцировать токсикоаллергическую реакцию. Поэтому следует обязательно своевременно выявлять вирус и сообщать о нём лечащим врачам, они будут подбирать антибиотики с учётом этого факта.
Тяжёлые последствия возникают, если первичное заражение происходит у женщины в период беременности. Вирус Эпштейна-Барр преодолевает плацентарный барьер, это грозит гибелью плода или значительными дефектами развития.
«После первичного инфицирования некоторые из этих инфекций организм не покидают. Они «спят» в определенных клетках, если с иммунной системой все в порядке и она хорошо контролирует их «сон». Цитата из материала «Чем опасны ТОРЧ-инфекции»
— Есть мнение, что вирус Эпштейна-Барр вызывает гепатит и даже лимфому. Это правда?
— Герпетические вирусы кровотоком разносятся по всему организму, поражают все группы лимфатических узлов. И печень, и селезёнка при остром течении мононуклеоза увеличены. При этом течение болезни обычно благоприятное, здоровье печени полностью восстанавливается.
Утверждать, что вирус Эпштейна-Барр непременно приводит к лимфоме, нельзя. Обнаружить вирус недостаточно: если инфицировано практически всё население планеты, естественно, анализы обнаружат наличие вируса в организме, но ведь лимфомой заболевает далеко не каждый. Конечно, хроническое подавление иммунной системы может приводить к разным нарушениям, в том числе к онкологическим заболеваниям. Но достоверной связи нет. А скомпенсировать иммунные нарушения современная медицина в силах.
Паниковать точно не стоит. Но и надеяться на самостоятельное излечение не надо. Когда ребёнок постоянно болеет, родители зачастую впадают в отчаяние. И хотя избавиться от герпес-вирусов навсегда невозможно, вполне можно облегчить состояние и в разы уменьшить частоту заболеваний. Лечиться можно и нужно.
Подробнее о гепатитах читайте в наших статьях:
— Какими методами можно проверить, присутствует ли в организме вирус Эпштейна-Барр? Какие анализы его выявляют?
— В нашем арсенале два метода: иммуноферментный анализ (ИФА) и полимеразная цепная реакция (ПЦР). Преимущество метода ПЦР – возможность определить ДНК вируса в слюне, соскобе из носоглотки. Благодаря этому можно не брать кровь и не нервировать ребёнка. Но если нет обострения, такой анализ может дать ложноотрицательный результат. Это значит, что вирус в организме есть, но он «спит», и, соответственно, в мазке из носоглотки может отсутствовать. А поскольку с помощью ПЦР ищут сам вирус, точнее, его нуклеиновые кислоты (ДНК), то и анализ будет отрицательным. Нередки также искажения из-за того, что мазок взят неправильно.
Метод ИФА точнее, он в любом случае покажет и наличие инфекции, и выраженность инфекционного процесса. Выводы в данном случае делают по присутствию в крови специфических иммуноглобулинов (антител) к вирусу. Например, если обнаружены иммуноглобулины класса М (IgM), можно говорить об острой фазе инфекции (первичном заражении либо реактивации вируса, когда-то попавшего в организм). Если найдена определённая фракция иммуноглобулина класса G (IgG), это свидетельствует, что организм в прошлом уже сталкивался с инфекцией. Поэтому для определения диагностического метода нужна консультация врача.
— Какими методами лечения вируса Эпштейна-Барр располагает современная медицина?
— Это сложная задача. Если для герпес-вирусов I и II типа (вирусов простого герпеса) есть специфические противовирусные средства, то для вируса Эпштейна-Барр и цитомегаловируса специфической терапии пока не разработали. При лёгком течении болезнь может пройти сама, но при тяжёлом течении с поражением костного мозга медицинская помощь необходима. Лечение направлено на стимуляцию иммунитета, применяются интерфероны. Схему лечения выбирают, исходя из множества факторов, определять её должен только врач.
После излечения вирус продолжает жить в организме. Периодически могут возникать обострения: из-за переохлаждения, длительного пребывания под солнцем, стресса и т. д. Проявления инфекции – всегда повод идти к врачу.
Беседовала Дарья Ушкова
Редакция рекомендует:
Для справки:
Королёва Елена Геннадьевна
Днк баррелей что такое
Выявление возбудителя клещевого боррелиоза (Borrelia burgdorferi), в ходе которого с помощью метода полимеразной цепной реакции в реальном времени (РТ-ПЦР) определяется генетический материал (ДНК) боррелий в крови, ликворе.
Синонимы английские
Borrelia burgdorferi sensu lato.
Метод исследования
Полимеразная цепная реакция (ПЦР).
Какой биоматериал можно использовать для исследования?
Венозная кровь, ликвор.
Общая информация об исследовании
Borrelia burgdorferi sensu lato – группа бактерий, состоящая из 10 геновидов, из которых минимум три – Borrelia burgdorferi sensu stricto, Borrelia garini и Borrelia afzelii – вызывают болезнь Лайма (клещевой боррелиоз). Borrelia имеют форму спирали, крайне подвижны.
Болезнь Лайма – заболевание, передающееся человеку через укус зараженного иксодового клеща и характеризующееся поражением кожи, опорно-двигательного аппарата, нервной и сердечно-сосудистой систем и склонностью к длительному течению. Название оно получило от города Лайм, где была зафиксирована вспышка артритов инфекционной этиологии у детей. Болезнь распространена на территории России, в Америке, Европе, Азии. Природным «резервуаром» боррелий являются животные (млекопитающие и птицы), как правило, дикие. Через зараженную кровь животного боррелия попадает в организм клеща, который является переносчиком болезни. От человека или животного к человеку заболевание не передается. На опасность заражения влияет количество зараженных клещей – в эндемичных районах оно может достигать 40 %. Инкубационный период составляет 3-32 дня. В месте укуса клеща через несколько дней образуется мигрирующая кольцевидная эритема – покраснение кожи, увеличивающееся в размерах, с постепенно светлеющим центром, при этом ощущается зуд или жжение. Кольцевидная эритема – специфический симптом болезни Лайма, облегчающий диагностику, однако у 20-30 % пациентов начало болезни не сопровождается кожными проявлениями. Также отмечаются слабость, повышение температуры, головная боль, увеличение лимфатических узлов.
Следующая фаза болезни – диссеминированная. Из места первичного заражения боррелии разносятся по организму, поражая различные органы. Диссеминированная форма продолжается несколько месяцев и без лечения переходит в персистирующую, которая может длиться годами. При неблагоприятном течении вероятен переход в резидуальную стадию – это необратимые структурные изменения органов.
При клещевом боррелиозе чаще поражаются опорно-двигательная, нервная, сердечно-сосудистая система, глаза, печень, почки, при этом развивается клиническая картина невритов, радикулитов, энцефалитов, артритов, конъюнктивитов, миокардитов, появляется сыпь вне места укуса клеща.
Во время беременности может произойти инфицирование плаценты и самопроизвольное прерывание беременности.
Лечение включает антибиотикотерапию, дезинтоксикацию, назначение противовоспалительных препаратов. Вакцинация против болезни Лайма не проводится.
Диагностика клещевого боррелиоза, особенно диссеминированной и персистирующей форм, представляет некоторые трудности из-за разнообразных клинических проявлений.
Помогает диагностике и позволяет заподозрить клещевой боррелиоз факт укуса, однако часто пациент не знает о нем. Этому способствует то, что переносчиками являются личиночные формы клещей, уступающие по размерам взрослым особям, сам укус безболезнен и, наконец, клещ может укусить в труднодоступное для обзора место (например, в волосистую часть головы).
ПЦР – полимеразно-цепная реакция – выявляет в тканях больных клещевым боррелиозом генетический материал Borrelia burgdorferi sensu lato, отсутствующий у здоровых людей. Это специфичный и быстрый метод диагностики клещевого боррелиоза. ПЦР позволяет поставить диагноз в ранние сроки и назначить подходящее лечение, что помогает предотвратить переход болезни в персистирующую стадию и развитие осложнений. Кроме того, ПЦР дает возможность контролировать эффективность лечения – положительный результат означает наличие возбудителя и необходимость продолжения приема препаратов или его корректировки. Взятие материала непосредственно из пораженного органа позволяет установить роль боррелий в конкретном заболевании. Так, например, у части больных клещевым боррелиозом формируются поражения суставов – артрит – аутоиммунной природы, при этом возбудитель в суставной жидкости отсутствует, что требует иного подхода в лечении по сравнению с инфекционным артритом, вызванным боррелией. Наконец, ПЦР, как исследование, направленное на обнаружение возбудителя в пораженном органе, позволяет правильно поставить диагноз и назначить лечение в ситуации, когда на фоне клещевого боррелиоза развилась другая болезнь, с ним не связанная.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Референсные значения: отрицательно.
Причины положительного результата
Причины отрицательного результата
Что может влиять на результат?
Прием антибиотиков (необходимо обсудить с врачом вопрос отмены терапии перед исследованием).
Диагностика персистирующей и диссеминированной форм болезни Лайма, основанная на клинических проявлениях, усложняется со временем, прошедшим от начала болезни, так как поздние симптомы менее специфичны по сравнению с ранними.
Кто назначает исследование?
Инфекционист, кардиолог, невролог, офтальмолог, ревматолог, акушер-гинеколог, терапевт, гастроэнтеролог, нефролог.
Клещевой боррелиоз: болезнь на всю жизнь?
Клещевой энцефалит — опасное вирусное заболевание, поражающее центральную нервную систему, — вряд ли нуждается в представлении, особенно в связи с недавним всплеском заболеваемости. А вот к проблеме другой, но уже бактериальной, инфекции, также переносимой клещами, внимание врачей и ученых России было привлечено сравнительно недавно
В России боррелиоз (или болезнь Лайма, как ее называют в США) был впервые серологически (т. е. на основе наличия специфических антител) выявлен сотрудниками научно-исследовательского института эпидемиологии и микробиологии им. Н. Ф. Гамалеи РАМН под руководством Э. И. Коренберга в 1985 г. Но только в 1991 г. иксодовые клещевые боррелиозы (ИКБ) были включены в официальный государственный перечень заболеваний, регистрируемых на территории России.
Наиболее распространенным этот недуг признан в США: ежегодно там заболевает более 16 тыс. человек. Рост заболеваемости боррелиозом в настоящее время наблюдается и во многих странах Европы.
Возбудитель — спирохета
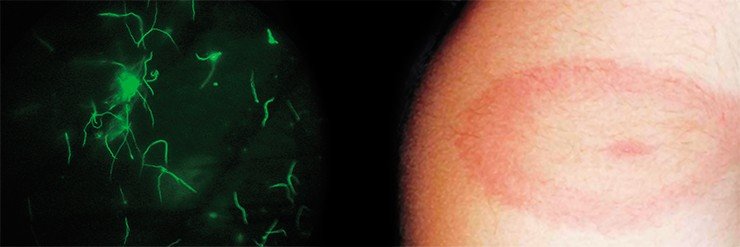
Уже из самого названия видно, что переносчиками этой болезни, также как и клещевого энцефалита, являются клещи. В США болезнь Лайма переносят клещи Ixodes scapularis (в 1982 г. американский исследователь В. Бургдорфер именно от этих клещей впервые изолировал самих инфекционных агентов — боррелий); в Европе эту функцию выполняют клещи Ixodes ricinus, а у нас — печально известные таежные клещи Ixodes persulcatus.
Возбудитель боррелиоза — спирохета комплекса под пышным латинским названием Borrelia burgdorferi sensu lato (s. l.) — состоит в близком родстве с трепонемой — возбудителем всем известного сифилиса — и лептоспирой — возбудителем лептоспироза, серьезного заболевания, которому подвержены многие виды животных, и человек в том числе. Все перечисленные спирохеты имеют сходный внешний вид и по форме напоминают извитую спираль.
К сегодняшнему дню на основании генетических и фенотипических различий выделено 12 видов боррелий, но опасными для человека до недавнего времени считалось только три вида: B. burgdorferi sensu stricto (s.s.), B. afzelii и B. garinii. Однако в последнее время появились сообщения, что от больных ИКБ был выделен еще один вид — B. spielmanii, что говорит о возможной патогенности и этого вида.
Боррелии способны не только передвигаться под кожей, но и проникать в кровеносные сосуды, перемещаясь с током крови во внутренние органы. Не является для них преградой и гематоэнцефалический барьер, защищающий кровеносные сосуды мозга
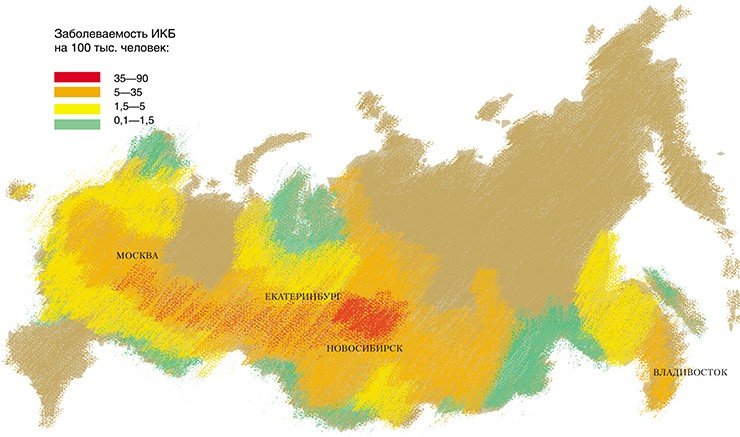
Боррелии распространены по регионам мира неравномерно. В России основное эпидемиологическое значение имеют два вида — B. afzelii и B. garinii, которые обнаружены в обширной лесной зоне от Прибалтики до Южного Сахалина.
В Институте химической биологии и фундаментальной медицины изучение боррелий было начато в 2000 г. Исследования, проведенные совместно с Институтом систематики и экологии животных СО РАН, направленные на выявление видового разнообразия боррелий, циркулирующих в природных очагах ИКБ Новосибирской области, позволили установить ряд фактов. Помимо широко распространенных B. afzelii и B. garinii были обнаружены редко встречающиеся генетические варианты этих видов.
Согласно данным световой микроскопии, зараженность таежных клещей боррелиями на территории Новосибирской области составляет 12—25 %. При микроскопическом исследовании фиксированных и витальных препаратов боррелии были выявлены как у взрослых клещей, собранных с растений, так и у частично или полностью напитавшихся личинок и нимф.
Поскольку эти спирохеты были обнаружены на всех стадиях развития клещей — от личинок до взрослых особей (имаго), все они могут служить источниками заражения. Цикл переноса возбудителя начинается с процесса питания неинфекционного клеща на инфицированном животном. Клещи, зараженные боррелиями, при следующем кормлении способны передавать эти микроорганизмы здоровым животным, а также продолжать воспринимать дополнительную «порцию» спирохет от инфицированных млекопитающих. На ранних этапах развития клеща в данный процесс вовлечены мелкие млекопитающие; взрослые клещи начинают питаться на крупных млекопитающих, и кроме того могут «покушаться» на человека, заражая его.
Проникнув в тело млекопитающего вместе со слюною клеща, спирохеты начинают усиленно размножаться в кожных покровах на месте укуса. Они способны не только передвигаться под кожей, но и проникать в кровеносные сосуды, перемещаясь с током крови во внутренние органы. Не является для них преградой и гематоэнцефалический барьер: размножаясь в спинномозговой жидкости, боррелии становятся причиной тяжелых нейроинфекций.
Первая стадия — обратимая
Иксодовый клещевой боррелиоз — полисистемное заболевание, при котором возможны поражения кожи, опорно-двигательного аппарата, нервной и сердечно-сосудистой систем. Характер клинических проявлений заболевания зависит от его стадии. Условно выделяют три стадии боррелиозной инфекции, хотя четко различить их не всегда удается. Заболевание, как правило, развивается последовательно, переходя из одной стадии в другую.
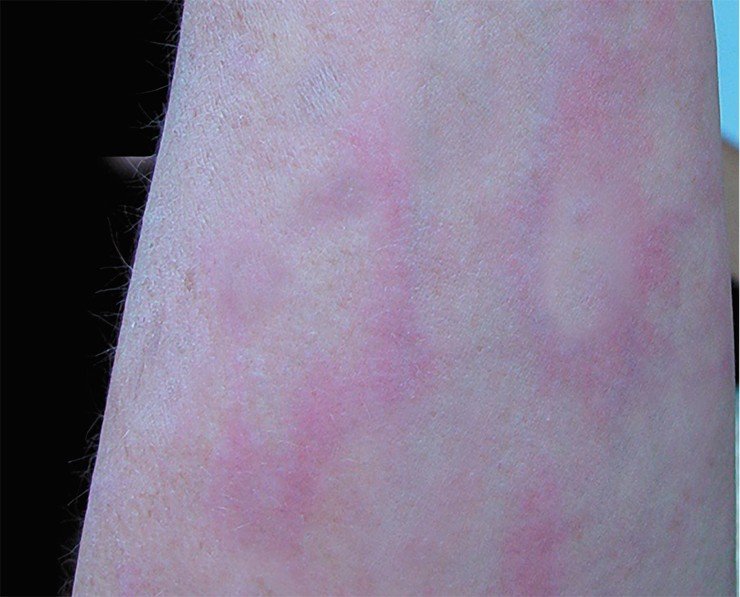
Первая стадия длится от 3 до 30 дней. За этот отрезок времени на коже (в области укуса клеща) вследствие воспалительной реакции может появиться красное кольцо, которое так и называется: кольцевая мигрирующая эритема. Начинается она с небольшого пятна в месте присасывания клеща, которое постепенно мигрирует к периферии. В типичных случаях центр пятна светлеет, а периферические участки образуют яркий красный валик в виде кольца неправильной формы диаметром до 15 см.
Исследования кожных проб, взятых из разных участков эритемы, свидетельствуют о том, что в центре эритемного кольца боррелии практически отсутствуют, но, как правило, они всегда обнаруживаются на периферии. По сравнению с другими воспалительными изменениями эритема может сохраняться на коже в течение достаточно длительного промежутка времени.
Примерно у четверти больных кожные проявления заболевания сопровождаются такими симптомами, как: озноб, сонливость, мышечная слабость, боли в суставах и увеличение лимфатических узлов. Это сигнализирует о том, что боррелии распространяются по организму. Однако у большинства больных с эритемой ранние стадии болезни не сопровождаются симптомами интоксикации. К тому же, существует и так называемая безэритемная форма, которая, как правило, начинается остро и осложнена высокой температурой, болью в суставах и головной болью.
Также нужно отметить, что отсутствие симптомов болезни в первое время после укуса клеща не исключает развития болезни в будущем. При проведении своевременного лечения на первой стадии заболевания возможно полное выздоровление.
Лечение поздней стадии боррелиоза, развивающейся через полгода — год после заражения, требует длительного курса антибактериальной терапии. И борьба с хронической болезнью не всегда бывает успешной
Вторая стадия боррелиоза развивается в среднем через 1—3 месяца после инфицирования. К этому времени боррелии с током крови и лимфы попадают в различные органы и ткани, такие как: мышцы, суставы, миокард, спинной и головной мозг, а также селезенка, печень, сетчатка глаза, — и поражают их. Вот почему данную стадию характеризует столь значительное разнообразие клинических проявлений заболевания: неврологических, сердечных, кожных и т. д.
Признаки поражения нервной системы проявляются в виде менингита, моно- и полиневритов, очень часто — неврита лицевого нерва и др. Многие из этих симптомов могут наблюдаться одновременно. Наиболее частым неврологическим проявлением можно назвать менингополирадикулоневрит (синдром Баннаварта), характеризующийся парезом лицевого нерва. Кроме того, на этой стадии у некоторых больных могут появиться вторичные эритемы.
Наконец, третья стадия боррелиоза развивается через полгода — год после проникновения инфекции в организм. Чаще всего встречаются поражения суставов (хронический артрит), кожи (атрофический акродерматит) и хронические поражения нервной системы (хронический нейроборрелиоз). Лечение поздней стадии боррелиоза требует длительного курса антибактериальной терапии, однако впоследствии у некоторых больных с артритами признаки хронической инфекции наблюдаются в течение месяцев и даже нескольких лет после курса лечения антибиотиками.
Иммунный ответ
В развитие боррелиозной инфекции, как правило, вовлечено несколько патогенных механизмов. Некоторые синдромы, такие как менингит и радикулит, вероятно, отражают результат прямой инфекции органа, а вот артрит и полиневрит могут быть связаны с непрямыми эффектами, вызванными вторичным аутоиммунным ответом.
Иммунный ответ организма на боррелиозную инфекцию проявляется по-разному. Для контроля над распространением инфекции организм использует как врожденный (неспецифическая резистентность), так и адаптивный специфический иммунный ответ, т. е. выработку специфических антител против инфекционного агента. В течение первых двух недель после начала болезни у большинства пациентов действительно обнаруживаются иммуноглобулины против определенных антигенов боррелий — инфекционных белков, запускающих в организме механизм иммунного ответа.
Еще в 90-х гг. прошлого века в США были проведены первые исследования, направленные на разработку антиборрелиозной вакцины. Но и на сегодняшний день эффективной вакцины, предохраняющей от этого опасного заболевания, не существует. Вероятно, трудности с получением безопасных вакцин имеют отношение к особенностям иммунного ответа, наблюдаемого при боррелиозной инфекции. Он может инициировать выработку антител против некоторых собственных белков организма, т. е. вызвать опасные аутоиммунные реакции.
Причиной подобного иммунного ответа является молекулярная мимикрия, сходство (например, между липопротеином боррелий OspA и белком адгезии hLFA-1α), который вырабатывается нашими Т-клетками в синовиальной оболочке, выстилающей внутренние поверхности суставов. Так, осложнения, возникающие после проведения вакцинации вакциной на основе липопротеина OspA, в большинстве случаев проявлялись в виде артритов и аутоиммунных ревматоидных артритов. Работа по созданию приемлемой, безвредной и в то же время эффективной вакцины продолжается до сих пор.
Как диагностировать ИКБ?
Диагностику ИКБ обычно проводят на основании так называемого эпидемиологического анамнеза (установления факта посещения леса, укуса клеща), а также клинических признаков заболевания, главным из которых является наличие мигрирующей эритемы.
Особую сложность для диагностики представляют заболевания, протекающие в безэритемных формах, одновременно с другими инфекциями, переносимыми клещами, например клещевым энцефалитом или анаплазмозом. В клинической практике известны случаи, когда у больного одновременно были выявлены безэритемная форма боррелиоза и клещевого энцефалита, которые привели его к повторной госпитализации по причине осложнений.
Случаи безэритемных форм можно диагностировать только с помощью лабораторных тестов. Выделение боррелий из проб кожи, проб сыворотки крови, спинномозговой или синовиальной жидкостей на специальные среды методом культивирования требует наличия специальных условий, дорогостоящих реактивов, занимает много времени, а главное — малоэффективно.
Первые исследования, направленные на разработку антиборрелиозной вакцины, были проведены еще в 90-х гг. прошлого века.
Но и на сегодняшний день эффективной вакцины против этого опасного заболевания не существует
Микроскопические исследования используются обычно при проведении анализа зараженности боррелиями клещей, но практически не применяются при диагностике ИКБ, поскольку в тканях и жидкостях организма инфицированного человека боррелии не накапливаются в таких количествах, чтобы их можно было обнаружить под микроскопом.
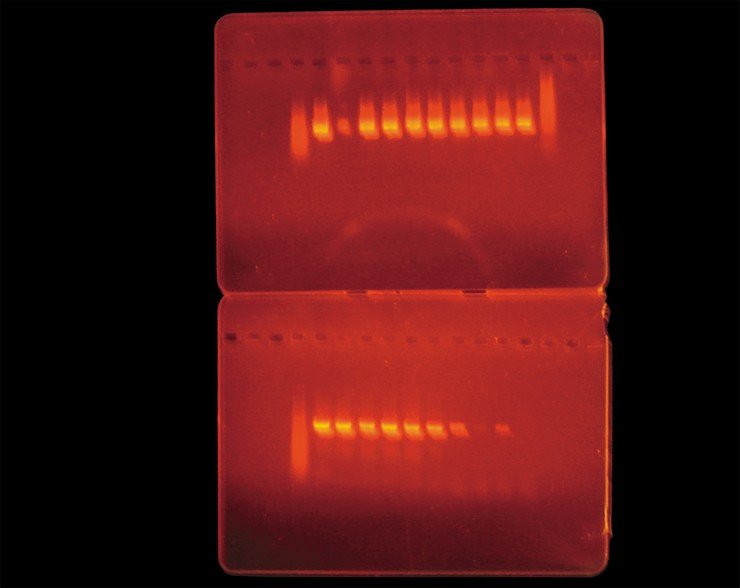
Для выявления боррелий может использоваться полимеразная цепная реакция (ПЦР), проведение которой позволяет обнаружить ДНК возбудителя. При проведении таких исследований нами было показано, что число боррелий, содержащихся в одном клеще, варьирует от одной до шести тысяч. Однако в настоящее время метод на основе ПЦР, как и все остальные методы диагностики боррелиоза, использовать в качестве самостоятельного теста для диагностики заболевания не рекомендуется, поскольку в данном случае чувствительность этого метода недостаточна, что может привести к так называемым «ложноотрицательным» результатам.
Тем не менее, при проведении совместных работ с Муниципальной инфекционной больницей № 1 г. Новосибирска было показано, что на ранней стадии болезни, до начала лечения, в комплексной диагностике заболевания метод ПЦР вполне применим наряду с иммунологическими методами анализа.
Для своевременного выявления смешанной инфекции определение ДНК необходимо проводить в первые четыре недели после присасывания клещей. Однако отрицательный результат, который при этом может быть получен, не исключает наличия заболевания и через 3—6 недель требует проведения серологических тестов (на специфические антитела).
Выявление антител к белкам боррелий сегодня и является основным способом лабораторной диагностики. В США и в странах Европы для повышения надежности серодиагностики боррелиоза было рекомендовано использовать двухступенчатую схему тестирования сывороток крови, однако в России двухступенчатый подход не применяется из-за отсутствия отечественных тест-систем. Кроме того, иммуноглобулины из сыворотки крови больных ИКБ могут по-разному реагировать с основными белками разных видов боррелий, поэтому критерии тестирования, разработанные для одной страны, могут быть непригодны для другой.
В России сейчас широко применяют серологические методы детекции: иммуноферментный анализ (ИФА) и реакцию непрямой иммунофлюоресценции (РНИФ), диагностическая значимость которых сопоставима. Однако применение второго метода может быть ограничено тем, что существует вероятность перекрестных реакций с близкородственными боррелиям микроорганизмами, в частности с Treponema palladium, возбудителем сифилиса. В целом же эффективность выявления у больных антител даже с помощью применения комбинации современных серологических тестов зависит от стадии заболевания.
Так что же такое боррелиоз — обычная инфекция или болезнь на всю жизнь? В действительности этот недуг не так безобиден, как представляется на первый взгляд.Иногда инфицирование организма боррелиями вызывает тяжелые отдаленные последствия, заболевания, которые только при ближайшем рассмотрении удается связать с боррелиозом, ранее перенесенным пациентами.
Благоприятный исход этого серьезного бактериального заболевания, переносимого клещами, во многом зависит от проведения своевременной, адекватной диагностики и соответствующей терапии. И лечение ИКБ должно заключаться не в бездумном приеме антибиотиков, как это иногда случается. Это — дело профессионалов, которые способны выявить не только клиническую симптоматику, но также индивидуальные особенности течения болезни и наличие сопутствующих заболеваний.