глицинат железа или бисглицинат в чем разница
Применение бисглицината железа у беременных и кормящих женщин
Несмотря на возросший уровень жизни, железодефицитная анемия (ЖДА) продолжает занимать ведущую позицию в структуре заболеваемости во всем мире. Распространённость анемии во время беременности значительно варьирует из-за различий в социально-экономических условиях, стиле жизни и практик по улучшению здоровья, применяемых в разных странах. По подсчётам ВОЗ, у 41,8% беременных женщин в мире наблюдается концентрация гемоглобина, указывающая на наличие анемии, что составляет 56 миллионов человек [1].
Уровни распространённости анемии среди беременных женщин варьируют в пределах 17,3–30,8% для Америки, 18,6–31,6% для Европы, 43,9–52,5% для Юго-Восточной Азии и 52,8–61,3% для Африки [1]. Экспертами ВОЗ опубликованы уровни значимости анемии для общественного здоровья и оценка количества стран относительно встречаемости анемии при беременности (таблица 1) [1,2].
анемии в популяции (%)
Уровень значимости для общественного здоровья
Не представляет значимости для
Представляет умеренную значимость для общественного здоровья
Значима для общественного здоровья
Представляет высокую значимость для
Опубликованные данные свидетельствуют о том, что у 2–7% беременных женщин концентрация гемоглобина составляет менее 70 г/л, и, вероятно у 15–20% уровень гемоглобина составляет менее 80 г/л [3,4]. Совет экспертов ВОЗ считает тяжелую анемию одной из основных причин материнской смертности в мире [5]. Кроме того, материнская анемия все еще является причиной высокой перинатальной заболеваемости и смертности [6, 7, 8].
По данным различных авторов до 95% случаев анемии у беременных женщин связаны с ДЖ [9,10]. К другим причинам анемии при беременности относят дефицит фолатов и витамина В12, гемолитические заболевания (серповидноклеточная анемия, малярия), хроническую кровопотерю, гельминтозы, гемоглобинопатии и др. [6, 11].
Анемия во время беременности определяется Всемирной организацией здравоохранения как уровень гемоглобина ≤ 11. г / дл. По оценкам Всемирной организации здравоохранения, в мире показатель распространенности составляет 38% среди беременных женщин. Лечение железодефицитной анемии во время беременности остается в числе основных направлений здравоохранения. Для лечения железодефицитной анемии рекомендуют пероральные соли железа, например, фумарат железа. Увеличение дозы фумарата двухвалентного железа увеличивает биодоступность препарата железа, однако такое увеличение приводит к росту частоты побочных эффектов со стороны желудочно-кишечного тракта таких как: тошнота, запор, диарея, метеоризм и окрашивание стула в черный цвет. Кроме того, биодоступность фумарата железа в желудочно-кишечном тракте может снизиться при приеме многих продуктов и/или препаратов, которые мешают его абсорбции, что приводит к вариабельности коррекции гемоглобина во время лечения. [12]
Бисглицинат железа представляет собой хелатный комплекс двухвалентного железа ковалентно соединенного с двумя молекулами аминокислоты глицина (хелатирование железа). В исследованиях подтверждается, что бисглицинат железа лучше переносится пациентами из-за меньшего количества побочных эффектов со стороны желудочно-кишечного тракта. [12]
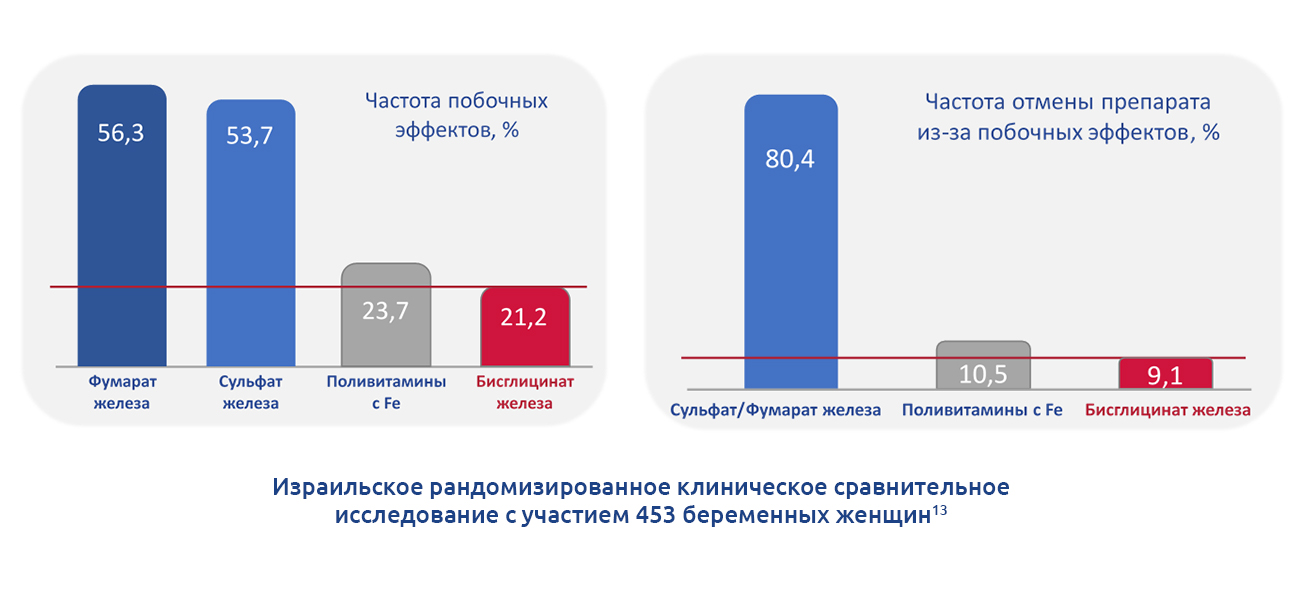
Также исследования показывают, что бисглицинат железа улучшает абсорбцию и запасы железа, а также повышает уровень гемоглобина лучше, чем ионные соли железа [12, 14] или полимальтозный комплекс железа [15]. Так, в исследовании Nils Milman и соавторы показано, что бисглицинат железа в дозировке 25 мг так же эффективен, как и сульфат железа 50 мг в профилактике дефицита железа и анемии во время беременности. [12, 14]
В исследовании Oscar Pineda и соавт. показано, что хелат бисглицината двухвалентного железа абсорбируется в 3,4 раза лучше, чем сульфат железа (биодоступность бисглицината железа и сульфата железа составила 90,9% и 26,7%, соответственно); а прием хелатного комплекса бисглицината железа привел к значительному увеличению ферритина (P [18] L-метилфолат, как кофермент, фактор роста и деления клеток, обеспечивает необходимый уровень эритропоэза.[19]
Для лечения анемии беременных компания «Ламира» предлагает Multizan® Феррум L, в состав которого входит оба компонента: бисглицинат железа 30 мг и L-метилфолат 400 мкг – в необходимой дозировке, рекомендованной ВОЗ.
Таким образом, очевидные преимущества Multizan® Феррум L в отношении эффективности, безопасности и переносимости дают основание рекомендовать его беременным и лактирующим женщинам с дефицитом железа, а также, для его профилактики.
1. Worldwide prevalence of anaemia 1993–2005: WHO global database on anaemia / B. Benoistr [et al.]. – Geneva: WHO Press, 2008. – 41 p.
2. Iron deficiency anemia assessment, prevention, and control. A guide for programme managers. – Geneva: World Health Organization, 2001. – 115 p.
3. Kongnyuy, E. Effets de la supplémentation systématique en fer, par voie orale, avec ou sans acide folique, chez la femme enceinte: Aspects pratiques de la BSG (dernière mise à jour: 4 janvier 2007) / E. Kongnyuy, N. van den Broek // Bibliothèque de Santé Génésique de l’OMS; Genève: Organisation mondiale de la Santé. [Ressource électronique]. – 2007.
4. Van den Broek, N. Anemia and micronutrient deficiencies / N. van den Broek // Br. Med. Bull. – 2003. – № 67. – P. 149–160.
5. Walraven, G. Treatments for iron-deficiency anaemia in pregnancy: RHL commentary (last revised: 20 June 2007). / G. Walraven // The WHO Reproductive Health Library; Geneva: World Health Organization. [Electronic resource]. – 2007.
6. Candio, F. Treatments for iron-deficiency anaemia in pregnancy: RHL commentary (last revised: 23 November 2007) / F. Candio, G.J. Hofmeyr // The WHO Reproductive Health Library; Geneva: World Health Organization. [Electronic resource]. – 2007.
7. Cutner, A. Failed response to treat anaemia in pregnancy: reasons and evaluation / A. Cutner, R. Bead, J. Harding // J. Obstet. Gynecol. – 1999. – № 102. – P. 523–527.
8. Maternal anaemia and its impact on perinatal outcome / F.W. Lone [et al.] // Tropical Medicine and International Health. – 2004. – Vol. 9, № 4. – P. 486 – 490.
9. Лакотко, Н.Н. Дефицит железа у беременных женщин: лечебно-диагностические аспекты, лактация, качество жизни: дис. … канд. мед.наук : 14.00.01 / Н.Н. Лакотко. – Минск, 2008. – 146 л.
10. Хух, Р. Анемия во время беременности и в послеродовом периоде / Р. Хух, К. Брейман. – Москва: Триада-Х, 2007. – 73 с.
11. Reveiz, L. Treatments for iron-deficiency anaemia in pregnancy (Review) / L. Reveiz, G.M.L. Gyte, L.G. Cuervo // The Cochrane Library. – 2007. – Issue 4. – John Wiley & Sons, 2007. – 109 p.
12. Реестр клинических исследований США «Эффективность бисглицината железа в лечении железодефицитной анемии у беременных»
14. Nils Milman, Lisbeth Jønsson, Pernille Dyre, Palle Lyngsie Pedersen and Lise Grupe Larsen
Ferrous bisglycinate 25 mg iron is as effective as ferrous sulfate 50 mg iron in the prophylaxis of iron deficiency and anemia during pregnancy in a randomized trial. JOURNAL OF PERINATAL MEDICINE. Mar 2014, p.197
16. Oscar Pineda, PhD, and H. DeW ayne Ashmead, PhD Effectiveness of Treatment of Iron-Deficiency
Anemia in Infants and Young Children With Ferrous Bis-glycinate Chelate Nutrition 2001;17:381–384.
17. Pineda O, Ashmead HD, Perez JM, Ponce-Lemus C. Effectiveness of iron amino acid chelate on the treatment of iron deficiency anemia in adolescents. J Appl Nutr 1994;46:2
18. Рандомизированное клиническое исследование по двойному слепому методу. Международный журнал по акушерству и гинекологии, сентябрь 2002 г., том 109, стр. 1009-1014 Джордж Джарез-Вазкез (а), Эрминио Бониззони (b), Аурелио Скотти (с*)
19. «ДОСТИЖЕНИЯ И РИСКИ ПРИМЕНЕНИЯ ФОЛАТОВ ВНЕ И ВО ВРЕМЯ БЕРЕМЕННОСТИ» О.А. ПУСТОТИНА, д.м.н., профессор, кафедра акушерства, гинекологии и репродуктивной медицины Российского университета дружбы народов. Медицинский совет, №9,2015
Эффективность и безопасность препаратов трехвалентного железа в лечении железодефицитной анемии
Рассмотрено применение препаратов железа на основе гидроксид-полимальтозного комплекса в лечении железодефицитной анемии. Показано, то они сопоставимы по эффективности с солевыми препаратами железа, но при их использовании значительно реже возникают нежел
Application of iron preparations based on hydroxide-polimaltosis for complex treatment of iron-deficiency anemia is examined. It is stated that in terms of efficiency they can be compared with the salt preparations of iron, but with their use undesirable phenomena appears considerably more rarely.
В настоящее время фармацевтическая промышленность выпускает довольно большое количество препаратов железа для лечения железодефицитной анемии (ЖДА) и продолжается разработка новых препаратов. Возникла необходимость классифицировать препараты железа (рис. 1) и описать их свойства для того, чтобы облегчить выбор. В зависимости от способа введения в организм препараты железа делятся на пероральные и парентеральные (внутривенные, внутримышечные). Пероральные препараты могут содержать различные соли железа (молекулы небольшого размера) или гидроокись железа с полимальтозным комплексом (молекулы большого размера, более 50 кД). Пероральные препараты железа могут быть простыми, т. е. содержащими только соединение железа, или комбинированными с добавлением других веществ (аскорбиновой кислоты, фолиевой кислоты, витамина В12, микроэлементов и других веществ). Комплексы железа для внутривенного введения могут содержать декстран (высокомолекулярный или низкомолекулярный), сахарозу или карбоксимальтозу.
Многие годы «золотым стандартом» среди пероральных препаратов железа являлся сульфат железа. Последний представляет собой солевой препарат железа, который недорог в производстве и, соответственно, имеет невысокую стоимость. Кроме того, оказалось, что сульфат железа обладает высокой всасываемостью в организме, которая выше, чем у глюконата, хлорида или фумарата железа. По этой причине в настоящее время выпускается большое количество препаратов железа, содержащих сульфат железа (Актиферрин, Гемофер пролонгатум, Сорбифер Дурулес, Тардиферон, Ферроплекс, Ферроградумет, Ферро-Фольгамма и др.) [1].
При использовании солевых препаратов железа возможно локальное раздражение слизистой оболочки желудка в месте растворения препарата и слизистой оболочки двенадцатиперстной кишки, где преимущественно происходит всасывание препарата. Процесс всасывания является пассивным, быстрым и дозозависимым. В связи с низкой молекулярной массой солевые препараты железа могут всасываться в большом количестве, приводя к опасным для организма концентрациям, что может вызвать интоксикацию и отравление. Диссоциация солей двухвалентного железа происходит в желудочно-кишечном тракте и сопровождается выделением свободных ионов железа. Следующим процессом метаболизма солевых препаратов железа является окисление, которое осуществляется также в желудочно-кишечном тракте и заключается в переходе двухвалентного железа в трехвалентное. Последнее поступает в кровь и в плазме связывается с транспортным белком — трансферрином и в виде этого комплекса (металлопротеина) направляется в костный мозг и органы депо железа (печень, селезенка). Возврат железа из этих органов осуществляется через лимфатическую систему. Нарушение процесса окисления приводит к высвобождению электронов, образованию свободных радикалов, активации перекисного окисления липидов, повреждению клеток паренхиматозных органов.
В процессе лечения ЖДА солевыми препаратами железа могут возникнуть следующие проблемы:
.jpg)
Препараты железа на основе ГПК обладают следующими свойствами и преимуществами перед солевыми препаратами железа [5]:
На сегодняшний день в арсенале врача имеются современные препараты трехвалентного железа на основе различных полисахаридных комплексов [1]: пероральные препараты железа на основе ГПК (Мальтофер, Мальтофер Фол, Феррум Лек); препараты железа на основе ГПК (Феррум Лек — раствор для внутримышечного введения); препараты железа на основе гидроксид сахарозного комплекса (Венофер — раствор для внутривенного введения); препараты железа на основе карбоксимальтозата (Феринжект) и другие.
Международной тенденцией является смена солевых препаратов железа на препараты железа на основе ГПК [6].
ЖДА — самое «благодарное» гематологическое заболевание и должна вылечиваться сразу и навсегда, что и наблюдается в большинстве случаев. Причинами неуспешного лечения ЖДА препаратами железа являются:
Лечение латентного дефицита железа (ЛДЖ), который рассматривается как предстадия ЖДА и характеризуется снижением запасов железа в депо при нормальной концентрация гемоглобина, проводится пероральными препаратами железа в 50-процентной дозировке в течение 2 мес [9]. Основная задача лечения ЛДЖ — пополнить запасы железа в депо и не дать этому состоянию перейти в ЖДА.
.gif)
Особенностью лечения указанных двух форм дефицита железа (ЛДЖ и ЖДА) является длительное применение пероральных препаратов железа, при котором часто возникают указанные выше нежелательные явления [11].
Показано, что препараты железа на основе ГПК обладают сходной с сульфатом железа биодоступностью [12], обладают стабильной структурой молекулы, имеют контролируемую абсорбцию железа из комплекса [13]. Метаанализ сравнительных исследований [14] подтвердил одинаковую эффективность препаратов железа на основе ГПК и сульфата железа в лечении ЖДА.
В литературе имеется большое количество работ, в которых сравнивается эффективность и переносимость различных солевых препаратов железа и препаратов железа на основе ГПК. Однако лишь недавно были опубликованы результаты рандомизированных исследований, которые являются наиболее доказательными в медицине. Например, в работе B. Yasa и соавт. [15] проведено сравнение эффективности лечения ЖДА и переносимости препаратов железа. Больные были рандомизированы на 2 группы: 1-я группа (52 пациента) получала лечение препаратом железа на основе ГПК в дозе 5 мг/кг в сутки в 1 прием, 2-я группа (51 больной) — сульфат железа в дозе 5 мг/кг в сутки в 2 приема. Эффективность лечения оценивали по приросту концентрации гемоглобина в двух точках — к концу 1-го и к концу 4-го месяцев лечения. Прирост концентрации гемоглобина у пациентов, которые получали препарат железа на основе ГПК, к концу 1-го и 4-го месяца в среднем составил 12 ± 9 и 23 ± 13 г/л соответственно (в обоих случаях р = 0,001 по сравнению с исходной концентрацией гемоглобина), а у пациентов, которые получали сульфат железа, — 18 ± 17 и 30 ± 23 г/л соответственно (в обоих случаях р = 0,001 по сравнению с исходной концентрацией гемоглобина). Статистически значимых различий между группами не получено. Переносимость препаратов оценивали с помощью регистрации нежелательных явлений (боли в животе, тошнота, запоры или сочетание этих симптомов). Нежелательные явления были зарегистрированы у 26,8% пациентов, которые получали препарат железа на основе ГПК, и у 50,8% пациентов, которые получали сульфат железа (р = 0,012).
Таким образом, препараты железа на основе ГПК сопоставимы по эффективности с солевыми препаратами железа, но при их использовании значительно реже возникают нежелательные явления, что обосновывает все возрастающий интерес врачей к препаратам этой группы.
Литература
* ФНКЦ ДГОИ им. Дмитрия Рогачева МЗ РФ,
** ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Эффективность и переносимость препаратов железа. Что важнее? Существует ли оптимальное решение?
Опубликовано в журнале:
Поликлиника 2/2014
Н.И. Стуклов, д.м.н., профессор кафедры госпитальной терапии РУДН, руководитель курса гематологии и клинической базы кафедры
М.Ю. Кунина, врач гематолог ООО Клиники «Будь здоров»
Е.Н. Семенова, учебный мастер кафедры госпитальной терапии РУДН Эффективность терапии железодефицитной анемии определяется не только биодоступностью железа из препарата, но также зависит от приверженности к лечению самого больного, на что существенным образом влияет переносимость препарата и стоимость лечения. Эффективность препаратов, содержащих двухвалентное железо доказана в многочисленных исследованиях (степень доказательности 1А) и не вызывает сомнения. Препараты на основе трехвалентного железа лучше переносятся, но не всегда эффективны и требуют более длительных курсов лечения. Благодаря уникальному составу (глюконат железа II + глюконат меди + глюконат марганца), препарат Тотема («Laboratoire Innotech International», Франция) позволяет быстро восстанавливать концентрацию гемоглобина и депо железа и при этом обладает хорошей переносимостью. Более того, Тотема может применяться в более низких дозах, чем сульфат железа без потери эффективности лечения. Медь и марганец входят в активные центры белков, обеспечивающих активный транспорт железа в кишечнике и быструю утилизацию, поступившего в кровь железа, тканями. Они входят в состав основных белков антиоксидантной защиты. Также марганец участвует в синтезе гемоглобина, регулирует поступление железа в митохондрии. Сравнение результатов трех мета-анализов показало, что Тотема обладает лучшей переносимостью (частота побочных эффектов 10,4%), чем сульфат железа II (34,1% и 20,4%; р
Лечение железодефицитной анемии и дефицита железа
Лечение железодефицитной анемии и дефицита железа
О современных представлениях коррекции дефицита железа и основных характеристиках железосодержащих препаратов, принципах их выбора и дозирования при железодефицитных состояниях.
Диета при железодефиците и источники железа в пище
Основным источником железа для человека являются продукты животного происхождения. В природе железо существует в двух химических формах: 2-валентное (гемовое) и 3-валентное (негемовое). Гемовое железо хорошо всасывается в кишечнике. Наиболее богаты гемовым железом мясо, особенно говядина, кровяная колбаса. В птице и рыбе гемового железа гораздо меньше. Печень (свиная и телячья), почки, сердце, ливерная колбаса богаты ферритином и гемосидерином, содержащими негемовое железо (последнее плохо всасывается в желудочно-кишечном тракте). Много негемового железа содержится в некоторых марках красного вина, фруктовых соках, яблоках, гранатах, гречневой крупе, молочных продуктах, яйцах, орехах и шоколаде. Биодоступность такого железа минимальна, и все эти продукты не являются источником железа. Вегетарианство является мощным фактором риска железодефицитной анемии (ЖДА) в любом возрасте. При этом в рацион должны входить зелень, овощи, фрукты, т. к. усвоение железа улучшается при наличии в пище витамина С. Всасывание железа ухудшают танин (содержащийся в чае и кофе), фитин (содержащийся в рисе, соевой муке), молоко и творог из-за высокого содержания кальция. Поскольку усвоение железа из пищи ограничено, медикаментозная терапия анемии является основной.
Всемирной организацией здравоохранения (ВОЗ) в 1993 – 2005 годах проведено глобальное исследование, показавшее, что 24,4% всех жителей земного шара страдает разными формами анемии. Чаще всего анемия встречается у детей дошкольного возраста (47% от общей популяции), беременных женщин (41,8%) и небеременных женщин детородного возраста (30,2%). В структуре анемий: 37% занимает железодефицитная анемия, 27% – анемия при хронических заболеваниях (АХЗ).
Среди женщин фертильного возраста лидирующие позиции занимает железодефицитная анемия (ЖДА). Анемический синдром является самым частым гематологическим синдромом, встречающимся в клинической практике. Анемия – это не диагноз, а только синдром, требующий особого алгоритма дифференциальной диагностики.
Исследование ВОЗ свидетельствуют о том, что ЖДА является третьей по распространенности причиной временной потери трудоспособности у женщин в возрасте 15–44 лет. Наряду с собственно ЖДА существует скрытый дефицит железа, который в Европе и России составляет 30–40%, в отдельных регионах – 50–60%. По данным ВОЗ, дефицит железа определяется у 20–25% всех младенцев, 43% – у детей в возрасте до 4 лет и до 50% – у подростков (девочки). Таким образом, наиболее частыми анемиями как в Беларуси, так и в других странах, являются ЖДА и АХЗ. Анемия является ведущим фактором ухудшения самочувствия пациента, по приблизительным оценкам ею страдают 2,4 млрд населения земного шара.
Основными причинами развития железодефицитной анемии являются: кровопотери (обильные менструальные кровотечения, беременность, роды, желудочно-кишечные, легочные, при заболевании почек); нарушения всасывания железа (резекция желудка и кишечника, недостаточность поджелудочной железы, глютеновая энтеропатия, болезнь Крона); повышенная потребность в железе (быстрый рост, недоношенные, новорожденные дети, подростки, беременность и лактация); недостаточное поступление с пищей (вегетарианская или веганская диета).
Необходимо помнить, что ЖДА – финал выраженного железодефицита, при котором снижается эритропоэз (кроветворение) и, как следствие, уменьшается содержание гемоглобина.
Предлатентный дефицит железа характеризуется снижением запасов микроэлемента без уменьшения расходования железа на эритропоэз. Латентный дефицит железа наблюдается при полном истощении запасов микроэлемента в депо, однако признаков развития анемии нет. Манифестный дефицит железа, или железодефицитная анемия (ЖДА), возникает при снижении гемоглобинового фонда железа и имеет характерные симптомы. Снижение концентрации сывороточного ферритина ниже 12 мкг/л у здоровых детей и 15 мкг/л у взрослых, с поправкой ниже 30 мкг/л у детей и 70 мкг/л у взрослых с инфекционными или воспалительными заболеваниями, означает неизбежное снижение концентрации гемоглобина в последующем.
Основой патогенетической терапии ЖДА является применение препаратов железа внутрь. Лечение препаратами железа должно быть длительным и зависит от исходной тяжести анемии (уровня гемоглобина и дефицита железа).
На амбулаторном этапе лечение осуществляется при уровне гемоглобина >80 г/л и удовлетворительном общем состоянии пациента. Пероральное назначение железосодержащих ЛС в дозе 200-300 мг/сутки в течение 4-6 недель до нормализации уровня гемоглобина, после чего продолжается прием ЛС в дозе 100 мг/сутки в течение 2-3 месяцев до содержания ферритина не менее 40 мкг/л. Необходим поиск причины дефицита железа и устранение причины дефицита железа – это лечение основного заболевания, вызвавшего дефицит железа.
Принципы выбора препарата железа для терапии
В настоящее время пероральные препараты железа разделены на две основные группы: ионные и неионные (последние представлены протеиновым и гидроксиполимальтозным комплексом 3-валентного железа).
Ионные препараты представлены солями 2-валентного железа, в т. ч. сульфатом железа (феррофол, тардиферон, ферроплекс, сорбифер, ферро-фольгамма и др.); хлоридом железа (гемофер); полисахаридными соединениями – глюконат-фумаратными комбинациями (хеферол, ферронал, мегаферрин). Хелаты 2-валентного железа (цитрат, лактат, глюконат, сукцинат) всасываются лучше, чем сульфат железа. В случае непереносимости солевых препаратов 2-валентного железа, являющихся на сегодняшний день наиболее эффективными в лечении анемии и восполнении депо железа, возможно использование неионных препаратов 3-валентного железа в виде гидроксиполимальтозного комплекса (мальтофер, биофер, феррум лек и др.).
При выборе лекарственного препарата и оптимального режима дозирования необходимо помнить, что адекватный прирост показателей гемоглобина при ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг 2-валентного железа. Учитывая, что при развитии ЖДА всасывание железа увеличивается на 25–30% (при нормальных запасах железа в организме – всего 3–7%), назначают от 100 до 300 мг 2-валентного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. Степень абсорбции 2-валентных солей железа в несколько раз выше, чем 3-валентного, поэтому препараты, содержащие 2-валентное железо, дают быстрый эффект и нормализуют уровень гемоглобина в среднем через 1–2 месяцев, а нормализация уровня железа в депо происходит через 3–4 месяца от начала лечения и зависит от степени тяжести анемии и дозы препарата. Требуется более длительное применение препаратов, содержащих железо в 3-валентном состоянии, в случае дефицита меди в организме они будут неэффективны. Нормализация уровня гемоглобина при лечении препаратом 3-валентного железа наступит только через 2–4 месяца, а восполнение дефицита железа в депо – через 5–7 месяцев от начала терапии. Степень абсорбции отражается и на частоте развития побочных эффектов. Уменьшить нежелательное влияние твердых форм препаратов железа (таблетированных, капсулированных) на слизистую оболочку ЖКТ можно, принимая их во время еды, но при этом уменьшается всасывание железа.
При приеме препаратов в достаточной дозе на 7–10-й день от начала лечения наблюдается повышение количества ретикулоцитов. Нормализация уровня гемоглобина отмечается через 3–4 недели от начала лечения, а в ряде случаев затягивается до 6–8 недель. Общая длительность лечения зависит от исходной тяжести анемии. Стандартные сроки проведения ферротерапии ЖДА: при легкой степени тяжести – 4-6 недель, при средней степени – 8–12 недель, при тяжелой – 16 недель и более. На фоне применения ферропрепаратов внутрь наиболее часто возникают тошнота, рвота, анорексия, запоры (т. к. железо связывает сероводород, являющийся физиологическим стимулятором моторики), реже – поносы, металлический привкус во рту, окрашивание слизистых оболочек и зубов в черный цвет, аллергические реакции, головная боль. Эти побочные эффекты приводят к частым отказам пациентов от лечения.
Биодоступность двухвалентных солей железа в несколько раз выше, чем трехвалентных, так как они свободно диффундируют через каналы ДМТ1-белков и ферропортин. Фармакологический эффект препаратов быстрый, и нормализация уровня гемоглобина в среднем происходит через 2 недели ‒ 2 месяца, а восполнение депо железа происходит уже через 3‒4 месяца от начала лечения, в зависимости от тяжести анемии и дозировки препарата. В связи с чем ВОЗ рекомендует препараты двухвалентного железа в качестве стартовой терапии железодефицитной анемии. Всасывание ионов из препаратов трехвалентного железа более медленное, так как необходима активная (энергозависимая) трансформация с участием феррооксидаз. Поэтому такие препараты требуют более длительного применения, а в случае дефицита меди в организме будут неэффективны вообще.
Лекарственный препарат Феррофол производства УП «Минскинтеркапс» содержит в одной капсуле 50 мг сульфата железа (II) и 500 мкг фолиевой кислоты. Применяя Феррофол в среднесуточной дозировке по 1 капсуле 2-3 раза в день за 1 час до еды (100-150 мг в сутки), достигается цель лечения железодефицитной анемии – введение железа в количестве, необходимом для нормализации уровня гемоглобина, соответствует рекомендации ВОЗ об оптимальной лечебной дозе.
Лекарственный препарат Феррофол отвечает основным требованиям к проведению лечения препаратами железа:
Преимущества препарата Феррофол:
выпускается в форме капсул пролонгированного действия, активные ингредиенты содержатся в пеллетах (микрогранулах), которые обеспечивают их всасывание в верхнем отделе тонкой кишки, в связи с чем отсутствует местное раздражающее действие на слизистую оболочку желудка, что обеспечивает хорошую желудочно-кишечную переносимость. Использование пеллет в капсулах Феррофол позволяет изолировать друг от друга активные вещества – фолиевую кислоту и железо в одной готовой форме. Фолиевая кислота повышает синтез ДНК в кроветворных клетках, что положительно влияет на скорость синтеза гемоглобина, а значит, более быстрое купирование анемии.
Лекарственный препарат Феррофол показан для профилактики и латентного дефицита железа и железодефицитной анемии, особенно во время беременности.
Профилактика железодефицитной анемии и латентного дефицита железа показана пациентам группы риска, к которым относятся:
Феррофол – комбинированный лекарственный препарат, восполняющий дефицит железа и фолиевой кислоты в организме.
Капсулы нужно глотать целиком, запивая стаканом воды. Капсулу нельзя рассасывать, разжевывать и держать во рту.
Прием осуществляют до или во время приема пищи, в зависимости от желудочно-кишечной переносимости.
Имеются медицинские противопоказания и нежелательные реакции.
ПЕРЕД ПРИМЕНЕНИЕМ ЛЕКАРСТВЕННОГО ПРЕПАРАТА ОЗНАКОМЬТЕСЬ С ИНСТРУКЦИЕЙ
_500.gif)

