гормонозависимый кольпит что это
Что такое атрофический кольпит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Лантухова Э. С., гинеколога со стажем в 14 лет.
Определение болезни. Причины заболевания
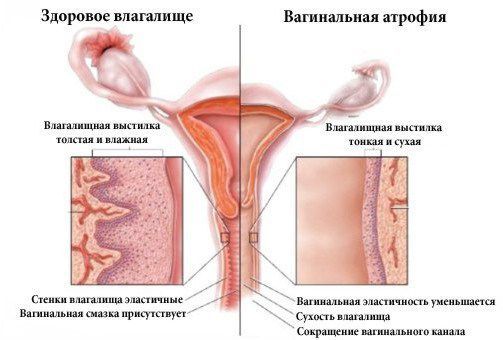
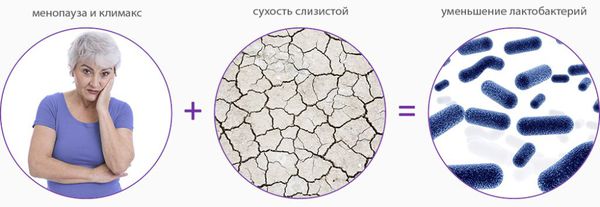
Атрофический кольпит (вагинальная атрофия, генитоуринарный синдром) — это состояние влагалища, которое характеризуется атрофическими изменениями (истончением слизистой, сухостью, нарушением защитных функций тканей), и связано с дефицитом воздействия эстрогенов и других гормонов на слизистые. Чаще всего возникает в менопаузе.
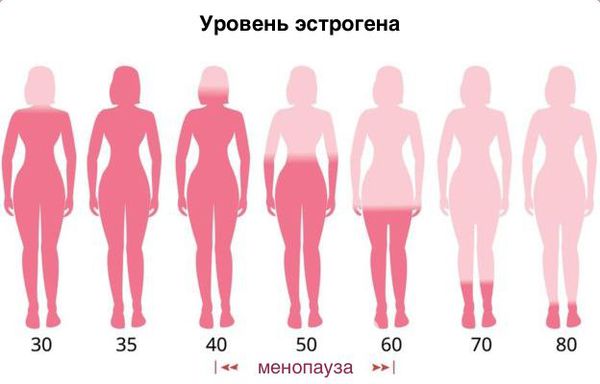
Основная причина развития генитоуринарного синдрома — возрастное снижение эстрогенов в пре- и постменопаузе. Схожие симптомы могут испытывать женщины репродуктивного возраста по следующим причинам:
Симптомы атрофического кольпита
Самый ранний симптом недостаточности эстрогенов — снижение увлажнённости влагалища, замечаемое при половом акте. Другие частые симптомы атрофического кольпита (вагинальной атрофии):
Симптомами атрофического цистоуретрита (эстрогендефицитных атрофических изменений в уретре и мочевом пузыре) являются:
Симптомы атрофического цистоуретрита могут быть изолированными или сочетаться с недержанием мочи при напряжении.
Патогенез атрофического кольпита
В основе развития атрофических изменений при данном заболевании лежит изменение гормонального фона.
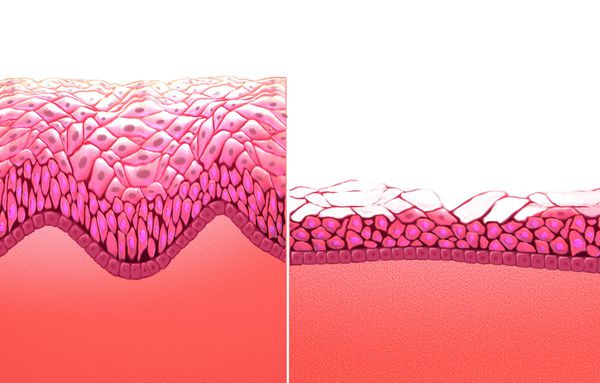
Дефицит эстрогенов блокирует деление эпителиальных клеток стенки влагалища, в результате чего угнетается клеточная пролиферация (увеличение числа клеток и рост ткани) и образование гликогена — питательной среды для лактобактерий. Это приводит к почти полному исчезновению этих бактерий и нарушениям влагалищного микробиома, так как именно кисломолочные бактерии поддерживают оптимальный уровень pH и подавляют рост патогенной и условно-патогенной флоры. В дальнейшем изменение баланса микроорганизмов ведёт к развитию воспалительных процессов.
Поскольку рецепторы к эстрогенам содержатся в эндотелии сосудов (сосудистой стенке) и нервных клетках, при заболевании снижается кровообращение, развивается ишемия тканей, появляются симптомы жжения, зуда и боли.
В связи с единым эмбриональным происхождением мочеполовой системы данные изменения затрагивают не только влагалище, но и уретру, мочевой пузырь, мышцы и связки тазового дна.
Классификация и стадии развития атрофического кольпита
Различают три степени тяжести урогенитальных расстройств:
Осложнения атрофического кольпита
При отсутствии лечения генитоуринального синдрома возможно развитие выраженных изменений. К осложнениям заболевания относятся:
Диагностика атрофического кольпита
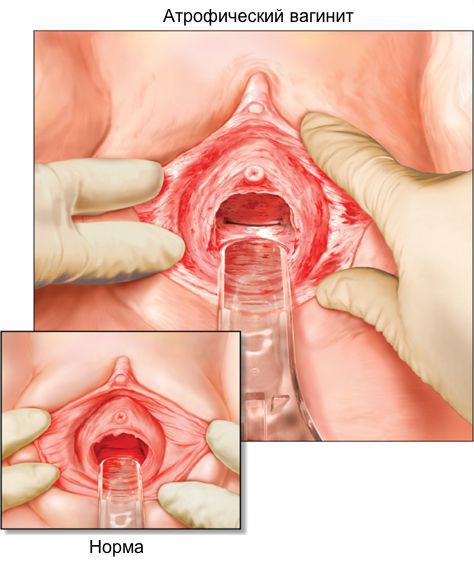
К объективной диагностике атрофического вагинита относятся:
При урологических симптомах проводят общий анализ мочи, посевы мочи, УЗИ почек и мочевого пузыря, КУДИ (комплексное уродинамическое исследование), консультацию уролога. Для исключения кожных заболеваний при необходимости требуется консультация дерматолога.
Лечение атрофического кольпита
При наличии воспаления на фоне атрофии первым этапом проводится санация (устранение возбудителя инфекции), а затем — мероприятия по восстановлению микрофлоры и слизистой.
Лечение симптомов атрофии должно быть дифференцированным и индивидуальным.
Урогенитальные расстройства являются независимым показанием к назначению гормональной терапии. Лучше всего атрофические изменения нивелируют эстрогены для местного применения (эстриол). Препараты эстриола для местного применения имеют минимальную системную абсорбцию (концентрация в плазме не превышает 20 пг/мл), а положительный эффект наступает быстро — через 2-3 недели. При этом у гормональной терапии не выявлено негативного влияния на эндометрий при длительном наблюдении (от 6 до 24 месяцев).
К новым методам лечения умеренной и тяжёлой диспареунии относится одобренный FDA селективный модулятор эстрогеновых рецепторов — оспемифен для приема внутрь, но он имеет ряд противопоказаний и побочных действий.
С целью лечения недержания мочи могут быть использованы инъекции препаратов на основе гиалуроновой кислоты. Востребована и биоревитализация гиалуроной кислотой, в результате которой происходит увлажнение слизистой оболочки, повышение тонуса мышц, усиление либидо. Данные методики имеют временный эффект, так как с течением времени происходит расщепление гиалуроновой кислоты ферментом нашего организма.
Эффективно применение собственной плазмы крови человека, то есть тромбоцитарной аутологичной плазмы — биологического стимулятора процессов регенерации.
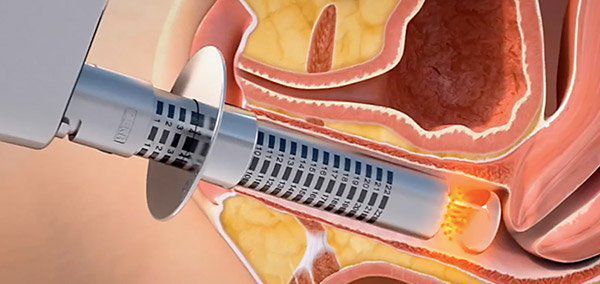
Особой популярностью в настоящее время в профилактике и лечении вагинальной атрофии, недержании мочи и опущения стенок влагалища пользуются лазерные технологии (интимный лазерный фототермолиз).
Методика безопасна, безболезненна, имеет короткий курс реабилитации, проводится амбулаторно. В результате происходит улучшение состояния кожи и тонуса мышц, слизистая оболочка восстанавливает эластичность и натуральную лубрикацию, увеличивается её толщина и мягкость за счёт процессов неоколлагенеза и новой васкуляризации.
Прогноз. Профилактика
При выраженных нарушениях (III-IV степени выпадения половых органов, когда опущение выходит за пределы половой щели, появлении изъязвлений, пролежней, свищей, сращений слизистой, а также при отсутствии желаемого результата от консервативной терапии) проводится хирургическое лечение, однако оно в некоторых случаях может быть не полностью эффективным, иметь рецидивы и осложнения. Для улучшения прогноза на этапах подготовки к оперативным вмешательствам и после операции проводится консервативная гормональная терапия.
Профилактика развития генитоуринарного синдрома основывается на систематических осмотрах и своевременном назначении гормональной заместительной терапии после наступления менопаузы.
Атрофический кольпит ( Сенильный кольпит )
Атрофический кольпит – это невоспалительное заболевание, которое характеризуется истончением слизистой оболочки влагалища, его сухостью и развитием диспареунии. Также наблюдается изменение кислотно-основного состояния. Заболевание проявляется чувством стягивания, жжения. Основная причина атрофического кольпита заключается в недостатке эстрогенов, которые необходимы для запасания гликогена и поддержания состава нормальной микрофлоры. Диагностика проводится во время гинекологического осмотра, используется кольпоскопия, цитологическое исследование и рН-метрия. Лечение направлено на восполнение дефицита эстрогенов.
МКБ-10
Общие сведения
Атрофический (сенильный) кольпит или вагинит относится к ранним симптомам приближения менопаузы. Его выявляют у 21% женщин в перименопаузе, при прекращении менструаций жжение и зуд появляются у 73% пациенток. Наиболее выраженные признаки беспокоят через 4-6 лет после искусственной или естественной менопаузы. В 70 лет и старше атрофический кольпит диагностируется почти у всех женщин, может сопровождаться другими урогенитальными расстройствами, связанными с нехваткой женских половых гормонов.
Причины
У женщин состояние слизистой влагалища зависит от функционирования яичников и уровня эстрогенов. Они стимулируют запасание гликогена, который при слущивании эпителия становится питательным субстратом для лакто- и бифидобактерий. Чаще всего атрофический кольпит наблюдается в позднем репродуктивном возрасте, но может развиваться и при других состояниях. Основными причинами являются:
Патогенез
Изменения в урогенитальном тракте относятся к ранним проявлениям менопаузы. Они могут появляться при первых признаках недостатка эстрогенов, которые отмечаются уже в 45 лет. У женщин с синдромом истощения яичников эстрогенная недостаточность наблюдается раньше. Нехватка половых гормонов приводит к снижению защитных свойств вагинального секрета, образуемого при участии лактобацилл и бифидобактерий.
При снижении концентрации половых гормонов эпителий теряет способность запасать гликоген, уменьшается количество слоев клеток. У бактерий нет субстрата для размножения, они гибнут, а рН повышается из-за отсутствия молочной кислоты. Слизистая истончается, становится сухой и ранимой. Отсутствие факторов защиты способствует размножению условно-патогенной микрофлоры или развитию бактериального вагиноза.
Наблюдаются изменения кровотока в сосудах влагалища. Ткани страдают от гипоксии, что усиливает высвобождение эндотелиального фактора роста, стимулирующего образование микрокапилляров в эпителиальной оболочке. Эпителий легко повреждается, кровоточит при манипуляциях. Длительно существующее состояние гипоксии может стать причиной изъязвлений.
Классификация
Специальная классификация атрофического кольпита не разработана. Механизмы, которые запускают истончение эпителия и появление характерных симптомов, а также методы лечения аналогичны во всех случаях патологии вне зависимости от ее причины. В Международной классификации болезней 10 пересмотра выделяют два варианта заболевания:
Симптомы атрофического кольпита
Симптомы заболевания возникают постепенно. Сначала начинает беспокоить ощущение дискомфорта в области половых губ, преддверия влагалища. Позже оно переходит в чувство сухости и стянутости кожи. Иногда выраженные атрофические процессы на малых половых губах приводят к жгучей раздражающей боли. Одновременно на вульварном кольце появляются склеротические изменения.
Боль при интимных отношениях связана и со склерозом вульварного кольца, а также постепенной констрикцией влагалища, которое теряет складчатость, становится менее растяжимым. Может изменяться чувствительность. При устойчивом зуде появляется ложное чувство, напоминающее сексуальное возбуждение, во время активных фрикций оно угасает и сменяется болью.
Присоединение инфекционного процесса сопровождается характерными выделениями. Бактериальный вагиноз ведет к появлению запаха тухлой рыбы, который усиливается во время секса или использования мыла. Выделения обильные, белые с сероватым оттенком. При неспецифическом воспалении зуд усиливается, могут присоединяться дизурические расстройства в виде учащенных позывов, дискомфорта при мочеиспускании. Выделения становятся желтоватыми.
Осложнения
Осложнения атрофического кольпита развиваются при игнорировании симптомов и несвоевременном лечении. Далеко зашедшие процессы атрофии приводят к возникновению крауроза вульвы, для которого характерен нестерпимый зуд, резистентный к гормональным средствам. Осложнения атрофических процессов могут быть связаны с присоединением инфекции. Если она распространится восходящим путем, есть вероятность развития цервицита, эндометрита, аднексита.
Недостаток эстрогенов сказывается на всем урогенитальном тракте. После появления сухости и зуда атрофические процессы распространяются на мышечные и соединительные ткани. У женщин развивается опущение влагалища, которое приводит к недержанию мочи, ее подтеканию во время смеха, кашля. Позывы к мочеиспусканию, а иногда и к дефекации становятся императивными.
Диагностика
Женщинам необходимо ежегодно проходить осмотр у врача акушера-гинеколога, чтобы заметить патологические изменения на ранней стадии. Если по результатам диагностики выявляются признаки дисплазии тяжелой степени, назначается консультация онколога. Обследование направлено на оценку степени атрофических изменений при невоспалительном кольпите. Используются:
Лечение атрофического кольпита
При лечении заболевания предпочтение отдается местным средствам, действие которых ограничивается урогенитальным трактом. Женщина проходит лечение в домашних условиях, но периодически посещает врача-гинеколога в женской консультации. Госпитализация в отделение гинекологии не требуется. Консервативная терапия проводится следующими препаратами:
Прогноз и профилактика
При своевременном обращении к врачу и отсутствии противопоказаний к гормональному лечению можно уменьшить неприятные симптомы, облегчить состояние при помощи местных препаратов. Профилактика атрофического кольпита заключается в здоровом образе жизни, предотвращении заражения половыми инфекциями, правильном использовании оральных контрацептивов. Остановить наступление менопаузы невозможно, но при рациональном поведении в этот период, профилактическом посещении врача-гинеколога раз в год можно подготовиться к ее приходу.
Урогенитальные расстройства в постменопаузе и заместительная гормонотерапия
Изменение демографической структуры общества во второй половине XX в. привело к увеличению в популяции доли женщин старшей возрастной группы. С каждым годом возрастает число женщин, вступающих в период менопаузы. Если
Изменение демографической структуры общества во второй половине XX в. привело к увеличению в популяции доли женщин старшей возрастной группы. С каждым годом возрастает число женщин, вступающих в период менопаузы. Если 75 лет принять за 100%, то продолжительность препубертатного периода составляет 16%, репродуктивного — 44%, пременопаузального — 7%, а постменопаузального — 33% (H. Нaney, 1986). То есть более трети своей жизни женщина проводит в состоянии дефицита женских половых гормонов. Менопауза, не являясь собственно заболеванием, приводит к нарушению эндокринного равновесия в организме женщины, вызывая приливы, раздражительность, бессонницу, урогенитальные расстройства, а также повышая риск развития остеопороза и сердечно-сосудистых заболеваний. Все эти данные свидетельствуют о необходимости разработки целого ряда медицинских и социальных мер по защите здоровья, сохранению работоспособности и достойного качества жизни женщин пери- и постменопаузального периода.
В последние годы в симптоматологии климактерических нарушений стала лидировать проблема урогенитальных расстройств, что связано с их выраженным отрицательным влиянием на качество жизни женщины в постменопаузе. Частота развития возрастных урогенитальных расстройств достигает 30%. В перименопаузальном периоде урогенитальные нарушения встречаются у 10% женщин, тогда как в возрастной группе 55—60 лет — у 50%. К 75 годам уже 2/3 женщин испытывают урогенитальный дискомфорт, а после 75 лет трудно встретить женщину, у которой не наблюдалось отдельных симптомов урогенитальных расстройств.
Урогенитальные расстройства в климактерии — это симптомокомплекс вторичных изменений, связанных с развитием атрофических и дистрофических процессов в эстроген-зависимых тканях и структурах нижней трети мочеполового тракта, мочевом пузыре, уретре, влагалище, связочном аппарате малого таза и мышцах тазового дна.
Прогрессирующее увеличение с возрастом частоты развития урогенитальной атрофии связывают с развивающимися на фоне эстрогенного дефицита необратимыми возрастными метаболическими изменениями. Влагалище, уретра, мочевой пузырь и нижняя треть мочеточников имеют единое эмбриональное происхождение и развиваются из урогенитального синуса. Это объясняет наличие рецепторов к эстрогенам, прогестерону и андрогенам в мышцах, слизистой оболочке, сосудистых сплетениях влагалища, мочевого пузыря и уретры, а также в мышцах и связочном аппарате малого таза.
Процессы старения урогенитального тракта развиваются в двух направлениях:
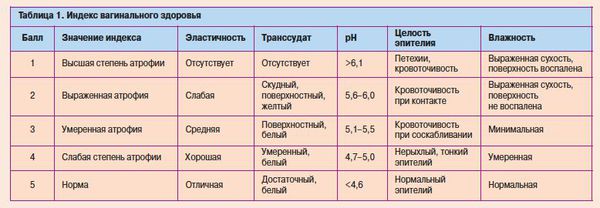
Атрофический вагинит возникает в результате эстрогенного дефицита и характеризуется резким истончением слизистой оболочки влагалища, прекращением пролиферативных процессов во влагалищном эпителии, уменьшением продукции гликогена эпителиальными клетками, снижением или полным исчезновением лактобацилл, повышением влагалищного рН (см. таблицу 1).
Основные клинические проявлениями атрофического вагинита — это сухость и зуд во влагалище, рецидивирующие выделения, диспареуния, контактные кровянистые выделения.
Диагностика атрофического вагинита включает:
К проявлениям атрофического цистоуретрита относятся «сенсорные» или раздражающие симптомы:
Обследование женщин с расстройствами мочеиспускания:
Вычленение симптомов атрофического вагинита и цистоуретрита условно, так как в большинстве случаев они сочетаются. Различные сочетания симптомов атрофического вагинита и цистоуретрита позволили выделить три степени тяжести урогенитальных расстройств (В. Е. Балан, 1997).
К легким урогенитальным расстройствам (16% женщин) относится сочетание симптомов атрофического вагинита и «сенсорных симптомов» атрофического цистоуретрита без нарушения акта мочеиспускания.
К среднетяжелым урогенитальным расстройствам (80% женщин) относится сочетание симптомов атрофического вагинита, цистоуретрита и истинного недержания мочи при напряжении.
К тяжелым урогенитальным расстройствам (4% женщин) относится сочетание симптомов атрофического вагинита, цистоуретрита, истинного недержания мочи при напряжении и неудержание мочи.
Итак, установлено, что эстрогенный дефицит является причиной развития урогенитальных нарушений у женщин в климактерии. Проблема лечения урогенитальных расстройств неоднозначна. Акцент ставится на том, какой вид заместительной гормонотерапии (ЗГТ) считать оптимальным. ЗГТ урогенитальных нарушений может осуществляться препаратами, обладающими как системным, так и местным действием. К системной ЗГТ относятся все препараты, содержащие эстрадиол, эстрадиол валерат и конъюгированные эстрогены.
К местной ЗГТ — препараты, содержащие эстриол. Выбор типа ЗГТ для лечения урогенитальных расстройств является индивидуальным и зависит от возраста пациентки, длительности постменопаузы, ведущих жалоб, необходимости лечения климактерического синдрома либо профилактики поздних метаболических нарушений.
Назначение системной ЗГТ должно соответствовать общепринятым правилам с учетом абсолютных и относительных противопоказаний. При назначении ЗГТ пациенткам с урогенитальными нарушениями преследуется цель восстановления нормального состояния местных гормонозависимых структур нижних отделов мочеполовой системы и стимуляции механизмов биологической тканевой защиты.
При решении вопроса о выборе типа препарата для ЗГТ крайне важно определить:
При интактной матке применяется комбинированная терапия препаратами, содержащими эстрогены и гестагены:
У женщин после гистерэктомии системное воздействие обеспечивает монотерапия натуральными эстрогенами в циклическом или непрерывном режиме (эстрофем, прогинова, климара, дивигель, эстрадерм).
Приоритетная роль в выборе ЗГТ расстройств урогенитального тракта, обусловленных снижением функции гонад, принадлежит эстриол-содержащим препаратам, обладающим избирательной активностью в отношении мочеполовой системы. Специфичность действия эстриола определяется особенностями его метаболизма и сродством с соответствующими рецепторными системами. Местный эффект стероидных гормонов реализуется путем пассивной диффузии их в клетки организма. Задерживаясь лишь в клетках чувствительных тканей, они образуют комплексы с цитозольными рецепторами с последующей транслокацией в ядро клетки. Таким путем реализуется действие на уровне генетических структур клетки. Это и определяет специфичность эффекта, свойственного данной ткани.
Ответ тканей на воздействие эстрогенов определяется концентрацией рецепторов, их структурой и свойствами эстрогенов. Эстриол является конечным метаболитом в обмене эстрогенов. Он выводится из организма в конъюгированной форме с мочой и лишь в незначительном количестве экскретируется с калом, в основном в неконъюгированной форме.
При пероральном введении эстриола его максимальная концентрация в плазме крови достигается через 1-2 ч. Попавший в плазму крови эстриол не связывается с глобулином, связывающим половые стероиды, и довольно быстро элиминируется. Эстриол является наименее активным эстрогеном с кратковременным действием.
Установлено, что ткани, чувствительные к эстриолу, широко представлены в нижних отделах урогенитального тракта. Терапия эстриолом способствует развитию и восстановлению влагалищного эпителия, а также приводит к восстановлению основных элементов соединительной ткани — коллагена и эластина. При этом главным в назначении эстриол-содержащих препаратов является минимальное системное действие. Известно, что для стимуляции развития эндометрия связь его рецепторов с эстрогеном должна быть длительной, не менее 8—10 ч. Эстриол же связывается с чувствительными к нему структурами не более чем на 2—4 ч. Такого непродолжительного действия недостаточно для пролиферативной реакции эндометрия, но достаточно для эффективного воздействия на структуры нижних отделов урогенитального тракта. Таким образом, при однократном введении эстриол связывается с ядерным рецептором на непродолжительное время и не вызывает пролиферацию эндометрия, поэтому при его назначении не требуется добавления прогестагенов.
При урогенитальных расстройствах традиционно отдается предпочтение местному введению эстрогенов и именно эстриола (овестин) в мазях и свечах (см. таблицу 2).
В любой форме эстриол-содержащие препараты принимаются один раз в сутки. Не рекомендуется сочетание системных и местных форм препарата.
Выбор терапии зависит также от степени тяжести урогенитальных расстройств.
При легкой степени тяжести урогенитальных расстройств применяются препараты эстриола (свечи, крем) ежедневно или три раза в неделю, в зависимости от степени выраженности клинических симптомов. При сочетании явлений атрофического вагинита или атрофического цистоуретрита с климактерическим синдромом назначаются препараты для системной ЗГТ.
При средней степени тяжести урогенитальных расстройств проводится сочетанная терапия (системная и местная) не менее шести месяцев для нормализации уродинамических показателей.
При тяжелой степени урогенитальных расстройств в случае имеющихся показаний к системной ЗГТ проводится комбинированная терапия препаратами для системной ЗГТ в сочетании с местным введением препаратов эстриола и одного из препаратов аддитивного воздействия, обладающих избирательным действием на холинергические (парасимпатические) и адренергические (симпатические) или мускариновые рецепторы, расположенные в мышечной стенке мочевого пузыря и различных структурах урогенитального тракта: гладкомышечной мускулатуре уретры и мышцах тазового дна, участвующих в создании уретральной поддержки. Комбинированную терапию необходимо проводить в течение шести месяцев и более, после чего вопрос о типе терапии решается индивидуально в отношении каждой пациентки (см. таблицу 3).
 |
| Таблица 3. Схема лечения урогенитальных расстройств. |
Такая система дифференцированной ЗГТ позволяет повысить качество жизни больных с урогенитальными расстройствами на 60—70%.
Таким образом, представленные данные позволяют говорить о ЗГТ как об основной терапии урогенитальных нарушений в постменопаузе.
В связи с прогрессирующим характером урогенитальных расстройств преимущество отдается профилактическому назначению ЗГТ и ее долговременному применению. ЗГТ урогенитальных расстройств должна назначаться длительно, практически пожизненно, и в этой ситуации на помощь приходит именно местная терапия эстриолом.
На сегодняшний день современная медицина располагает достаточно широким выбором хороших препаратов для ЗГТ и опытом их применения, свидетельствующим о том, что преимущества назначения ЗГТ заметно преобладают над риском развития побочных эффектов. Все это дает основание рекомендовать широкое применение ЗГТ для профилактики и лечения урогенитальных нарушений в пери- и постменопаузе с целью улучшения качества жизни и сохранения работоспособности женщин, вступающих в этот «осенний» период.
А. Л. Тихомиров, доктор медицинских наук, профессор
Ч. Г. Олейник, кандидат медицинских наук
МГМСУ, Москва