группа триазолов это что
Триазолы
Содержание:
Подробнее при переходе по ссылке
«>фунгицидов, ингибиторов синтеза стеринов. Вещества различаются степенью активности, спектром воздействия на возбудителей болезней, нормой расхода, степенью риска для экосистем, населения и работающего персонала, окупаемостью затрат на их использование.
История
Подробнее при переходе по ссылке
«>фунгицидов из группы триазолов, применявшихся в России с 1970-х годов, является триадимефон.
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
«>фунгицид из данной группы – начал продаваться в 1970-х годах, порядка сорока различных веществ, производных триазола, были коммерциализированы агрохимическими компаниями. Наиболее популярными стали дифеноконазол, тебуконазол и эпоксиконазол.
Активное изучение группы триазолов привело к тому, что многие вещества стали ведущими в системах защиты растений агрокомпаний. Тебуконазол (Байер) и дифеноконазол (Сингента) попали в перечень десяти наиболее продаваемых препаратов – их продажи в 2008 году составили 354 и 210 млн. долларов соответственно. Эпоксиконазол (БАСФ) – один из наиболее важных продуктов, составляющих ассортимент компании.
Физико-химические свойства
Все азолы являются гидролитически и термически стабильными веществами, имеющими слабые основные свойства. Малорастворимые в воде, они хорошо растворяются в органических растворителях. Имеют невысокое давление паров.
Действие на вредные организмы
Подробнее при переходе по ссылке
«>фунгициды) или для профилактических обработок. Некоторые вещества способны ингибировать спорообразование, ослабляя, таким образом, распространение болезни. Но, если фитопатогены уже образуют споры на зараженных растениях, данные Фунгицид – вещество химического или биологического происхождения, предназначенное для борьбы с заболеваниями растений.
Подробнее при переходе по ссылке
Триазолы
действующие вещества
Механизм действия пестицидов – совокупность и последовательность биохимических, физиологических и других процессов, протекающих на молекулярном, клеточном и субклеточном уровнях и приводящих к нарушению нормальной жизнедеятельности вредного организма и его гибели.
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Для формирования проростковой гифы споры содержат достаточное количество стеролов, поэтому на прорастающие споры грибов триазолы фунгицидного действия не оказывают. Если отдельные споры содержат достаточное количество стерола даже для образования инфекционных структур, триазолы не способны противодействовать проникновению инфекции в ткани растения.
Различные вещества из производных триазола воздействуют на разные этапы биосинтеза стеролов. Вследствие этого, спектр активности веществ данного химического класса отличается. Специфичной активностью против ржавчинных грибов обладает ципроконазол.
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
«>фунгицид против базидиальных и сумчатых грибов. Вызывая ингибирование биосинтеза эргостерина, он тем самым нарушет образование клеточной оболочки и развитие гиф мицелия. Обладает также фумигантным действием, особенно в отношении мучнисторосяных грибов.
Подробнее при переходе по ссылке
«>метаболизм, и этим тебуконазол отличается от других триазолов. Препараты на основе данного действующего вещества замедляют темпы развития приобретенной устойчивости патогенов к производным триазола.
Тетраконазол – наиболее эффективный из всех триазолов в отношении мучнистой росы зерновых и тыквенных культур, парши яблони, сетчатой пятнистости ячменя и других болезней. Подавляет биосинтез стерина. Действует также в виде паров (против мучнистой росы огурца и бурой ржавчины пшеницы).
Пропиконазол более фунгициден для вегетативных органов грибов, чем для генеративных, но угнетает спорообразование. Увеличивает интенсивность фотосинтеза в флаговых листьях озимой пшеницы. Отмечено некоторое действие в газовой фазе.
Устойчивые виды
Резистентность (от латинского resistento-сопротивляемость) – устойчивость различных организмов к химическим и биологическим препаратам.
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Инсектицидные свойства
Применение
Баковые смеси
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
Фитотоксичность – способность пестицидов или друхих веществ оказывать токсическое (отравляющее) воздействие на растения.
Подробнее при переходе по ссылке
Подробнее при переходе по ссылке
«>обработке семян зерновых средства задерживают удаление первичного листа и нарушают его геотропизм. Тебуконазол также обладает росторегулирующим влиянием, которое при неблагоприятных условиях (переувлажнение почвы, недостаток влаги, низкая полевая всхожесть семян и энергия прорастания и др.) может перейти в ретардантное. Такие же свойства присущи тритиконазолу, в меньшей степени – другим азолам.
Триазолы
Содержание
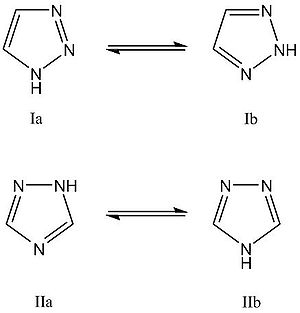
Изомерия
Свойства
Свойства некоторых триазолов:
| Соединение | Тпл, о С | Ткип, о С (при давлении, мм.рт.ст.) | pKb (основания) | pKa (кислоты) |
|---|---|---|---|---|
| 1,2,3-триазол | 23 | 203 (739) | 1,17 | 9,4 |
| 1-метил-1,2,3-триазол | 15-16 | 228 (752) | 1,25 | |
| 1-фенил-1,2,3-триазол | 56 | 172-174 (18,5) | ||
| 1-бензил-1,2,3-триазол | 61 | 180-183 (16) | ||
| 1,2,4-триазол | 120-121 | 250 (760) | 2,2 | 10 |
| 4-метил-1,2,4-триазол | 90 | 3,4 | ||
| 1-фенил-1,2,4-триазол | 47 | 266 (760) | ||
| 3-фенил-1,2,4-триазол | 47 | 119,5-120 | ||
| 4-фенил-1,2,4-триазол | 122 |
Триазолы и их алкил- или арилпроизводные представляют собой бесцветные кристаллы или высококипящие жидкости. Хорошо растворимы в большинстве органических растворителей; незамещённые триазолы растворимы в воде. Проявляют кислотные и слабые основные свойства.
Триазолы относятся к 6π-электронным ароматическим системам. Вступают в реакции электрофильного замещения по атомам углерода или азота. Наиболее характерны реакции алкилирования и ацилирования. 1,2,3-триазол и его 1-замещенные гомологи алкилируются акилгалогенидами, диметилсульфатом, диазометаном, вступают в реакцию Манниха.
В щелочной среде 1,2,4-триазолы алкилируются до 1-алкилпроизводных и с дальнейшим образованием четвертичных солей по атому N-4.
В кислой среде электрофильное замещение триазолов не происходит, так как они в кислой среде превращаются в неактивные триазолиевые катионы.
Устойчивы к нагреванию, действию кислот и оснований, некоторых окислителей (KMnO4, H2O2) и восстановителей (Zn в CH3COOH, Na в NH3, LiAlH4).
Получение
1,2,3-Триазолы получают взаимодействием азидов с ацетиленами, ацетиленидами металлов или реактивами Гриньяра; с соединениями, содержащими активированные метиленовые группы, а также реакцией диазаалканов с активированными нитрилами (дицианом, галогенцианидами, эфирами циановой кислоты).
1,2,4-Триазолы синтезируют из производных гидразина методами конденсации, а также из других гетероциклов.
Применение
Производные триазолов применяются как биологически активные вещества различного действия, обладают противобактериальной, нейролептической, гипотензивной и спазмолитической активностью, стимулируют сердечную деятельность. Используются как лиганды в металлорганических комплексах, как оптические отбеливатели, полупродукты для получения пластификаторов, ингибиторы коррозии, гербициды, катализаторы.
См. также
Литература
Полезное
Смотреть что такое «Триазолы» в других словарях:
Триазолы — см. Пирроазолы … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ТРИАЗОЛЫ — мол. М. 69,6. Различают 1,2,3 Т. (озотриазол), или вицинальный (ф ла I), и 1,2,4 Т. (пирродиазол), или симметричный (II). Незамещенные и С замещенные Т. могут существовать в двух таутомерных формах: для 1,2,3 Т. 1H и 2H формы (Iaи Iбсоотв.), для… … Химическая энциклопедия
ПОЛИТРИАЗОЛЫ — полимеры, содержащие в основной цепи 1,2,3 или 1,2,4 триазольные циклы: Наиб. интерес представляют полифенилен 4 фенил 1,2,4 триазолы, т. к. они наиб. термостойки и их можно перерабатывать из р ров обычными методами. Эти П. аморфные в ва; т.… … Химическая энциклопедия
Тетразотовые кислоты — (хим.) кислоты общей формулы RI CN4H, где RI одноатомный остаток ароматического углеводорода, получены Лоссеном между продуктами восстановления амальгамой натрия диокситетразотовых кислот общей формулы: RI CN4O2H, образующихся (Лоссен) при… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Азид-алкиновое циклоприсоединение — Азид алкиновое циклоприсоединение реакция между азидами и алкинами с образованием 1,2,3 триазолов. Реакция впервые была описана Михаэлем в 1893 г., который обнаружил, что при нагреве эфирного раствора фенилазида и диметилового эфира… … Википедия
Полиазолы — суть органические соединения, имеющие в своем составе группу из 5 атомов, сомкнутых в кольцо; атомное кольцо в П. неоднородно, и в него входят или только атомы азота и углерода, или азота, углерода и серы или кислорода. В органической химии… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Тиоацеталдегид — см. Тиоальдегиды. Т. ацетамид см. Тиоамиды. Т. бензойный, Т. валериановый альдегид см. Тиоальдегиды. Т. диазолы см. Тиополиазолы. Т. основания см. Сера. T. пропионамид см. Тиоамиды. Т. резорцин см. Тиофенолы. Т. соли см. Сульфосоли и Сера. Т.… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ — это углеродные циклические соединения, в которых один или несколько атомов кольцевой системы являются отличными от углерода неметаллами (кислородом, азотом или серой). Как и карбоциклические соединения, гетероциклы можно подразделить на имеющие… … Энциклопедия Кольера
АНТИФИДАНТЫ — (от греч. anti приставка, означающая противодействие, и англ, feed поедать), в ва, предохраняющие растения и материалы от поедания животными. наиб. изучены А. насекомых. Эти А., как и репелленты (отпугивающие в ва), насекомых не убивают. В… … Химическая энциклопедия
Триазолы не оказывают фунгицидного действия на прорастающие споры грибов, поскольку споры содержат достаточное количество стеролов.
Фунгициды на основе производных триазола широко используются на различных растениях: полевых культурах, плодовых деревьях и кустарниках, на овощных культурах и на газонах. Эти фунгициды обладают высокой эффективностью против различных болезней. Особенно высокую эффективность триазолы проявляют против мучнистых рос, ржавчин и разнообразных пятнистостей листьев.
Различные производные триазола могут воздействовать на разные части биосинтеза стеролов. Благодаря этому, существуют определенные различия в спектре активности различных триазолов.
Важно отметить, что триазолы не оказывают фунгицидного действия на прорастающие споры грибов, поскольку споры содержат достаточное количество стеролов для формирования проростковой гифы. Некоторые споры содержат достаточное количество стерола даже для образования инфекционных структур. В этих случаях триазолы не способны противодействовать проникновению инфекции в ткани растения.
Триазолы могут применяться для профилактических обработок или для обработок на ранних фазах развития болезни. Некоторые производные триазолов способны ингибировать спорообразование и, таким образом, помогают ослабить распространение болезни. Однако, в большинстве случаев, если фитопатогены уже приступили к образованию спор на зараженных растениях, триазольные фунгициды окажутся неэффективными.
В тканях растений триазолы достаточно подвижны. Действующие вещества быстро проникают в лист и активно распространяются по нему. Исследования показали, что три капли меченного производного триазола, нанесенные на тройчатый лист сои, распространяются по всему листу в течение одного дня. Однако, необходимо знать, что триазолы не всегда способны перемещаться из одного листа в другой и из одной части растения в другую. Они также не способны передвигаться вниз по растению по флоэме. Большинство производных триазола имеют защитный период около 14 дней.
В связи с тем, что все триазолы ингибируют лишь один специфический фермент (С14-диметилазу), у фитопатоганов возможно возникновение устойчивости к ним. Некоторые производные триазола полностью исчезли с рынка пестицидов именно из-за этого явления.
Чтобы избежать возникновения устойчивости патогенов необходимо соблюдать следующие рекомендации:
Обзор рынка
Триазолы заменили бензимидазолы и стали самыми продаваемыми фунгицидами с уникальным механизмом действия и широким спектром действия. С тех пор как первый фунгицид из группы триазолов – триадимефон от компании Байер – начал продаваться в 1970-х годах, около 40 различных производных триазола были коммерциализированы агрохимическими компаниями. Среди них них наиболее популярными действующими веществами стали тебуконазол, эпоксиконазол и дифеноконазол.
Основные действующие вещества из группы триазолов
ИМИДАЗОЛЫ
Данная группа представлена препаратами для местного применения и кетоконазолом, который используется внутрь и местно. Между препаратами для местного применения (клотримазол, миконазол, оксиконазол, эконазол и др.) нет принципиальных различий. Несколько обособленную позицию занимает бифоназол.
КЛОТРИМАЗОЛ
Канестен
Обладает широким спектром противогрибковой активности, но основное значение имеет активность против кандид. Сообщается об активности по отношению к ряду бактерий (стрептококки, стафилококки, бактероиды) и трихомонад, однако действие на эти микроорганизмы в достаточной мере не изучено. Используется местно.
Нежелательные реакции
Может вызывать легкую эритему, жжение, зуд, сыпь.
Показания
Формы выпуска
Крем, 1%; раствор, 1%; вагинальные таблетки по 0,1 г.
Входит в состав комбинированного препарата «Тридерм» (мазь и крем, содержащие клотримазол 1%, гентамицин 0,1% и бетаметазон 0,05%), который применяется при дерматитах, осложненных вторичной инфекцией, и эпидермофитии стоп.
МИКОНАЗОЛ
Препарат для местного применения. По спектру активности близок к клотримазолу.
Формы выпуска и показания
ОКСИКОНАЗОЛ
Мифунгар-крем
Препарат для местного применения. По спектру активности близок к клотримазолу.
Нежелательные реакции
Иногда вызывает эритему, жжение, покалывание, зуд в месте применения.
Показания
Форма выпуска
БИФОНАЗОЛ
Микоспор
Активен в отношении дерматофитов (Epidermophyton spp., Trichophyton spp., Microsporum spp.), дрожжевых и плесневых грибов, возбудителей эритразмы (C.minutissimum) и разноцветного лишая (M.furfur).
Хорошо проникает в инфицированные слои кожи и длительно там сохраняется.
Может вызывать местные кожные реакции (покраснение, шелушение и др.).
Показания
Дозировка
Применяется местно (кроме влагалища!) 1 раз в день, лучше перед сном.
Формы выпуска
Крем, 1%; гель, 1%; раствор, 1%; крем в наборе для лечения онихомикоза (с добавлением мочевины); пудра.
КЕТОКОНАЗОЛ
Низорал, Ороназол
Спектр активности
По широте спектра противогрибковой активности близок к амфотерицину В. В отличие от последнего действует на дерматофиты (Epidermophyton spp., Trichophyton spp., Microsporum spp.) и Pseudoallescheria boydii, но не действует на аспергиллы и мукор.
Фармакокинетика
Нежелательные реакции
Лекарственные взаимодействия
Антациды, холиноблокаторы, Н2-блокаторы и ингибиторы протонного насоса уменьшают всасывание кетоконазола, так как понижают кислотность в желудке. Поэтому кетоконазол необходимо принимать за 2 ч до приёма этих препаратов.
Ингибируя микросомальные ферменты печени (цитохром Р450), кетоконазол тормозит метаболизм циклоспорина, глюкокортикоидов, непрямых антикоагулянтов, повышая их концентрацию в крови.
Нельзя сочетать кетоконазол с цизапридом, терфенадином и астемизолом ввиду риска развития смертельных аритмий.
Показания
Предупреждения
Перед назначением кетоконазола необходимо сопоставить его потенциальные преимущества с риском поражения печени. Рекомендуется регулярно контролировать функцию печени.
Дозировка
Взрослые
Формы выпуска
Таблетки по 0,2 г; шампунь, 2%.
ТРИАЗОЛЫ
ФЛУКОНАЗОЛ
Дифлюкан
Современный противогрибковый препарат, имеющий меньший спектр активности по сравнению с амфотерицином В и кетоконазолом, но обладающий гораздо лучшей переносимостью. В равной степени эффективен при приеме внутрь и внутривенном введении.
Спектр активности
Резистентность к флуконазолу часто отмечается у C.glabrata и C.krusei.
Фармакокинетика
Практически полностью всасывается в ЖКТ, биодоступность (75%) не зависит от приёма пищи. Хорошо проникает в различные ткани, проходит через ГЭБ. Не метаболизируется в организме, выводится преимущественно через почки. Имеет длительный T1/2 (30 ч), который значительно возрастает при почечной недостаточности.
Нежелательные реакции
Лекарственные взаимодействия
Флуконазол значительно повышает концентрации фенитоина, глипизида и циклоспорина в крови. Отмечается также умеренное повышение концентраций теофиллина и непрямых антикоагулянтов.
Рифампицин на 25% снижает концентрацию флуконазола в крови.
Показания
Дозировка
Взрослые
Формы выпуска
Капсулы по 0,05 г, 0,1 г, 0,15 г и 0,2 г; флаконы с раствором по 0,05 г, 0,1 г и 0,2 г.
ИТРАКОНАЗОЛ
Орунгал
Современный противогрибковый препарат с несколько отличным от флуконазола спектром активности. Принципиальное значение имеет активность итраконазола в отношении к аспергилл.
Спектр активности
Фармакокинетика
Хорошо всасывается в ЖКТ, причем для абсорбции необходим нормальный уровень кислотности в желудке. Биодоступность выше при приеме во время еды (более 80%), чем натощак (55%). Хорошо проникает в различные ткани. Высокие концентрации отмечаются в эпидермисе и ногтевых пластинках, легких, печени, коже, костях, гениталиях. Однако в отличие от флуконазола не проникает через ГЭБ. Метаболизируется в печени, экскретируется преимущественно через ЖКТ. Имеет длительный Т1/2 (30-45 ч), который не изменяется при почечной недостаточности.
Нежелательные реакции
При применении в высоких дозах (более 0,4-0,6 г/сут) возможны:
Лекарственные взаимодействия
Ингибируя микросомальные ферменты печени (цитохром Р450), итраконазол нарушает печеночный метаболизм и тем самым увеличивает концентрацию в крови многих препаратов: непрямых антикоагулянтов, пероральных антидиабетических препаратов, циклоспорина, дигоксина и др. Поэтому нельзя сочетать итраконазол с цизапридом, терфенадином и астемизолом вследствие высокого риска развития тяжелых аритмий.
Антациды, холиноблокаторы, Н2-блокаторы и ингибиторы протонного насоса, снижая кислотность в желудке, ухудшают всасывание итраконазола и примерно в 2 раза снижают его концентрацию в плазме.
Индукторы микросомальных ферментов печени (рифампицин, фенобарбитал и др.) уменьшают концентрацию итраконазола в крови.
Показания
Предупреждение
Итраконазол нельзя применять при церебральных микозах, так как он не проникает через ГЭБ.
Дозировка
Взрослые
Формы выпуска
Капсулы по 0,1 г; раствор для приёма внутрь, 100 мг/10 мл; раствор для инъекций в ампулах, 10 мг/мл.
Адрес этой страницы: http://www.antibiotic.ru/books/mach/mac0302.shtml
Дата последнего изменения: 24.05.2004 18:56
Триазолы
Триазолы – самая большая группа фунгицидов, относится к классу азолов. Препараты могут применяться для обработок растений на ранних фазах развития заболевания или для профилактических обработок. Используются против возбудителей различных заболеваний плодовых и овощных культур.
Содержание:
Триазолы – это наиболее обширная группа фунгицидов, ингибиторов синтеза стеринов. [5] Вещества различаются степенью активности, спектром воздействия на возбудителей болезней, нормой расхода, степенью риска для экосистем, населения и работающего персонала, окупаемостью затрат на их использование. [5]
История
Одним из первых фунгицидов из группы триазолов, применявшихся в России с 1970-х годов, является триадимефон. [5]
Фунгициды группы триазолов заменили устаревающие бензимидазолы и, благодаря уникальному механизму действия, а также широкому спектру активности, стали самыми продаваемыми фунгицидами. С того времени, как триадимефон (разработчик – компания Байер) – первый фунгицид из данной группы – начал продаваться в 1970-х годах, порядка сорока различных веществ, производных триазола, были коммерциализированы агрохимическими компаниями. Наиболее популярными стали дифеноконазол, тебуконазол и эпоксиконазол. [8]
Активное изучение группы триазолов привело к тому, что многие вещества стали ведущими в системах защиты растений агрокомпаний. Тебуконазол (Байер) и дифеноконазол (Сингента) попали в перечень десяти наиболее продаваемых препаратов – их продажи в 2008 году составили 354 и 210 млн. долларов соответственно. Эпоксиконазол (БАСФ) – один из наиболее важных продуктов, составляющих ассортимент компании. [8]
Триадимефон
Трехмерная модель молекулы.
Физико-химические свойства
Все азолы являются гидролитически и термически стабильными веществами, имеющими слабые основные свойства. Малорастворимые в воде, они хорошо растворяются в органических растворителях. Имеют невысокое давление паров. [5]
Действие на вредные организмы
Триазолы могут использоваться для обработок растений на ранних фазах развития заболевания (как лечебные фунгициды) или для профилактических обработок. Некоторые вещества способны ингибировать спорообразование, ослабляя, таким образом, распространение болезни. Но, если фитопатогены уже образуют споры на зараженных растениях, данные фунгициды неэффективны. [8]
Механизм действия
Для формирования проростковой гифы споры содержат достаточное количество стеролов, поэтому на прорастающие споры грибов триазолы фунгицидного действия не оказывают. Если отдельные споры содержат достаточное количество стерола даже для образования инфекционных структур, триазолы не способны противодействовать проникновению инфекции в ткани растения. [8]
Различные вещества из производных триазола воздействуют на разные этапы биосинтеза стеролов. Вследствие этого, спектр активности веществ данного химического класса отличается. [8] Специфичной активностью против ржавчинных грибов обладает ципроконазол. [5]
Флутриафол – системный фунгицид против базидиальных и сумчатых грибов. Вызывая ингибирование биосинтеза эргостерина, он тем самым нарушет образование клеточной оболочки и развитие гиф мицелия. Обладает также фумигантным действием, особенно в отношении мучнисторосяных грибов. [3]
Тебуконазол подавляет биосинтез эргостерина в мембранах клеток фитопатогенов, ингибируя деметилирование в положение С-14. Образующиеся Д5-стерины также воздействуют на метаболизм, и этим тебуконазол отличается от других триазолов. [4] Препараты на основе данного действующего вещества замедляют темпы развития приобретенной устойчивости патогенов к производным триазола. [1]
Тетраконазол – наиболее эффективный из всех триазолов в отношении мучнистой росы зерновых и тыквенных культур, парши яблони, сетчатой пятнистости ячменя и других болезней. Подавляет биосинтез стерина. Действует также в виде паров (против мучнистой росы огурца и бурой ржавчины пшеницы). [4]
Пропиконазол более фунгициден для вегетативных органов грибов, чем для генеративных, но угнетает спорообразование. Увеличивает интенсивность фотосинтеза в флаговых листьях озимой пшеницы. Отмечено некоторое действие в газовой фазе. [4]