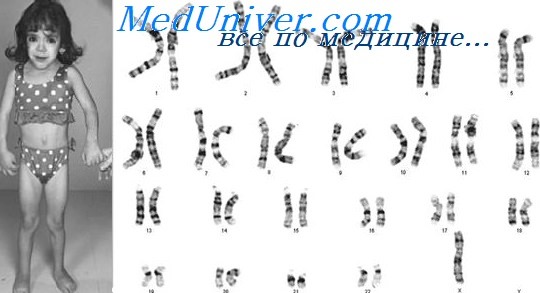
кариотип 46xx что значит
Инверсия пола 46 XX
OMIM 400045
Наша команда профессионалов ответит на ваши вопросы
46,ХХ инверсия пола характеризуется наличием мужского фенотипа (с полной или неполной маскулинизацией), наличием тестикулярной ткани при отсутствии в кариотипе Y-хромосомы. При этом данное нарушение формирования пола может быть обусловлено либо наличием синдрома «46,ХХ-мужчина» либо овотестикулярной формой нарушения формирования пола (истинный гермафродитизм). 46,ХХ инверсия пола может быть связана с наличием фрагмента Y-хромосомы и/или скрытого мозаицизма по Y-хромосоме (Y-позитивная форма) либо с аутосомными или Х-сцепленными мутациями (Y-негативная форма).
46,ХХ инверсия пола тип 1 (OMIM 400045)
В большинстве случаев ХХ-инверсия пола является результатом транслокации небольшого фрагмента короткого плеча Y-хромосомы, несущего ген SRY (OMIM 480000; Yp11.3), на Х-хромосому или аутосому. Нарушение формирования пола является врожденным состоянием, при котором наблюдается полное или частичное аномальное развитие и строение половых желез, внешних половых признаков, обусловленное аномалиями строения половых хромосом. У пациентов с истинным гермафродитизмом гистологически могут быть обнаружены как зрелые ткани яичников с фолликулами, так и яичек с семенными канальцами.
Ключевую роль в детерминации мужского пола и в дифференцировке яичек связана с геном SRY (Sex-determining region Y chromosome). Делеции или точковые мутации этого гена приводят к развитию «чистой» формы дисгенезии гонад при кариотипе 46,XY (синдром Свайера), тогда как его присутствие в геноме больных с 46,ХХ инверсией пола (синдром де ля Шапеля или синдром «46,ХХ-мужчина») обуславливает развитие по мужскому типу, а у больных с мозаицизмом по хромосоме Y, в том числе при синдроме Шерешевского-Тернера – с наличием и выраженностью маскулинизации и/или двойственного полового развития.
Ген SRY расположен на коротком плече Y-хромосомы в непосредственной близости к PAR1 региону, области гомологичной конъюгации хромосом Х и Y, происходящей в сперматогенезе. В процессе мейотического обмена между Х- и Y-хромосомами участок Y-хромосомы, содержащий ген SRY, может быть транслоцирован на Х-хромосому, что может привести к образованию сперматозоидов с перестроенными (дериватными) хромосомами: с Y-хромосомой, утратившей ген SRY, и Х-хромосомой, несущей этот ген. При оплодотворении такими гаметами яйцеклетки, соответственно, возможно рождение мужчин с кариотипом 46,ХХ с транслокацией гена SRY и женщин с кариотипом 46,XY, но с делецией гена SRY. Так, 85-90% больных с ХХ инверсией пола имеют в геноме небольшую часть короткого плеча Y-хромосомы, невидимую при стандартном цитогенетическом исследовании. Последовательности Y-хромосомы у таких больных транслоцированы, как правило, на Х-хромосому, реже на одну из аутосом, унаследованных от отца. Транслоцированный участок Y-хромосомы при этом содержит ген SRY. В редких случаях может встречаться скрытый мозаицизм по Y-несущему клону (например, 46,ХY), о чем свидетельствует наличие локусов SRY, AMGL и других Y-специфичных маркеров.
Для идентификации в геноме последовательностей Y-хромосомы, а также выявления делеции гена SRY, используется метод мультиплексной полимеразной цепной реакции (мПЦР), позволяющий исследовать наличия данного гена, а также гена амелогенина (AMG, AMELX), локализованного на коротком плече Х-хромосомы и его гомолога, локализованного на коротком плече Y-хромосомы (AMGL / AMELY). Для анализа наличия точковых мутаций гена SRY – прямое секвенирование его кодирующей последовательности.
С целью анализа количественных аномалий (анеуполидий) и некоторых структурных аномалий половых хромосом, а также гоносомного мозаицизма и химеризма, может быть использован метод количественной флюоресцентной ПЦР.
46,ХХ инверсия пола тип 2 (ОMIM 278850)
Данный тип ХХ-инверсии пола вызван дупликацией регуляторной области гена SOX9. Ген SOX9 располагается на длинном плече хромосомы 17 в локусе q24.3. Кодируемый геном белок является транскрипционным фактором, играющим важную роль в процессе эмбрионального развития. Особенно важен данный белок для развития скелета и репродуктивной системы. Дупликации локуса 17q24 приводит к увеличению числа копий гена SOX9, что у плодов с кариотипом 46,ХХ вызывает дифференцировку гонад по мужскому типу и развитие тестикул в отсутствие гена SRY и других генов Y-хромосомы (SRY-негативная ХХ-инверсия пола). При этом в большинстве случаев дупликаций гена SOX9 не происходит формирования нормальных тестикул, что ведет к овотестикулярной форме нарушения формирования пола (истинный гермафродитизм).
Точковые мутации в гене SOX9 у пациентов с кариотипом 46,ХХ и 46,ХY приводят к развитию кампомелической дисплазии (OMIM 114290) – заболеванию, которое влияет на развитие скелета и репродуктивной системы и часто является угрожающим жизни состоянием в период новорожденности. Пациенты с кариотипом 46,ХХ и точковыми мутациями в гене SOX9 имеют дисгенезию гонад без инверсии пола (фенотипически женщины), а у пациентов с кариотипом 46,XY дисгенезия гонад приводит к XY – инверсии пола или двойственному развитию половых органов.
В Центре Молекулярной Генетики проводится анализ ключевых генов, контролирующих дифференцировку пола: с помощью количественного метода MLPA проводится поиск делеций и дупликаций генов SRY и SOX9.
46,ХХ инверсия пола тип 3 (ОMIM 300833)
Данная форма ХХ-инверсии пола вызвана дупликацией гена SOX3 или делецией его негативно-регуляторной области. Ген SOX3 (sex determining region Y-box 3) является Х-сцепленным гомологом гена SRY, располагается на длинном плече Х-хромосомы в локусе Xq27.1 и подвержен Х-инактивации. Кодируемый им белок является членом семейства SOX (SRY-related HMG-box) – транскрипционных факторов, вовлеченных в контроль дифференцировки различных типов клеток, а также в регуляцию формирования головного мозга в ходе эмбрионального развития, развитие гипоталамо-гипофизарной системы. Он поддерживает недифференцированное состояние у нервных клеток, противодействуя влиянию факторов, стимулирующих их специализацию. Также наличие данного белка необходимо для инициирования формирования пола по мужскому типу. В дифференцирующихся тестикулах белок SOX3 поддерживает дифференцировку и развитие предшественников ‘поддерживающих клеток’ бипотенциальных (индифферентных) гонад в клетки Сертоли, а не в клетки гранулезы овариальной ткани.
Мутации, делеции или дупликации гена SOX3 являются причиной X-сцепленного гипопитуитаризма, некоторых форм аномалии развития нервной трубки (септо-оптической дисплазии), а также X-сцепленной умственной отсталости с изолированным дефицитом гормона роста. Дупликации Xq26-q27, включающие ген SOX3, являются одной из причин SRY-негативной ХХ-инверсии пола (46,ХХ тестикулярной и овотестикулярной форм нарушения формирования пола). Описано несколько случаев ХХ-инверсии пола, вызванных микродупликациями и микроделециями в локусе Xq27.1. При этом спектр фенотипических проявлений (от бесплодия при нормальном мужском фенотипе до аномалий развития пола, микроцефалии с задержкой умственного развития) зависел от локализации и размера перестройки.
Если кариотип не норма
Патология в кариотипе влияет на процесс созревания половых клеток у мужчин и женщин, их качество и количество. Хромосомные перестройки в организме одного из супругов могут быть причиной бесплодия, повторяющихся выкидышей и рождения детей с пороками развития.
Частота обнаружения хромосомных перестроек составляет 1 случай на 100-200 пар. У таких людей повышенный риск гибели эмбриона, часто отмечаются нерезультативные циклы ЭКО. Что же делать, если пришёл результат анализа и оказалось, что кариотип не норма?
Какие патологии могут быть обнаружены в анализе
В ходе проведения анализа на кариотип чаще всего выявляются:
Существует также множество других патологий: синдром Патау – кариотип 47,ХХ, 13 или 47,ХY, 13 (трисомия по 13 аутосоме), Дауна (трисомия по 21 хромосоме), Прадера-Вилли, Клайнфельтера и друге. Но они имеют явные клинические симптомы, поэтому случайное обнаружение у пар с бесплодием или проблемой привычного невынашивания перечисленных патологий маловероятно.
Что делать при выявлении хромосомных перестроек?
Если анализ на кариотип супругов показал патологию у одного из будущих родителей, требуется консультация генетика, чтобы понять, может ли человек быть генетическим родителем ребёнка. При некоторых хромосомных аномалиях зачатие невозможно, так как половые клетки у пациента попросту отсутствуют. В других ситуациях удаётся добиться беременности и рождения здоровых детей.
В любом случае беременеть лучше с использованием вспомогательных репродуктивных технологий. Они помогают снизить риск неудачных исходов беременности, рождения детей с хромосомными аномалиями или пороками развития внутренних органов. Для уменьшения вероятности подобных проблем используется ПГТ (преимплантационное генетическое тестирование).
Зачем делают ЭКО при хромосомных перестройках?
Во-первых, хромосомные перестройки часто становятся причиной бесплодия. Поэтому нередко супруги при всём желании не могут добиться беременности самостоятельно. Во-вторых, ЭКО и ПГТ позволяют снизить риск выкидыша и обеспечивают рождение здорового малыша.
Такой подход позволяет в большинстве случаев добиться наступления беременности, успешно выносить и родить здорового ребёнка.
Использование донорского биоматериала
В некоторых случаях ПГТ не позволяет решить проблему. Иногда половых клеток нет вообще. В иных случаях все они несут дефектный генетический материал, поэтому добиться получения жизнеспособных эмбрионов невозможно. В той ситуации используют донорскую сперму или ооциты.
Если проблемы с хромосомным набором обнаружены у мужчины, для оплодотворения используют искусственную инсеминацию. Сперму донора вводят при помощи тонкого катетера – гибкой трубки, помещенной в матку. Это делают 1 или 2 раза в течение цикла, в наиболее фертильные дни. Если беременности нет, процедуру повторяют в следующем цикле.
При наличии хромосомных перестроек, несовместимых с беременностью, у женщины, показано ЭКО с донорскими ооцитами. Половые клетки оплодотворяются спермой супруга. Затем они переносятся в матку. С высокой вероятностью в результате этой процедуры наступит беременность, которая будет нормально развиваться и закончится родами.
Поэтому не стоит отчаиваться, если кариотип – не норма. Современная медицина имеет в своём арсенале способы помочь паре зачать и родить здорового ребёнка.
Кариотип 46xx что значит
В отличие от пациентов с другими половыми хромосомными анеуплоидиями, девочек с синдромом Тернера часто идентифицируют при рождении или до половой зрелости из-за отчетливых фенотипических признаков. Синдром Тернера значительно более редкий, чем другие анеуплоидии по половым хромосомам. Встречаемость фенотипа синдрома Тернера — приблизительно 1 на 4000 новорожденных девочек, хотя в некоторых исследованиях приведены значительно более высокие цифры.
Наиболее частая хромосомная конституция при синдроме Тернера — 45,Х (иногда неправильно записываемая 45,Х0), без второй половой хромосомы. Тем не менее до 50% случаев имеет другие кариотипы. Около четверти случаев синдрома Тернера — мозаичные кариотипы, в которых только часть клеток содержит 45,Х. Наиболее частые кариотипы и их приближенные относительные частоты следующие:
1) 45,Х: 50%
2) 46,X,i(Xq): 15%
3) Мозаики 45,Х/46, XX: 15%
4) Мозаики 45,X/46,X,i (Xq): около 5%
5) 45,Х, другая аномалия X: около 5%
6) Другие мозаики 45,Х/?: около 5%
Состав хромосом клинически значим. Например, пациентки с i(Xq) подобны женщинам с классическим 45,Х, пациентки с делецией Хр имеют низкий рост и врожденные пороки развития, а с делецией Xq часто имеют только дисфункцию гонад.
Типичные аномалии при синдроме Тернера включают низкий рост, дизгенезию гонад (в результате нарушения их формирования яичники обычно представлены соединительнотканными полосками), характерное необычное лицо, складчатую шею, низкий рост волос на затылке, широкую грудную клетку с широко расположенными сосками и высокую частоту почечных и сердечно-сосудистых аномалий.
При рождении младенцы с этим синдромом часто имеют важный диагностический признак — отек тыльной стороны стоп и кистей.
У многих пациентов обнаруживают коарктацию аорты, женщины с синдромом Тернера имеют повышенный риск сердечно-сосудистых аномалий. Лимфоотек может проявляться во внутриутробном периоде, вызывая кистозную гигрому плода (обнаруживаемую при ультразвуковом исследовании — УЗИ), вызывающую видимые после родов шейные складки.
Синдром Тернера следует заподозрить у любой новорожденной девочки с отеком кистей и стоп или с гипоплазией левых отделов сердца или коарктацией аорты. Возможность этого диагноза нужно также учитывать в подростковом периоде у девушек с первичной или вторичной аменореей, особенно если они низкого роста. Терапия гормоном роста показана для всех девушек с синдромом Тернера и позволяет прибавить от 6 до 12 см роста.
Обычно считают, что интеллект у женщин с синдромом Тернера будет нормальным, хотя приблизительно 10% пациенток имеют значимую задержку развития, требующую специального образования. Даже среди тех, кто имеют нормальный интеллект, тем не менее, часто выявляют недостаточность в пространственном восприятии, двигательной и тонкой моторике.
Как следствие, невербальная оценка IQ значительно ниже вербальной, и большинство пациенток нуждается в педагогической поддержке, особенно по математике. Женщины с синдромом Тернера имеют высокий риск низкой социальной адаптации. Сравнение девушек 45,Х с материнским и отцовским происхождением Х-хромосомы показало значительно худшие социальные навыки при материнской Х-хромосоме. Поскольку эффект родительского происхождения может объясняться импринтингом, такую возможность исследуют для генов Х-хромосомы, которые влияют на фенотип.
Высокая встречаемость кариотипа 45,Х при спонтанных абортах уже упоминалась. Аномалия присутствует предположительно в 1-2% всех зачатий; выживание до срока родов — редкое явление, и более чем 99% таких беременностей спонтанно прерывается. Единственная Х-хромосома примерно в 70% случаев имеет материнское происхождение; другими словами, хромосомная ошибка, ведущая к потере половой хромосомы, обычно происходит у отца.
Основа для необыкновенно высокой частоты утраты Х- или Y-хромосомы неизвестна. Кроме того, неясно, почему кариотип 45,Х, столь часто летальный внутриутробно, очевидно полностью совместим с жизнью после родов. Утраченные гены, ответственные за фенотип синдрома Тернера, должны находиться как в Х-, так и Y-хромосоме. Предполагают, что эти гены входят в число генов, избегающих Х-инактивации, в частности, находящихся на коротком плече, включая псевдоаутосомную область.
Иногда у пациентов с низким ростом, дизгенезией гонад и умственной отсталостью выявляют небольшие кольцевые Х-хромосомы. Поскольку задержка умственного развития нетипична для синдрома Тернера, наличие такой задержки с другими аномалиями у больных с кариотипом 46,Х,r(Х) связывают с тем, что небольшие кольцевые Х-хромосомы утрачивают центр Х-инактивации.
Невозможность инактивировать кольцевую Х-хромосому приводит к избыточной экспрессии генов, в норме подлежащих инактивации. Обнаружение кольцевой Х-хромосомы при пренатальной диагностике может вести к большой неопределенности, в таком случае показано исследование экспрессии гена XIST. Большие кольца, содержащие центр Х-инактивации и экспрессирующие ген XIST, приводят к развитию фенотипа синдрома Тернера; при небольших кольцевых хромосомах без экспрессии гена XIST можно предполагать более серьезный фенотип.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Синдром Шерешевского-Тернера
Синдром Шерешевского-Тернера представляет собой генетическое заболевание, обусловленное отсутствием половой Х-хромосомы или структурными изменениями в ней при нормальном кариотипе, что провоцирует аномалии развития половых желез на ранних этапах развития эмбриона.
Причины развития синдрома
Хромосомные аномалии могут быть обусловлены как генетическим фактором, так и воздействием внешних факторов, таких как ионизирующее излучение или токсические вещества.
Симптомы Синдрома тернера
В ряде случаев какие-либо характерные симптомы, позволяющие заподозрить синдром Шерешевского-Тернера у новорожденного, могут почти полностью отсутствовать. Однако нередко обнаруживаются внешние специфические признаки, к которым можно отнести:
В дальнейшем у пациентов с синдромом Шерешевского-Тернера отмечается задержка в росте, что становится все более очевидным уже к подростковому возрасту и составляет у взрослого порядка 25-ти сантиметров.
В подростковом возрасте у девочек отмечается задержка полового развития, которая характеризуется первичной аменореей, недоразвитием вторичных половых признаков (в частности молочных желез, роста волос на в подмышечных впадинах и на лобке).
Нередко у пациентов с синдромом Шерешевского-Тернера выявляются пороки развития различных органов и систем организма: патологии опорно-двигательного аппарата, сердечно-сосудистой, мочевыделительной системы, органов слуха.
Возможно отставание в интеллектуальном развитии, эмоциональная нестабильность, повышенная тревожность, депрессивные состояния.
Наличие и степень проявления перечисленных симптомов зависят от вариантов заболевания, связанных с характером генетической патологии.
Кариотип при синдроме Шерешевского-Тернера
У пациенток могут определяться различные кариотипы.
Кариотип 45Х
Примерно у половины женщин, страдающих этим синдромом, в результате исследования определяется кариотип 45Х, что свидетельствует об утрате одной хромосомы (в 75% случаев обнаруживается отсутствие хромосомы, наследуемой с отцовской стороны). Влагалище и матка не обнаруживаются, в то же время в малом тазу присутствуют тяжи, аналогичные тем, которые обнаруживаются при синдроме Рокитанского-Кюстнера. У пациенток с таким кариотипом на месте яичников определяются соединительнотканные тяжи. Ткань яичников полностью отсутствует. Обследование выявляет повышенный уровень гонадотропных гормонов, в частности ФСГ (фолликулостимулирующего гормона). Выражены внешние характерные признаки, часто имеют место нарушения со стороны различных систем организма.
Мозаичный кариотип
Помимо этого, может быть определен мозаичный кариотип (наличие клеток с различным кариотипом), такой например, как 45Х/46XY или 45Х/46ХХ. В зависимости от мозаичного варианта и количества измененных клеток варьируются проявления синдрома.
Если у женщины определяется кариотип 45Х/46ХХ, то присутствуют яичники, размер которых уменьшен, и матка без аномалий развития. Для того чтобы оценить репродуктивную функцию пациентки, требуется тщательное обследование в клинике ЭКО, включающее в себя исследование матки, эндометрия и овариального запаса яичников. У пациенток с таким мозаичным вариантом синдрома Шерешевского-Тернера существует некая вероятность развития беременности без применения методов вспомогательной репродукции. При более значительном снижении фертильности могут быть эффективны различные схемы стимуляции овуляции или ЭКО с донорскими ооцитами.
У пациенток с кариотипом 45Х/46XY преодоление бесплодия требует проведения процедуры суррогатного материнства с использованием яйцеклеток донора, т.к. имеет места аплазия матки и влагалища. Яичники удаляют, поскольку наличие Y-хромосомы в кариотипе повышает риск развития злокачественных процессов. При таком мозаичном варианте имеет место вирилизация наружных половых органов (увеличенный клитор, измененный вход во влагалище).
Лечение синдрома Шерешевского-Тернера
Лечение различается в каждом конкретном случае и может предполагать прием анаболических стероидов (для коррекции отставания в росте) и гормональных препаратов (для развития скелета и вторичных половых признаков), а также проведение пластических операций (для удаления крыловидных складок и коррекции косметических дефектов). Помимо этого, проводится терапия выявленных патологий (удвоение почек, дефект межжелудочковой перегородки, остеопороз и т.д.).
Лечение бесплодия при синдроме Шерешевского-Тернера
Схема лечения бесплодия при синдроме Шерешевского-Тернера, как мы уже говорили выше, разрабатывается лечащим врачом гинекологом-репродуктологом в индивидуальном порядке после тщательного обследования.
Кариотипирование
46,XX (кариотип женщины)
46,XY (кариотип мужчины)
Кариотипирование основано на цитогенетическом методе и дает возможность проанализировать хромосомы, их число и структуру. Данный метод позволяет выявить отклонения, которые могут служить как причиной бесплодия или невынашивания беременности, так и свидетельствовать о высоком риске рождения ребенка с тяжелыми врожденными патологиями. Современные методы диагностики позволяют своевременно обнаружить нарушения в хромосомном составе и сделать соответствующие выводы.
Данные методы помогают выявить врожденные дефекты хромосомной цепочки, которые передаются по наследству. Но на изменение структуры хромосомных пар могут повлиять внешние факторы: вирусы, воздействие радиации, неблагоприятная экология. Такие изменения называют аберрациями (обывательское название – «поломки» хромосом). Выявить эти «поломки» можно с помощью расширенного исследования – кариотипирования с аберрациями. Интересно, что небольшие отклонения в структуре хромосом находятся практически у каждого, даже если человек не страдает никакими заболеваниями. Некоторые аберрации влияют на способность к зачатию, другие никак не затрагивают ее.
Проведение кариотипирования, как правило, назначается врачами-генетиками в двух случаях:
Некоторые структурные и количественные нарушения не приводят к явно заметным симптомам, и пациент может даже не догадываться о том, что он является носителем хромосомной аномалии. Как правило, в таких случаях причиной для обращения к врачу является невозможность забеременеть. Поэтому клиника лечения бесплодия зачастую является единственным местом, где может быть выявлено подобное нарушение.
Цитогенетический метод исследования показан в следующих ситуациях: