клексан или фраксипарин что лучше при ковид
Антикоагулянты, действующие на процесс тромбообразования
Ч. 1 Тромбоэмболия легочной артерии и тромбоз глубоких вен — самые распространенные причины смертности и инвалидности при сердечно–сосудистых заболеваниях.
Преферанская Нина Германовна
Доцент кафедры фармакологии образовательного департамента Института фармации и трансляционной медицины Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Единственным доказательным по эффективности методом профилактики тромбозов и тромбоэмболических осложнений является применение антикоагулянтов, изменяющих вязкость крови, способствующих разжижению и повышению текучести крови. Стандартная схема лечения рекомендует начинать использовать антикоагулянты сразу после диагностирования таких заболеваний. Применение антикоагулянтов с момента появления симптомов позволяет предотвратить формирование сгустка крови, его увеличение и закупоривание сосудов. Большинство антикоагулянтов оказывают влияние не на сам кровяной сгусток, а на активность свертывающей системы крови.
Низкомолекулярные гепарины для парентерального введения (селективные ингибиторы фактора Ха)
Низкомолекулярные гепарины состоят из фрагментов гепарина с молекулярной массой от 2000 до 10 000 (в среднем 4000–5000 Да), получают путем фракционирования, гидролиза или деполимеризации обычного нефракционированного гепарина. В отечественной практике используют следующие препараты низкомолекулярных (фракционированных) гепаринов:
Эти препараты неоднородны по своему составу, т.к. содержат разные фракции гепарина и отличаются друг от друга антикоагулянтной активностью, физико-химическими и фармакокинетическими свойствами, но обладают антикоагулянтным и антитромботическим действием. Антикоагулянтный эффект продолжительный и зависит от действующего вещества (от 6 до 18 час.). При выборе антикоагулянта не учитывается возраст больных, тяжесть сопутствующих заболеваний, уровень тромбоза и степень нарушения внутрисердечной гемодинамики.
Низкомолекулярные гепарины блокируют процесс свертывания крови, угнетая в большей степени преимущественно активность фактора Ха, некоторые из них незначительно оказывают влияние на снижение образования протромбиназы (активатора протромбина) и активность фактора IIа. Протромбиназа (prothrombinase complex) — сложный комплекс, состоящий из активированных факторов свертывания Ха и Vа и др. факторов, который формируется на поверхности мембран тромбоцитов в присутствии ионов кальция. В процессе свертывания крови образуется как тканевая, так и кровяная протромбиназа. При применении антикоагулянтов количество образовавшейся протромбиназы очень мало, оно недостаточно для перевода протромбина в тромбин.
Прямые антикоагулянты катализируют образование комплекса с антитромбином III, тромбином и др. активированными факторами. Образуется тройной комплекс с антитромбином III, они необратимо изменяют его конфигурацию и сокращают период его полужизни до 3–6 часов. Связывание с антитромбином III усиливает угнетающее действие на активность фактора Ха, тем самым снижается переход протромбина в тромбин. В результате нейтрализации происходит ингибирование тромбина и формирование тромбов. В отличие от гепарина низкомолекулярные гепарины не связываются с фактором фон Виллебранда, легко инактивируются на поверхности тромбоцитов, что снижает риск геморрагических осложнений, реже развивается тромбоцитопения и остеопороз.
Низкомолекулярные гепарины, так же, как и гепарин, действуют на факторы свертывания через антитромбин III, но отличаются от гепарина следующими свойствами:
Низкомолекулярные гепарины способны блокировать каскад коагуляции на более ранних его этапах, обладают быстрым, выраженным, стабильным и более предсказуемым антикоагулянтным эффектом. Они имеют меньшее сродство к фактору 4 тромбоцитов и поэтому реже, чем стандартный гепарин, вызывают побочные эффекты. Фактор 4 тромбоцитов — антигепариновый, обладает выраженной антигепариновой активностью, устраняет эффект гепарина, его влияние на образование протромбиназы и на увеличение проницаемости сосудов. Антигепариновой активностью обладают также разрушенные и интактные тромбоциты, что связано со способностью тромбоцитов адсорбировать гепарин и его фрагменты и выделять фактор 4 тромбоцитов в плазму крови.
Применяют низкомолекулярные гепарины в основном для профилактики и лечения тромбоза глубоких вен (после хирургического вмешательства), для предупреждения тромбоэмболии легочной артерии. Низкомолекулярные гепарины показаны при нестабильной стенокардии, остром ишемическом инсульте и инфаркте миокарда, для профилактики и терапии тромбозов в акушерско–гинекологической практике, колоректальной и ортопедической хирургии. Их используют для профилактики свертывания крови в системе экстракорпорального кровообращения при длительном проведении гемодиализа или гемофильтрации.
Важно! При применении низкомолекулярных гепаринов могут возникать кровотечения. В первые дни лечения возможна умеренная тромбоцитопения. Низкомолекулярные гепарины в ряде случаев повышают активность печеночных ферментов, могут вызвать аллергические реакции и при длительном применении возникает опасность развития остеопороза. При передозировке протамин сульфат полностью не устраняет эффекты низкомолекулярных гепаринов (≤ 60%). Противопоказанием к их применению является повышенная чувствительность к тому или иному препарату, тяжелая почечная дисфункция, внутричерепное кровоизлияние, беременность, кормление грудью и др.
Формы выпуска низкомолекулярных гепаринов – специальные шприцы-дозаторы разового использования (в блистере по 2 шприца одноразового применения, упак. — 10 шт.).
Доза действующего вещества выражается в международных единицах (МЕ) с активностью подавления фактора Ха в плазме крови и выпускается в виде раствора для инъекций в мл.
Выпускается в растворе для п/к и в/в введения 2,5 м/0,5 мл. 0,5 мл помещают в специальный шприц с иглой вместимостью 1 мл, снабженный автоматической системой безопасности. После подкожной инокуляции Фондапаринукс полностью всасывается из места инъекции, выводится почками в течение 3 суток.
Важно! Применяют с осторожностью при повышенном риске развития кровотечений и гиперчувствительности к препарату. Препарат не рекомендуется смешивать с другими медикаментами.
ПРЯМЫЕ НИЗКОМОЛЕКУЛЯРНЫЕ АНТИКОАГУЛЯНТЫ ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ
К пероральным антикоагулянтам, прямым ингибиторам фактора свертывания крови Ха (активированного фактора Стюарта–Прауэра) относят Апиксабан (Эликвис), Ривароксабан (Ксарелто).
Апиксабан (Эликвис, тб., покр. обол., 2,5 мг и 5 мг) является мощным прямым ингибитором фактора свертывания крови Xa. Он избирательно и обратимо блокирует активный центр фермента, угнетает активность протромбиназы. Для реализации его антитромботического действия не требуется наличия антитромбина III. В результате ингибирования фактора свертывания крови Xa изменяются значения показателей системы свертывания крови: удлиняется активированное тромбопластиновое время и протромбиновое время. Препарат опосредованно влияет на агрегацию тромбоцитов, оказывая антиагрегантный эффект. Апиксабан быстро всасывается из желудочно–кишечного тракта. Абсолютная биодоступность при приеме 10 мг достигает 50%, максимальная концентрация достигается в течение 3 час. после приема внутрь. Период полувыведения (Т½) составляет около 12 час. Прием пищи не оказывает влияния на фармакокинетические показатели. С белками плазмы крови связывается на 87%. Основным путем выведения является кишечник.
Важно! При временном перерыве в терапии Апиксабаном (преднамеренном или случайном) возрастает риск тромбоза. Пациентов следует проинструктировать о необходимости избегать таких перерывов. При временной остановке антикоагуляционного лечения по любым причинам оно должно быть возобновлено как можно скорее.
Не рекомендуется применять у пациентов с заболеванием печени и с повышенным риском кровотечений, во время беременности и в период грудного вскармливания.
Ривароксабан (Ксарелто, тб., покр. обол., 2,5 мг, 10 мг, 15 мг, 20 мг) — высокоселективный дозозависимый прямой ингибитор фактора Ха. Активация фактора X с образованием фактора Ха через внутренний и внешний пути свертывания играет центральную роль в коагуляционном каскаде. Высокая биодоступность (80–100%) наблюдается при приеме в дозе 10 мг, которая не зависит от приема пищи. При приеме натощак 20 мг препарата биодоступность составляла всего F=66%. Максимальная концентрация достигается через 2–4 час. после приема. Большая часть Ривароксабана (92–95%) связывается с белками плазмы крови.
Ривароксабан, 2,5 мг, применяют с целью профилактики смертности вследствие сердечно–сосудистых осложнений, инфаркта миокарда у пациентов после острого коронарного синдрома; 10 мг — в профилактике венозной тромбоэмболии у пациентов, которым проводят обширные ортопедические хирургические вмешательства на нижних конечностях, 15 и 20 мг – для лечения тромбоза глубоких вен и тромбоэмболии легочной артерии, а также с целью профилактики их рецидивов и для профилактики системной тромбоэмболии и инсульта у пациентов с фибрилляцией предсердий неклапанного происхождения.
Важно! Не рекомендуется применять препарат во время беременности, в период грудного вскармливания, детям и подросткам до 18 лет, при наличии болезней почек, при наличии злокачественных новообразований и гиперчувствительности у пациентов.
Клексан или фраксипарин что лучше при ковид
COVID-19 ассоциируется с усилением свертываемости крови. У пациентов с COVID-19 часто повышен уровень Д-димера, высокая концентрация которого является предиктором смерти. Эксперты Международного общества специалистов по тромбозу и гемостазу (ISTH) полагают, что повышение уровня Д-димера в 3-4 раза у пациента с COVID-19 является самостоятельным показанием для госпитализации.
Механизм гиперкоагуляции у пациентов с COVID-19, предположительно, связан с выраженной эндотелиальной дисфункцией и индукцией агрегации тромбоцитов (эндотелий несет на себе рецепторы АПФ2 и является мишенью для вируса SARS-COV-2). Также опубликованы отдельные серии работ, в которых у пациентов с COVID-19 и массивным тромбозом выявлено повышение титров антител к фосфолипидам (https://www.nejm.org/doi/full/10.1056/NEJMc2007575), однако подобные транзиторные изменения могут носить неспецифический характер, поскольку часто выявляются при выраженной воспалительной реакции.
Сейчас назначение антикоагулянтов в профилактической дозе у госпитализированных пациентов с тяжелым течением COVID-19 с целью профилактики венозной тромбоэмболии стало практически повсеместной практикой; показано, что такая терапия снижает смертность у пациентов с COVID-19. Не определены четкие показания к назначению антикоагулянтов, до конца не решен вопрос, какие препараты при этом лучше использовать. Теоретически представляется, что нефракционированный гепарин, обладающий собственным противовоспалительным действием, может иметь определенные преимущества. Более того, есть мнение, что он может снижать связывание вирусных частиц с клетками-мишенями. С другой стороны, использование НФГ требует более частого визита медсестры к пациенту (несколько раз в сутки), что подвергает персонал большему риску. Поэтому во многих клиниках в США для профилактики ВТЭО применяют прямые пероральные антикоагулянты.
У тяжелых пациентов с COVID-19 частота тромботических осложнений остается высокой даже на фоне применения антикоагулянтов в профилактической дозе, поэтому некоторыми экспертами обсуждается возможность назначения антикоагулянтов в полной, лечебной дозе.
Учитывая отсутствие адекватной доказательной базы, тактика в отношении антикоагулянтной терапии у каждого тяжелого пациента с COVID-19 должна быть обсуждена индивидуально с учетом риска тромбозов и кровотечений.
Эксперты рекомендуют контролировать такие показатели, характеризующие свертывание крови, как протромбиновое время, уровень Д-димера, фибриногена, число тромбоцитов.
У пациентов с COVID-19 тяжелого течения достаточно часто развивается тромбоцитопения, однако геморрагические осложнения редки. Лабораторные признаки гипокоагуляции без кровотечения не требуют какой-либо коррекции.
Клексан или фраксипарин что лучше при ковид
Данные о частоте тромботических осложнений после выписки из COVID- стационаров, специфичных для COVID-19 подходах к стратификации риска тромбозов, а также об эффективности и безопасности профилактической антикоагулянтной терапии ограничены. Мнение экспертов на этот счет основывается, прежде всего, на доказательной базе, полученной для пациентов, госпитализированных с иными тяжелыми терапевтическими заболеваниями (включая сепсис и пневмонию). Известно, что у таких пациентов увеличен риск тромбоэмболических осложнений, а профилактическая антикоагулянтная терапия снижает этот риск на треть.
В журнале Blood опубликованы результаты хорошо спланированного крупного многоцентрового проспективного регистра CORE-19. В регистр было включено 4906 пациентов, выписанных после подтвержденного COVID-19, для которых были доступны данные наблюдения за 3 последующих месяца. Средний возраст пациентов составил 61,7 лет, наиболее распространенной сопутствующей патологией была АГ (38.6%), диабет (25.1%), ожирение (18.9%), анамнез онкологического заболевания (13.1%). Профилактическая терапия антикоагулянтами (эноксапарин 40 мг 1 раз в сутки или ривароксабан 10 мг 1 раз в сутки на 30 дней) была назначена у 13,2% пациентов. Терапия назначалась пациентам с предположительно повышенным риском ВТЭО: в случае повышения Д-димера в 2 и более раз от верхней границы референсного интервала или при числе баллов по шкале IMPROVE–DD VTE 4 и более.
За 3 месяца после выписки частота венозных тромбоэмболических осложнений составила 1,55%, артериальных тромботических осложнений – 1,71%, смерти от всех причин – 4,83%, больших кровотечений – 1,73%. Среди перенесших большое кровотечение пациентов лишь 17% получали антикоагулянты после выписки. Согласно данным многофакторного анализа, независимыми предикторами комбинированной конечной точки ВТЭО/артериальные тромбозы/смерть от всех причин оказались такие параметры, как возраст старше 75 лет, анамнез ВТЭО, пребывание в ПИТ, хроническая болезнь почек, атеросклеротическая болезнь периферических артерий, ИБС, число баллов по шкале IMPROVE–DD VTE ≥4. Прием антикоагулянтов снижал риск первичной конечной точки вдвое: ОШ 0.54, 95% ДИ 0.47-0.81).
Мы с нетерпением ожидаем результатов рандомизированных исследований, оценивающих эффективность и безопасность антикоагулянтов после выписки пациентов с COVID-19, которые бы позволили оптимизировать показания к такому лечению.
Giannis D, Allen S, Tsang J, et al. Post-Discharge Thromboembolic Outcomes and Mortality of Hospitalized COVID-19 Patients: The CORE-19 Registry. Blood. 2021 Apr 6:blood.2020010529. doi: 10.1182/blood.2020010529. Epub ahead of print. PMID: 33824972; PMCID: PMC8032474.
Тромбозы при короновирусе
Используйте навигацию по текущей странице

Почему развивается тромбоз в организме людей с коронавирусом?
Последние данные из Европы показывают, что у 30-70% пациентов с коронавирусом, поступающих в отделения интенсивной терапии (ОИТ) выявляются тромбы в глубоких венах ног или в лёгких. Вирус вызывает повреждение стенки сосудов, что запускает процесс тромбообразования, который в норме защищает человека от кровотечения. При ковиде поражение эндотелия приводит к активации системы комплимента, повышение активности иммунной системы, которая атакует собственные клетки организма.
Примерно у каждого четвёртого пациента с коронавирусом, поступившего в отделение интенсивной терапии, развиваются признаки тромбоэмболии лёгочной артерии. Постельный режим сам по себе повышает риск тромбоза нижних конечностей при коронавирусе. Частота тромбоза намного выше, чем мы обычно наблюдаем у пациентов, нуждающихся в госпитализации по другим причинам, отличным от COVID-19.
Экспертные аппараты и Лучшие специалисты
Повышенный риск инсульта
Пациенты, поступающие в больницу с COVID-19, также более подвержены инсульту по сравнению с неинфицированным населением. Вероятность инсульта обычно связана с возрастом, а также с другими факторами риска, такими как высокое кровяное давление, повышенный уровень холестерина или курение. Однако выявлена более высокая частота инсультов у пациентов с COVID-19 у людей в возрасте до 50 лет, без других факторов риска инсульта. У пожилых людей, принимающих лекарства против тромбов снижаются риски сосудистых катастроф при Covid-19.
Низкий уровень кислорода
COVID-19 также связан со сгустками крови в крошечных кровеносных сосудах, которые важны для переноса кислорода в органах. В отчётах о вскрытии обнаружены элементы SARS-CoV-2, вируса, вызывающего COVID-19, в клетках, выстилающих эти небольшие кровеносные сосуды в лёгких, почках и кишечнике.
Это может привести к образованию крошечных сгустков крови в этих мелких кровеносных сосудах, которые нарушают нормальный кровоток и способность крови доставлять кислород к этим органам. Важно отметить, что эти небольшие сгустки крови могут нарушить нормальную функцию лёгких. Это может объяснить, почему у пациентов с тяжёлой формой COVID-19 может быть очень низкий уровень кислорода.
Как лечить и диагностировать тромбы
Когда пациенты поступают в больницу из-за ковида, обычной практикой является введение низких доз антитромботических препаратов для предотвращения образования тромбов. С 2020 года проводятся испытания, чтобы уточнить схемы назначения этих препаратов для максимального эффекта. Диагностика этих тромбов у пациентов с COVID-19 также может быть особенно сложной задачей.
Симптомы обострения лёгочной инфекции, связанной с вирусом, могут быть неотличимы от симптомов тромбоэмболии лёгочной артерии. Симптомы тромбоза глубоких вен после коронавируса неотличимы от классических:
Основные лабораторные признаки тромбоза при коронавирусе включают изменения коагулограммы. Проблема, связанная с COVID-19, заключается в том, что вирус может влиять на лабораторные тесты, которые также могут использоваться для диагностики венозных сгустков крови. У некоторых пациентов это означает, что тест на D-димер возможно не помогает диагностировать тромбы и вовремя начать их лечить.
Каждому пациенту с диагностированной коронавирусной инфекцией необходимо проводить исследование вен нижних конечностей. Обычно для этой цели достаточно ультразвуковой диагностики. Важно понимать, что тромбы могут возникать и в отдалённом периоде после заболевания, поэтому стандартом должна быть ультразвуковая диагностика вен ежемесячно на протяжении полугода после перенесённого ковида. Точный диагноз тромбоза, как осложнения коронавируса может поставить флеболог с помощью УЗИ диагностики. Назначение лекарственных средств против тромбозов позволит предотвратить тяжёлые осложнения.
Почему COVID-19 вызывает свёртывание крови?
Одна из теорий заключается в том, что повышенная скорость образования тромбов при ковиде — это просто отражение общего недомогания и неподвижности. Однако текущие данные показывают, что риск образования тромбов и тромбоэмболии у пациентов с ковидом значительно выше, чем у пациентов, госпитализированных в стационар и в отделения интенсивной терапии.
Предварительные исследования показывают, что обычно используемый гепарин для профилактики тромбоза при коронавирусе, может оказывать противовирусное действие, связываясь с SARS-CoV-2 и подавляя ключевой белок, который нужно использовать вирусу для закрепления на клетках.
Что мы знаем точно, так это то, что осложнения со свёртыванием крови быстро становятся серьёзной угрозой COVID-19. В этой области нам ещё многое предстоит узнать о вирусе, о том, как он влияет на свёртываемость крови, и проверить данные о лучших вариантах профилактики и лечения этих тромбов.
Двойной удар
Сгустки крови, желеобразные сгустки клеток и белков, являются механизмом организма для остановки кровотечения. Тромбы образуются в сосудах в ответ на повреждение внутренней стенки. Некоторые исследователи рассматривают свёртывание крови как ключевую особенность COVID-19.
Воздействие вируса на иммунную систему также может проявляться повышенной свёртываемостью крови. У некоторых людей COVID-19 побуждает иммунные клетки высвобождать поток химических сигналов, усиливающих воспаление, которое связано с коагуляцией и свёртыванием крови различными путями. И вирус, похоже, активирует систему комплемента, защитный механизм, который вызывает свёртывание крови и повышает риск тромбоза при коронавирусе.
Как избежать тромбоза лёгких при коронавирусе?
Похоже, что также важно учитывать стадию течения болезни и место обследования пациента: обычная палата или отделение интенсивной терапии (ОИТ). Оба этих фактора будут влиять на количество антикоагулянтов, которое может получить пациент, что, в свою очередь, может повлиять на последующий тромбоз. Большинство исследований относится к тромбоэмболии лёгочной артерии (ТЭЛА), тогда как есть убедительные доказательства того, что большая часть этого может быть тромбозом лёгочной артерии « in situ». Высокая частота тромбоза лёгких при COVID-19, вероятно, обусловлена слиянием трёх процессов:
интенсивного эндотелиального воспаления, описанного выше, приводящего к тромбозу « in situ », включая тромбоз микрососудов;
уменьшение лёгочного кровотока в ответ на паренхиматозный процесс проявляется низкой скоростью движения крови в сосудах;
классический переход тромбоза глубоких вен в тромбоэмболию лёгочной артерии.
Срочно необходимо проверить результаты текущих испытаний для дальнейшего информирования клинической практики об использовании антикоагулянтов. Сюда входят как пациенты, госпитализированные в отделения интенсивной терапии, так и пациенты из группы риска, находящиеся в палате общего профиля.
Для пациентов, не нуждающихся интенсивной терапии важно решить: каковы поводы для более интенсивной антикоагуляции там, где визуализация недоступна? Можно ли назначать антикоагулянты, используя только анализ на D-димер, и какие пороговые значения следует использовать для точки отсчёта?
Антикоагулянтные препараты
Выбор антикоагулянта, который будет вам назначен, основан на различных факторах: функции почек, массе тела и других принимаемых вами лекарствах. Профилактика тромбозов при ковиде должна проводится с первого дня после установления диагноза и продолжаться не менее месяца после прекращения всех симптомов перенесённого заболевания. Стоит иметь в виду, что некоторые антитромботические препараты получены из животных (свиного происхождения). Существуют таблетированные и инъекционные формы лекарственных препаратов, которые выбирает врач.
Назначаемые схемы
Как долго нужно пить антикоагулянты?
Вам будет предоставлена подробная информация о том, как долго вам следует принимать антикоагулянтные препараты, а также инструкции на этикетке лекарства и больничной документации. Обычно срок антитромботической профилактики не менее месяца после исчезновения всех клинических проявлений. Перед окончанием профилактического курса необходимо провериться на УЗИ и определить необходимость его продолжения. Такой подход позволит предотвратить развитие поздних тромботических осложнений в виде постэмболической пневмонии и массивной ТЭЛА. В информационном поле постоянно появляются случаи преждевременной смерти от тромбоэмболии через несколько месяцев после перенесённой коронавирусной пневмонии. Важно, чтобы вы пили лекарства в течение рекомендованного времени и завершили курс.
Что делать, если вы пропустите приём?
Если вы пропустили приём и вспомнили об этом в тот же день, примите пропущенную дозу, как только вспомните, в этот день. Примите следующую дозу на следующий день и продолжайте принимать один раз в день. Не принимайте двойную дозу, чтобы восполнить пропущенную дозу. При любых подозрениях на тромбоз необходимо провериться флеболога, чтобы определить возможные тромбы.
Клексан или фраксипарин что лучше при ковид
«У большинства умерших от коронавирусной инфекции были тромбы»
Врач клиники «Семейная» Василий Купрейчик с 13 апреля работает в Первой Градской Больнице им. Пирогова терапевтом приемного отделения госпиталя COVID-19. Он рассказал на своей странице в Facebook о результатах изучения историй болезни коронавирусных больных, от какого лечения у них наблюдалась положительная динамика, а какие из нынешних препаратов, принимаемых пациентами с COVID, бесполезны.
Я опущу описание своих суток, фотографию переносицы и прочие популярные атрибуты бойца с Covid, которыми пестрят социальные сети и перейду к гораздо более интересной теме (на мой взгляд), которую я нарыл за последнюю неделю.
Почти всё свободное время в приемном отделении я посвящаю изучению историй болезни. Я смотрю снимки КТ тех пациентов, у которых можно оценить динамику, и иду анализировать их истории. Какие у них показатели крови, какая терапия и т.д., чтобы выявить какую-то взаимосвязь в отсутствии динамики, в наличии положительной или отрицательной динамики.
И, как мне кажется, я наткнулся на один примечательный момент.
Стандартная терапия пациента с коронавирусом в наших реалиях предполагает использование плаквенила (противомалярийный), калетры (противовирусный), антибиотиков (против бактерий), жидкости. У ряда больных к терапии добавляется фраксипарин (антикоагулянт).
Так вот, я обратил внимание, что, если больному “обогащают” эту схему клексаном (еще один антикоагулянт), отмечается явная положительная динамика.
Что я понимаю под положительной динамикой:
– изменения в анализах крови в нужную нам сторону (уходит тромбоцито- и лимфопения, снижаются маркеры воспаления);
– происходят положительные изменения на КТ лёгких – больной либо переводится из ОРИТ обратно в отделение, либо не попадает в ОРИТ.
Для себя, я смог объяснить этот феномен статьёй, согласно которой можно сделать вывод о том, что клексан эффективнее фраксипарина. Но почему антикоагулянты? Ведь вирусная пневмония, цитокиновый шторм и вот это вот всё? Ответ я нашел не сразу.
Случайно, я попадаю на вебинар Джованни Ландони, который является реаниматологом, профессором из Италии в госпитале Сан Рафаэль. Через его ОРИТ в период с начала марта по середину апреля прошло примерно 850 ковид+ больных. Джованни 20 раз акцентировался на важном слайде, который гласит: COVID-19 стоит расценивать как болезнь, которая приводит к повышенному тромбообразованию. Об этом он в соавторстве со своими коллегами написал статью, в которой вообще предлагает переназвать COVID-19 в MicroCLOTS (microvascular COVID-19 lung vessels obstructive thromboinflammatory syndrome).
20 раз сделав акцент на тромбообразовании, Джованни 40 раз сделал акцент на том, что лечение должно проводиться любыми доступными вам антикоагулянтами, лишь бы антикоагулянтами. Примечательно, что калетру (тот который противовирусный) с 19 марта они не используют вообще, ни у кого. Плаквенил (тот который малярийный) продолжают использовать, однако связи с положительной динамикой они, как я понял, не видят. Антибиотики, если не выявлен возбудитель и не доказано бактериальное поражение, не используют. То есть, по сути, лечат антикоагулянтами.
Тогда я полез искать информацию о том, пишет ли ещё кто-то о антикоагулянтах и коронавирусе. Нашел обращение греческого доктора из университета в Афинах, которое вышло 18 апреля. Доктор пытается призвать внимание общественности к коагулопатии с развитием ДВС-синдрома.
После этого нашел статью от 21 апреля в Ланцет. Авторы также сообщают нам о коагулопатии, высоченном риске тромбозов и необходимости ранней антикоагуляции.
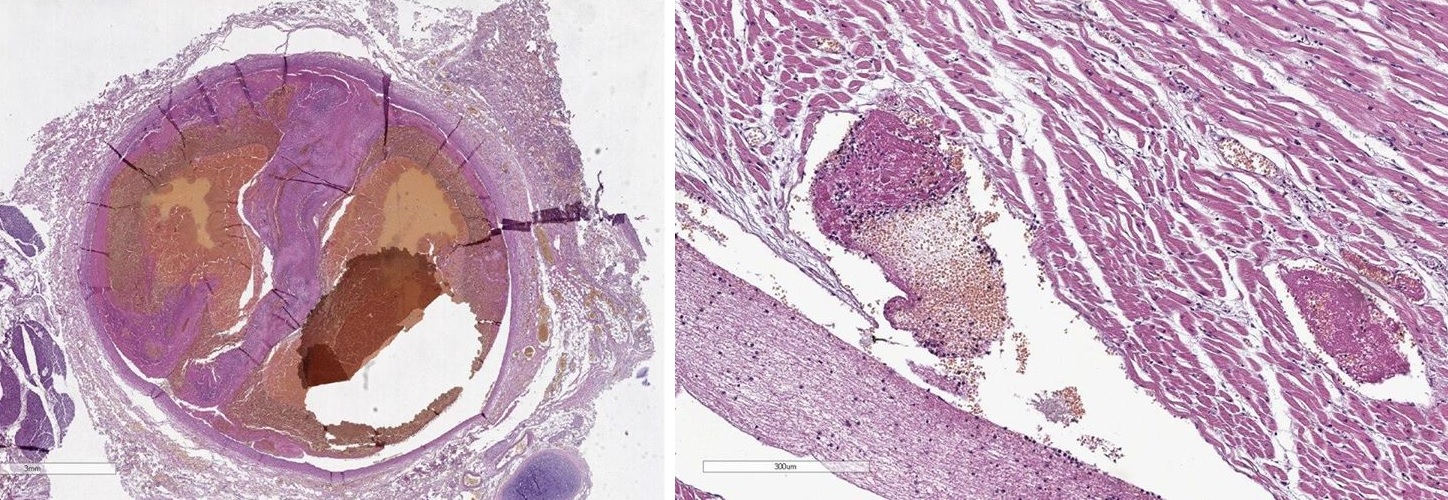
И практически убедившись в том, что я постиг что-то сокровенное и сокрытое ото всех, я случайно знакомлюсь с прекрасным патоморфологом Лилией Селивановой, с которой мы общаемся по переписке. Лилия занимается исследованием умерших пациентов с ковид+. И видит, что у большинства умерших от коронавирусной инфекции были тромбы: в легочной артерии, в мелких венах, в коронарных артериях, картина практически идентичная у всех больных. Ни в одном случае не было бактериальной пневмонии. Альеволы заполнены отечной жидкостью, гиалиновыми мембранами, десквамированными альвеолоцитами, где-то были эритроциты.
Причем Лилия также замечает, что примерно 1/3 больных были молодыми, накаченными мужчинами, что лично я связываю с возможным использованием стероидов или гормона роста, которые у культуристов ассоциированы с развитием тромбоза, и гипертрофической кардиомиопатии. Но для подтверждения моего объяснения необходимо брать анализы на тестостерон и соматотропин. Что, конечно, вряд ли кто-то делает у этого пула больных при посмертном анализе.
Какой из этого всего я делаю вывод для себя и своей семьи (никого ни к чему не призываю). Если/когда я заболею и это будет вызывать дыхательную недостаточность, и я смогу удерживаться дома и не госпитализироваться, то я:
– как можно раньше начну антикоагулянтную терапию;
– не буду использовать гидроксихлорохин. Оценка его эффективности привела к вынужденной остановке исследования в Бразилии ввиду высокого риска смертности от жизнеугрожающих аритмий;
– не буду использовать калетру. Не понимаю как она должна помочь, плюс она также увеличивает риски развития нарушений ритма сердца и токсического поражения почек;
– буду использовать антибиотики только в случае, если докажу наличие бактериального поражения. В противном случае не буду принимать антибиотики;
– не буду знать, что делать с антиагрегантами: скорее, не буду использовать для того, чтобы не наращивать риски возможного кровотечения (см. п.1);
– остальной менеджмент – симптоматическая терапия;
– и да, пожалуйста, не подключайте меня к ИВЛ. В пользу этого говорит не только базовая медицина, но и пугает статья на JAMA, авторы которой удивили меня статистикой смертности у пациентов на ИВЛ. 89% это конечно че-то многовато. Понятно, что методология подсчета была нарушена, но обилия плюсов от ИВЛ я всё ещё не могу найти. Поэтому скорее нет, чем да. Но тут как пойдет. Не будут же врачи молча и безучастливо наблюдать за тем, как нарастает дыхательная недостаточность… Такое себе зрелище для бездействия.
Кстати, из той же статьи на JAMA – некурящих людей аж 84%. Не успел углубиться в эту тему, возможно это наблюдение объясняется сниженным количеством АСЕ2 рецепторов у курильщиков. Возможно, причины в другом. Надо почитать поглубже. Но пока руки не дошли.