В клетках незрелого метаплазированного эпителия отмечаются признаки репарации что это значит
Цитологическая диагностика заболеваний шейки матки
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.
Цитология шм
Добрый вечер! Помогите, пожалуйста, расшифровать результаты цитологии: В препарате обнаружены клетки плоского эпителия промежуточного и поверхностного слоев с реактивными изменениями части клеток. Скопления цилиндрического эпителия с реактивными изменениями, в части клеток дегенеративно-дистрофические изменения. Участки из метаплазированных клеток с репаративными изменениями, ядра округлые, хроматин распределен равномерно, цитоплазма плотная, гомогенная.
Воспалительный компонент. Паракератоз в части клеток.
Клеток с признаками интраэпителиальных изменений и признаками злокачественности в пределах исследуемого материала не найдены. Лейкоцитарная реакция умеренно-выраженная. Специфический инфекционный агент не выявлен. Цитограмма соответствует воспалительному процессу слизистой оболочки (NILM). Эту цитологию сдавала 2 февраля, а до этого брали так же цитологию 30 числа( она получше по результатам). Может ли повлиять повреждение слизистой на результат второй цитологии после проведения первой?
Мазок на флору с небольшим повышением лейкоцитов, посев на флору : обнаружен рост нормофлоры
На сервисе СпросиВрача доступна консультация гинеколога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!
Светлана, врачи никогда не осмотре не говорили ничего про такое..говорили, что все хорошо. Кольпоскопию не делали, только осмотр со стеклом был и забор мазков) на данный момент ничего не беспокоит, месяц назад только выделения были и зуд(ставила свечи пимафуцин)
Просто мне один гинеколог брал цитологию 30 числа, и второй гинеколог тоже взял, но 2 числа
Первая цитология была лучше, может стоит опираться на ее результаты?
Так же результат NILM. Состою шейки матки: в препарате обнаружены скопления из клеток плоского эпителия поверхностных слоев с пикнотичными ядрами, обильной цитоплазмой и промежуточных слоев с овальными ядрами, контуры ровные, хроматин зернистый, распределён равномерно. Клетки с прищепками атипии не обнаружены. Соскоб с цервикального канала: в препарате обнаружены клетки цилиндрического эпителия обычного строения, расположенных разрозненно и скоплениями, с овальными ядрами, контуры ровные, хроматин зернистый, распределён равномерно. Единичные группы метаплазированного эпителия без патологии. Плоский эпителий поверхностных слоев с пикнотичными ядрами, обильной цитоплазмой и промежуточных слоев с овальными ядрами, контуры ровные, хроматин зернистый, распределён равномерно. Клетки с признаками интраэпиталиальных изменений и злокачественности не обнаружено. Лейкоцитарная реакция незначительная
Ольга, здравствуйте! Просто мне один гинеколог брал цитологию 30 числа, и второй гинеколог тоже взял, но 2 числа
Первая цитология была лучше, может стоит опираться на ее результаты?
Так же результат NILM. Состою шейки матки: в препарате обнаружены скопления из клеток плоского эпителия поверхностных слоев с пикнотичными ядрами, обильной цитоплазмой и промежуточных слоев с овальными ядрами, контуры ровные, хроматин зернистый, распределён равномерно. Клетки с прищепками атипии не обнаружены. Соскоб с цервикального канала: в препарате обнаружены клетки цилиндрического эпителия обычного строения, расположенных разрозненно и скоплениями, с овальными ядрами, контуры ровные, хроматин зернистый, распределён равномерно. Единичные группы метаплазированного эпителия без патологии. Плоский эпителий поверхностных слоев с пикнотичными ядрами, обильной цитоплазмой и промежуточных слоев с овальными ядрами, контуры ровные, хроматин зернистый, распределён равномерно. Клетки с признаками интраэпиталиальных изменений и злокачественности не обнаружено. Лейкоцитарная реакция незначительная
Классификация патологии шейки матки
Существует несколько классификаций патологий шейки матки:
Различают три основные группы заболеваний шейки матки: фоновые, предраковые и рак.
Фоновые или доброкачественные процессы – состояния, при которых изменений в клетках нет, т.е., сохраняется так называемая нормоплазия эпителия. Клетки правильно размножаются, растут, дифференцируются. К этим заболеваниям относятся: эктопия шейки матки, эктропион, полип, эндометриоз, лейкоплакия, папиллома, цервициты, истинная эрозия.
Эктопия шейки матки или эктопия цилиндрического эпителия. Это особенный диагноз и требует специального акцента. Состояние эктопии выявляется примерно у половины гинекологических пациенток. Представляет собой смещение границ эпителия, то есть внутренняя часть клеток как бы сползает вниз. Это не болезнь, а скорее нарушение клеточных границ. Обычно стык внутренних и внешних клеток шейки (зона трансформации) располагается во внутренней части канала и не видна. Но если граница смещается на влагалищную часть шейки, то это визуализируется при осмотре.
Врожденная неосложненная форма эктопии в номенклатуру патологий не внесена, болезнью не является и представляет собой физиологическое состояние. Буквально еще несколько лет назад любое красное пятно на шейке называлось «эрозией» и нещадно залечивалось. Именно поэтому эрозией болели огромное количество советских и российских женщин, и это был лидирующий диагноз! На сегодняшний день правильным определением смещения цилиндрического эпителия является «эктопия цилиндрического эпителия». Физиологическая эктопия шейки матки является вариантом нормы у молодых женщин до 25 лет, в более зрелом возрасте требует регулярного осмотра, цитологического и кольпоскопического контроля. Риск развития рака на фоне эктопии возникает при сочетании с другой патологией – воспаления, лейкоплакии, плоских кондилом. Осложненная форма эктопии сочетается с воспалительными и предраковыми процессами и требует тщательного подхода к обследованию и лечению.
Эктропион – выворот слизистой оболочки канала. Он возникает после разрывов и/или неправильного ушивания шейки матки. Это последствие послеродовых травм или абортов. То есть приобретенный эктропион всегда имеет травматический генез; врожденный встречается крайне редко и обычно сочетается с нарушением менструального цикла.
Полип шейки матки – разрастание слизистой оболочки округлой формы, с гладкой поверхностью. При расположении полипа внутри цервикального канала никаких симптомов не бывает, но если он разрастается и выглядывает из шеечного канала, то может себя проявить кровянистыми выделениями вне менструации и/или во время полового контакта.
Эндометриоз шейки матки характеризуется появлением очагов эндометриоза на шейке. Обычно протекает бессимптомно и выявляется только при осмотре в виде красных точек, так называемых «глазков». Редко проявляет себя кровянистыми выделениями или ощущением дискомфорта. Эндометриоз шейки возникает после хирургических вмешательств с использованием острых инструментов – в место прокола или надреза проникают клетки эндометрия и приживаются там, как при любом экстрагенитальном эндометриозе. Эндометриоз шейки, как правило, не представляет никакой опасности и требует обычного наблюдения и цитологической диспансеризации.
Кондиломы и папилломы – ВПЧ (HPV) – называют ассоциированными патологиями. Проявляются разрастаниями эпителия, являясь следствием инфицирования вирусом папилломы человека. Остроконечные кондиломы (папилломы) представляют собой отдельные прозрачные сосочки, имеют складчатость, выросты и ворсинки. Плоская кондилома выглядит как контур неправильной формы, слегка возвышающийся над слизистой. Эти образования могут располагаться как на шейке, так и в складках влагалища, на промежности и в перианальной зоне.
Предраковыми называют процессы, при которых возникают изменения в строении и росте клеток с нарушением дифференцирования. К этим процессам относятся: CIN, лейкоплакия с атипией, эритроплакия, аденоматоз. Это группа патологических изменений, занимающая промежуточное положение между нормальным эпителием шейки и раком.
По Международной классификации болезней выделяют следующие виды дисплазий:
CIN I – слабая дисплазия
CIN III – резко выраженная, а также карцинома in situ
Распространенность дисплазии в мире чрезвычайно высока. Этот диагноз поставлен миллионам женщин в мире. Наиболее часто регистрируется CIN II, ежегодно около 10 миллионов случаев. Но не каждая дисплазия переходит в рак и об этом важно знать! Скрининг, своевременная диагностика и лечение значительно (!) снижают вероятность перехода дисплазии в рак.
Дисплазии слабой и умеренной степени часто сочетаются с воспалительным процессом. Качественное лечение воспаления позволяет не только предотвратить переход дисплазии в следующую фазу, но и восстановить нормальную структуру тканей и избавиться от самой дисплазии. Важно обращать внимание на самочувствие, регулярно сдавать гинекологический мазок на микрофлору и половые инфекции, и своевременное обнаружение проблем и лечение позволят содержать флору влагалища в устойчивом состоянии, и снизит вероятность возникновения дисплазии.
Рак шейки матки никогда не возникает «вдруг», это заболевание обязательно должно пройти все стадии своего развития. И на каждом этапе правильные диагностика и лечение в состоянии прервать процесс развития рака. Именно поэтому столь важно относиться к диагностике внимательно – цитология, кольпоскопия, своевременная (!) биопсия могут дать быстрое обнаружение предраковых процессов.
Сдать анализ на цитологическое исследование по системе Бетесда
| Исследуемый биоматериал | Соскоб из экзо/эндоцервикса |
| Метод исследования | световая микроскопия |
| Cрок исполнения с момента поступления биоматериала в лабораторию | 2 к.д. |
Описание
ПАП-тест, или цитологическое исследование мазков из экзо- и эндоцервикса методом Папаниколау, является скрининговым методом диагностики патологии шейки матки. Данный вид цитологического исследования рекомендован большинством сообществ и входит в современные клинические рекомендации. В рамках настоящего анализа ПАП-тест проводится классическим методом, а именно материал наносится на стекло. Забор мазков проводит врач, используя специальные эндобраши (цитощеточки) для изолированного получения мазков с поверхности шейки матки (экзоцервикс) и из цервикального канала. Мазки наносятся на стекло, которое в дальнейшем будет направлено врачам-цитологам для оценки полученного материала. Метод Папаниколау является наиболее точным исследованием клеток экзо- и эндоцервикса. В отличие от других методов используется несколько сложных красок для лучшего окрашивание цитоплазмы и ядер. Также мазок фиксирует 96% спиртом. Такая методика позволяет снизить количество ошибок, допущенных из-за недостаточной подготовки материала непосредственно к исследованию, а также дает возможность цитологам оценить максимально окрашенный материал. Описание цитограммы при этом всегда развернутое, а заключение согласно существующей классификации Бетесда.
Классификация Бетесда.
Оценка качества мазка:
Материал полноценный, содержит клетки плоского и цилиндрического эпителия в достаточном количестве.
Неудовлетворительный для оценки (неинформативный) материал, Скудное количество клеток или их отсутствие.
Цитограмма в пределах нормы (NILM):
Содержит клетки поверхностного и промежуточного слоев многослойного плоского эпителия, клетки метаплазированного эпителия, лейкоциты, клетки цилиндрического эпителия, клетки эпителия эндометрия.
Метаплазия (норма), клетки плоского метаплазированного эпителия свидетельствуют о том, что материал забран из зоны трансформации.
Реактивные изменения:
Цитограмма воспаления, дегенеративные и реактивные изменения клеток, воспалительная атипия, плоскоклеточная метаплазия, гиперкератоз, паракератоз, койлоцитоз и другие признаки вирусного поражения.
Патологические изменения эпителия:
ASCUS (atypical squmous cells of undetermined significance), Изменения, которые трудно дифференцировать между реактивными изменениями эпителия и дисплазией. При ASCUS определяются клетки, трактовка которых затруднена — клетки с дискариозом, укрупненными и гиперхромными ядрами. Рекомендуется динамическое наблюдение и дообследование, а именно повторное цитологическое исследование через 6 месяцев и ВПЧ-тестирование. В случае подтверждении ASCUS и наличии вируса папилломы человека высокого онкогенного риска — проводится кольпоскопия. Исследования показывают, что 20% женщин с ASC имеют дисплазию после более тщательного обследования.
Предопухолевые изменения:
LSIL (CIN I), слабовыраженное интраэпителиальное поражение, включающее папилломавирусную инфекцию. Рекомендуется наблюдение без активной терапии. У большинства женщин LSIL самостоятельно регрессирует в течение нескольких лет. В эту группу объединены все изменения с низким злокачественным потенциалом, поскольку цитолог зачастую не может отличить изменения при ВПЧ инфекции и CIN 1.
HSIL (CIN II-III), умеренно выраженное и тяжелое интраэпителиальное поражение. Рекомендуется удаление всех пораженных тканей методом (конизация) с последующим морфологическим исследованием. В эту группу объединены все изменения с высоким злокачественным потенциалом.
AGC (atypical glandular cells), Атипические клетки цилиндрического эпителия. Рекомендуется выскабливание цервикального канала для гистологического исследования.
Опухолевые изменения:
Плоскоклеточный рак, злокачественная опухоль из плоского эпителия.
Железистый рак, злокачественная опухоль из железистого эпителия эндоцервикального типа.
Эндометриальный рак, злокачественная опухоль, развивающаяся из слизистой оболочки матки и прорастающая в цервикальный канал.
Подготовка
У женщин репродуктивного возраста рекомендуется забирать мазки не ранее, чем на 5-й день менструального цикла и не позднее, чем за 5 дней до предполагаемого начала менструации.
Показания
Интерпретация результата
Результаты лабораторных исследований не являются единственным критерием, учитываемым лечащим врачом при постановке диагноза и назначении соответствующего лечения, и должны рассматриваться в комплексе с данными анамнеза и результатами других возможных обследований, включая инструментальные методы диагностики.
В медицинской компании «LabQuest» Вы можете получить персональную консультацию врача службы «Doctor Q» по результатам исследований во время приема или по телефону.
Терминологическая система Бетезда(TBS-2014). Алгоритмы ведения пациенток

«В центре нашего внимания женщина, чьё предраковое поражение шейки матки должно быть диагностировано точно, быстро и полностью удалено, с тем, чтобы предотвратить развитие инвазивной карциномы и вернуть ей радость жизни».
История проблемы
«Я не мог убедить своих коллег в практичности процедуры».
Джорж Папаниколау, 1928 год.
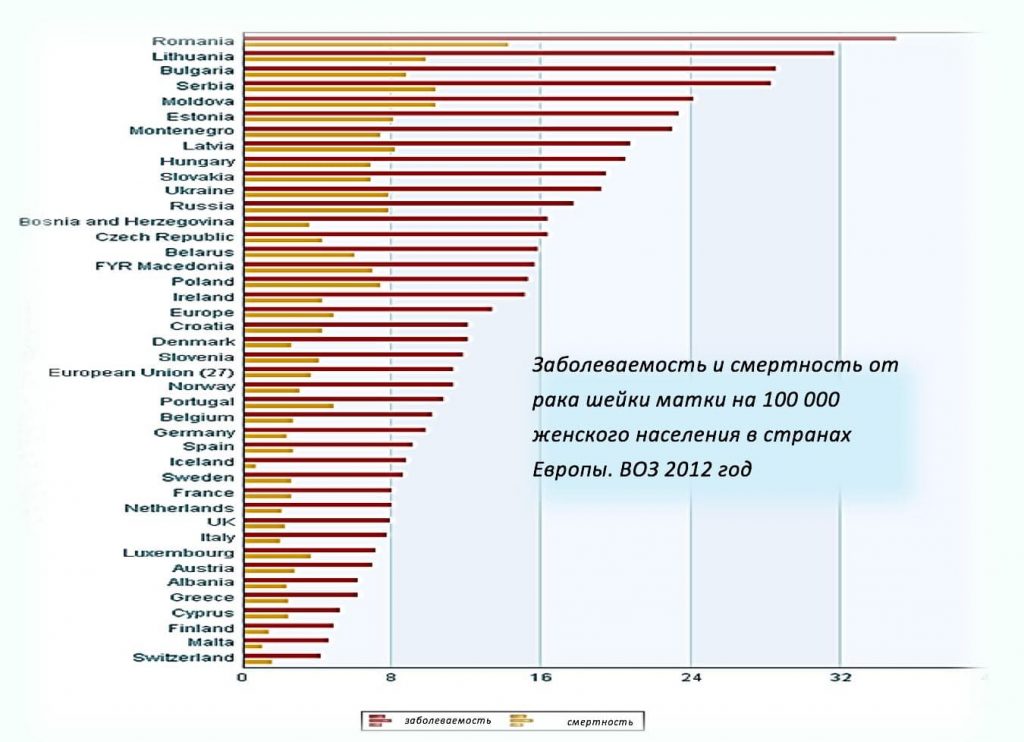
Эпидемиология рака шейки

По данным ВОЗ (2012):
Этиология

Рак шейки матки связан с персистированием ДНК вируса папилломы человека высокого риска (hrHPV). Согласно результатам мета-анализа (Li et al.2011) превалирование (hrHPV) обнаруживают в 85.9%-92.9% случаев рака. Аногенитальные типы HPV, вовлечённые в развитие карциномы и кондилом принадлежат к α-роду и подразделяются на два основных типа: hr (высокого риска) и lr (низкого риска).
lrHPV ассоциированы с кондиломами и транзиторной инфекцией. В большинстве случаев иммунная система, посредством апоптоза инфицированных клеток, элиминирует вирус lrHPV, а повреждения восстанавливаются регенерацией плоского эпителия.
hrHPV способен интегрироваться в ДНК человека и при отсутствии лечения вызывает карциномы урогенитальной и орофарингеальной области.
Частота выявления различных типов hrHPV при цервикальной карциноме в Европе
(de Sanjose et al.2010): HPV 16 – 66%, HPV 18 – 7%, HPV 33 – 6%,HPV 45 – 4%,HPV 31 – 3%.
При аденокарциномах наиболее часто выявляют: HPV 16,18,45.
Карциногенный эффект hrHPV необходимо рассматривать в контексте факторов риска, которые способствуют персистированию вируса:
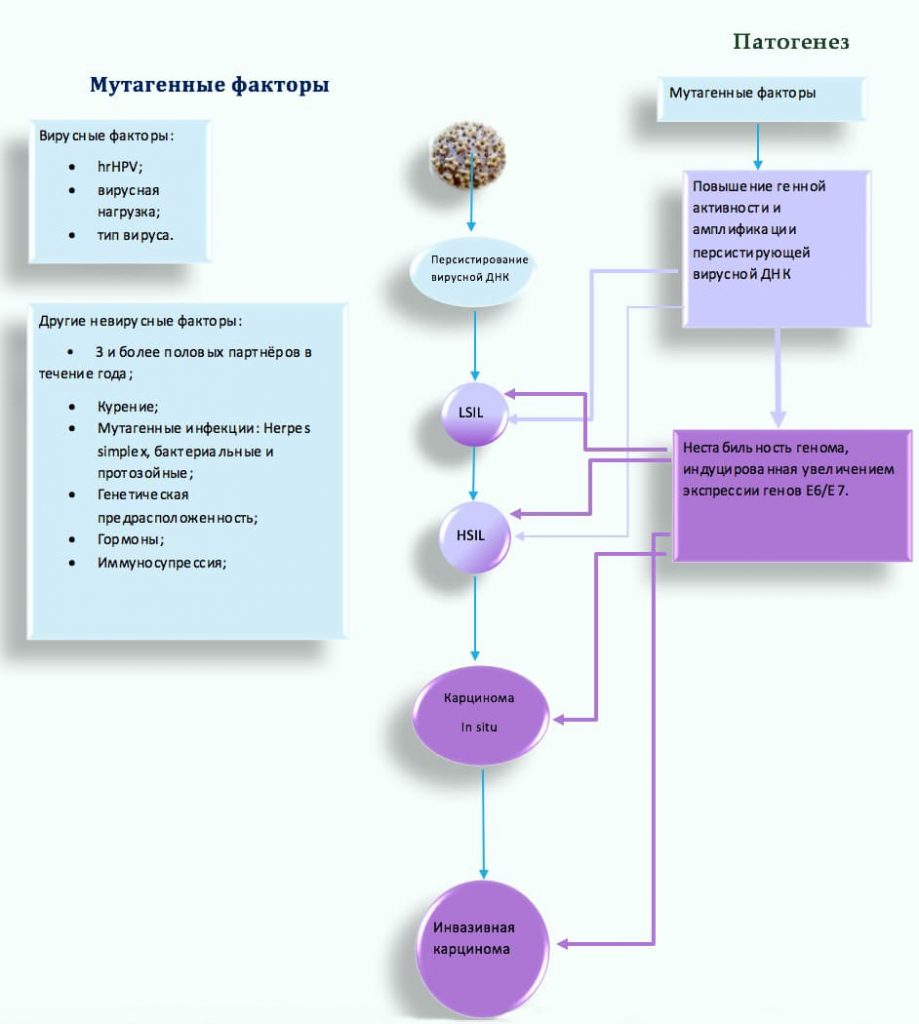
Роль HPV и других факторов риска в онкогенезе
Формы существования ВПЧ в инфицированных клетках и ключевые, интегральные вирусные гены.
Ключевую роль в патогенезе играют:
P53 и Rb – белки, вовлечённые в процессы восстановления повреждённой ДНК и активации апоптоза клеток, с необратимыми структурными нарушениями генома.
Этапы развития инвазивной плоскоклеточной цервикальной карциномы
Инвазивной плоскоклеточной карциноме предшествует цервикальная интраэпителиальная неоплазия (CIN I,II,III).
CIN (I,II,III) – гистологические типы не инвазивной стадии заболевания, напрямую связанные с процессами инфицирования и интеграции ВПЧ, при которой аномальные клетки ограничены слоем эпителия.

ВПЧ16 и 33 характеризуются самым высоким риском прогрессии в CIN III.
ВПЧ 16 и 31 практически никогда не регрессируют.
Итак CIN I или LSIL – в большинстве случаев,
продуктивная или эписомальная стадия инфицирования ВПЧ.
CIN II, III или HSIL – интегративная или интросомальная стадии инфицирования ВПЧ.
Регуляция процесса деления (переход клетки из G1 в S фазу) нормальной эпителиальной клетки и при эписомальной инфекции ВПЧ
Нарушение регуляции клеточного деления при трансформирующей интросомальной инфекции ВПЧ
Избыточная экспрессия p16 высоко коррелирует с онкогенной трансформацией, вызванной персистирующим вирусом ВПЧ высокого риска (hrHPV).
В клетках эпителия, инфицированных трансформирующей hrHPV, онкопротеин вирусной ДНК E7 замыкает белок ретинобластомы, что нарушает образование комплекса pRb E2F. Это приводит к бесконтрольной пролиферации клеток эпителия, с вирусной ДНК, генетической нестабильности, гиперэкспрессии белка p16, которую выявляют при иммуноцитохимическом окрашивании жидкостных Пап-препаратов.
Таким образом, иммуноцитохимическое окрашивание на белок p16 позволяет:

А-LSIL (CIN I) – слабоположительное окрашивание.
Б-HSIL (CIN II) – умеренное окрашивание.
В-HSIL (CIS) – резко положительное окрашивание.
Г – HSIL (CIS) – резко положительное окрашивание. (И.П.Шабалова, К.Т. Касоян.2016).
Роль иммуногистохимического окрашивания на белок p16 в выработке тактики ведения пациенток по результатам гистоморфологического исследования.
А. Использование иммуногистохимического окрашивания биопсийного материала на белок p16 с целью дифференциальной диагностики HSIL от не неопластических мимикрирующих процессов, таких как незрелая плоскоклеточная метаплазия, атрофическая метаплазия и репарация.
Иммуноцитохимический тест P16/Ki67 (CINtec Plus).
В последние годы большое внимание цитологов направлено на исследование диагностической значимости одновременного определения экспрессии белков р16 и Ki-67 в цитологических препаратах для идентификации плоскоклеточного интраэпителиального поражения высокой степени (HSIL) в Pap-тесте с диагнозом ASC-US (клетки плоского эпителия с атипией неясного значения, LSIL (плоскоклеточное интраэпителиальное поражение низкой степени) и ASC-H, при которых представляется затруднительным исключить HSIL. По результатам одного из самых значительных проспективном диагностическом исследовании, в которое вошло 27 000 женщин из разных стран (PALMS- Primary, ASC-US, LSIL Marker Study), были сделаны следующие выводы о диагностической значимости теста P16/Ki67:

Взаимодействие ВПЧ с эпителиальной клеткой происходит по 2 основным сценариям:

Особенности и неоспоримые преимущества ЖЦ
Правила подготовки к проведению Пап-теста 
Наилучшее время для Пап-теста: промежуток между 5-м и 22-м днями цикла. Если Вам предстоит Пап-тест, то в за 2 дня Вы не должны:
Техника взятия материала для проведения BD SurePath Пап-теста
Цитологическое заключение составляется в течение 3-х рабочий дней с интерпретацией результатов по системе Bethesda 2014 (TBS-2014)
Этапы роботизированной пробоподготовки и клеточного обогащения SurePath
Окрашивание мазков, приготовленных по технологии BD SurePath
Технология BD SurePath предусматривает единственный метод окрашивания мазков – по Папаниколау. Это метод полихромного окрашивания клеточной суспензии. По признанию всех специалистов, он является наилучшим для гинекологических препаратов. Окраска по Папаниколау обладает целым рядом преимуществ перед другими методами, которые делают её мировым стандартом окрашивания мазков при проведении Пап-теста:
Фундаментальные принципы системы Bethesda:
Терминология цитологического заключения Пап-теста должна быть:
Основные категории
Атипия плоского эпителия
Атипия железистого эпителия
Причины последнего пересмотра TBS в 2014 году

В настоящее время TBS-2014 рекомендована во всём мире, как наиболее оптимальная терминологическая классификация патологических изменений шейки матки, которая составляет основу формирования цитологического заключения.

Более того, на основе ключевых принципов терминологической системы цервикальной патологии, позднее стали формироваться стандартизированные цитологические классификации для описания патологии иных локализаций: система Бетезда для щитовидной железы 2010 года, поджелудочной железы и Парижская система интерпретации патологии уринарного тракта 2013 года. В соответствии со «стилем Бетезда», каждая диагностическая категория в этих системах описана с ориентировочным риском развития злокачественной патологии и рекомендациями по ведению пациентов. И, самое главное, что аналогичная двухуровневая терминологическая система для плоскоклеточных поражений LSIL и HSIL, используемая цитологическами классификациями, в настоящее время рекомендована ВОЗ и ACSSP, для гистоморфологических описаний ВПЧ-ассоциированных поражений нижнего аногенитального тракта (Stoler M. Et al, 2014).
Пункты, которые содержит цитологическое заключение по системе Бетесда 2014, приведены в таблице 1.
Специфические инфекционные агенты:
Другие: клетки эндометрия (у женщин в возрасте старше 45 лет).
Атипичные клетки железистого эпителия:
Атипичные клетки железистого эпителия: эндоцервикальные клетки/железистые клетки с подозрением на неоплазию (AGC favor neoplastic);
Эндоцервикальная аденокарцинома in situ (AIS). Аденокарцинома:
Другие злокачественные новообразования (указать какие).
Дополнительные тесты (Результаты исследования).
Указание использования компьютеризированной интерпретации препарата (если применялясь).
Особенности последней редакции TBS-2014
Глава 1. Оценка адекватности образца.
Чувствительность Пап-теста в значительной степени определяется качеством взятия материала и способом приготовления цитологического препарата. Поэтому в цитологическом отчете важно указать метод исследования (традиционный или жидкостной). Для каждого из них существуют строго определённые требования к количественному составу клеточных элементов плоского эпителия, цилиндрического и метаплазированного.
Критерии адекватности по системе Бетезда
Образец считают удовлетворительным для оценки если:
При отсутствии клеток ЗТ образец может быть признан адекватным для оценки, но с обязательным указанием, что в образце не представлены клетки цилиндрического или метаплазированного эпителия, что отразится на тактике ведения пациентки.
Неудовлетворительным образец считают в следующих ситуациях:
Рекомендации при неудовлетворительном образце:
Система Бетезда: Т-зона. Цитологическое резюме:
Алгоритм ведения пациенток с цитологическим заключением NILM, нет ЗТ.
Глава 2. TBS-2014 посвящена категории неопухолевых изменений NILM (негативные в отношении интраэпителиальных поражений и злокачественности) с указанием типа:
I.Неопухолевые клеточные изменения:
II. Реактивные изменения, связанные с:
А также указывают на наличие специфических инфекционных агентов:
NILM –это категория, в которую входят все случаи без признаков внутриэпителиальной неоплазии. И это не только абсолютная норма, но и образцы с различными доброкачественными изменениями, которые возникают по ряду причин, а именно: острое и хроническое воспаление, гормональные сдвиги, беременность, кормление грудью, изменения pH, использование контрацептивов, облучение и химиотерапия в лечебных протоколах. Среди неопухолевых доброкачественных процессов, на которые необходимо акцентировать внимание, выделяют следующие:

Кератоз (без признаков атипии) – проявления защитной реакции в виде ороговения верхних слоёв эпителия, которая возникает, как правило, в ответ на хроническое воспаление, в том числе, вызываемое низкими титрами ВПЧ, при отсутствии каких-либо признаков неоплазии. Считают, что кератоз – это вторая линия защиты эпителиальных клеток, после метаплазии, которая представляет собой первую реакцию в ответ на действие повреждающего фактора. Кератоз, паракератоз, гиперкератоз и дискератоз – это описательные термины, которые в прошлом использовались непоследовательно. Потому в последней редакции для описания выявленных доброкачественных изменений используется единый термин «кератоз». После метаплазии, хроническое воздействие повреждающего фактора приводит, как правило, к образованию в клетках кератогиалиновых гранул и последующему кератозу.
Критерии гиперкератоза: безъядерные клетки плоского эпителия поверхностных слоёв, полностью сохранившие клеточные контуры, но с пустыми пространствами на месте ядра, так называемыми «ядрами-призраками». Ранними признаками наступающего гиперкератоза являются клетки поверхностного эпителия с керато-гиалиновыми гранулами.
Критерии паракератоза: миниатюрные клетки поверхностных слоёв различной формы, с оранжевой или розовой цитоплазмой и маленькими пикнотичными ядрами. Ядерно-цитоплазматическое соотношение не нарушено, ядра округлые, с ровным контуром и напоминают по форме и размерам ядра соседних клеток. При обнаружении паракератозных клеток, необходимо полностью убедиться в отсутствии признаков ядерной атипии, в противном случае, при наличии плеоморфизма ядер, гиперхромазии и увеличенного ядерно-цитоплазматического соотношения, паракератоз интерпретируют, как ASC-US или ASC-H, или SIL. Для полной уверенности в интерпретации изменений, как NILM, следует провести ко-тестирование на ДНК ВПЧ.


Трубная метаплазия – это метапластический феномен, при котором нормальные эндоцервикальные клетки замещаются эпителием фаллопиевых труб. Этот феномен часто обнаруживается в верхней части цервикального канала.
Критерии трубной метаплазии

Цилиндрические реснитчатые клетки, располагающиеся небольшими группами. Круглые или овальные ядра часто бывают гиперхромными и плеоморфными. Хроматин распределён равномерно, ядрышки, как правило не видны. Ядерно-цитоплазматическое соотношение может быть увеличенным. Наличие ресничек и терминальной полоски – это самый важный отличительный признак этих клеток.
Трубная метаплазия – это доброкачественный процесс, но его часто принимают и интерпретируют, как атипичные эндоцервикальные клетки. Это происходит из-за увеличенных гиперхромных ядер, наслаивающихся друг на друга. Следует обращать внимание на наличие ресничек и терминальной полоски – признаков, позволяющих убедиться в доброкачественном характере обнаруженных структур.
Атрофия
Атрофия – это физиологический возрастной феномен, обусловленный снижением гормональной стимуляции, которая приводит к истончению эпителиального слоя, состоящего исключительно из незрелых базально/парабазальных клеток.

Атрофия с воспалением. Характерен фон препарата: дегенеративные изменения парабазальных клеток и полиморфноядерных нейтрофилов (ЖЦ).
В сложных случаях реактивно-репаративных изменений в клетках парабазального эпителия, иммуноцитохимическое окрашивание на белок р16 позволяет установить доброкачественную природу выявленных изменений.
Изменения, связанные с беременностью
В течение беременности в цитологических препаратах отмечают изменения, которые напоминают неопластические процессы. Это объясняется изменением гормонального фона, который приводит к неполному созреванию эпителия. Доминирующим клоном клеток во время беременности являются промежуточные клетки. Они напоминают лодочку и называются навикулярными клетками. Во время беременности отмечают феномен Ариас-Стеллы. Он представляет собой доброкачественный процесс, в который вовлечены клетки железистого эпителия (эндоцервикальные и эндометриальные). Критерии феномена:


Глава 3. TBS-2014 посвящена вопросу о необходимости указания в цитологическом заключении на наличие доброкачественных эндометриальных клеток у женщин старше 45 лет.

Глава 4. Эпителиальная атипия плоского эпителия. Клетки плоского эпителия с атипией неясного значения. (ASC).
В категорию ASC входят все случаи интраэпителиальных изменений, которые по качественным и/или количественным цитоморфологическим характеристикам не возможно отнести к LSIL или HSIL. В соответствии с критериями TBS-2014, в данной категории выделяют две группы клеток с атипией:
Категория ASC-US предполагает наличие клеточных изменений, более выраженных, чем реактивные, но по качеству или количеству, недостаточных для постановки LSIL. По данным различных исследований, в 40-50% случаев обнаруживают ДНК HR-HPV, а причина остальных цитоморфологических заключений, как ASC-US – реативно-репаративные процессы, присутствие специфического инфекционного агента, применение ВМС, атрофия, инфицированность ВПЧ низкого онкогенного риска, либо остаётся неизвестной. Однако, при интерпретации выявленных изменений, используя данные анамнеза и клинического осмотра, по возможности и данные пересмотра предыдущих исследований, а также ВПЧ-тестирования, следует помнить, что в 10-20% случаев ASC-US гистоморфологическое исследование даёт заключение HSIL. Hr-HPV тестирование является основным дифференциально диагностическим подходом для тактики ведения пациенток с цитологическим заключением ASC-US (R. Nayar, David C. Wilbur.2015). Обнаружение у пациентки любого возраста hr-HPV и цитоморфологических изменений, соответствующих критериям атипии неясного значения, позволяет поставить диагноз ASC-US или LSIL. При наличии указаний в цитологическом заключении на атипичную репарацию, вызванную воспалительным процессом, повторный Пап-тест назначают не раньше, чем через 2 месяца после окончания противовоспалительного лечения (И.П. Шабалова, К.Т. Касоян, 2016).
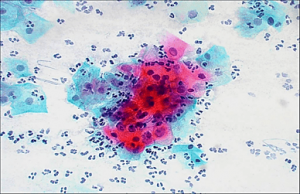
На данном слайде представлен кластер атипичных клеток, отнесённых к категории ASC-US. Клетки полиморфны по форме, размерам, ядерной гиперхромазии. Оксифильная цитоплазма клеток позволяет предположить HPV, однако классических койлоцитов в данном кластере нет.
Данная категория предполагает наличие всех убедительных цитоморфологических признаков LSIL в препарате, а также тех, которые подозрительны, но не совсем достаточны для заключения о наличии интраэпителиальных поражений высокой степени злокачественности (HSIL).
Цитоморфологические критерии:
При обнаружении резко выраженных изменений в структуре ядра (гиперхромия, высокое ядерно-цитоплазматическое соотношение, неровный контур), предпочтительным считают заключение HSIL. Цитологический диагноз ASC-H, не зависимо от результатов hr-HPV-тестирования, является показанием для проведения кольпоскопии. В практике цитологических исследований существует три основных ситуации, при которых устанавливают диагноз ASC-H:

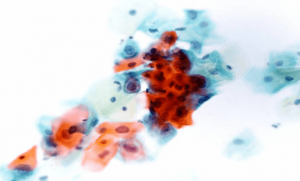
На данном слайде представлен цитологический образец ASC-H в метаплазированных клетках. Последующая биопсия установила диагноз HSIL – интраэпителиального поражения высокой степени злокачественности.
Риски для категории ASC-US/ASC-H развития HSIL в течение 5 лет.
На основании представленных рисков развития интраэпителиальных поражений высокой степени злокачественности (HSIL), специалистами ASCCP в 2012 году были разработаны алгоритмы ведения пациенток для всех категорий, в том числе и при атипии неясного значения. Основной принцип, положенный в основу всех алгоритмов при цервикальном скрининге – соответствие менеджмента риску. При этом Пап-тест специалисты рассматривают, как основную меру или эталон принятия решений.
Глава 5. Атипия плоского эпителия. LSIL/HSIL
Двухуровневая система разделения атипии плоского эпителия составляет основу терминологической системы Бетезда, которая полностью отражает биологию вирусно-эпителиальных взаимодействий. Поражения низкой степени злокачественности (LSIL) представляют собой продуктивную, транзиентную, эписомальную форму ВПЧ-обусловленных изменений плоского эпителия. Если продукты трансляции вируса (ранние и поздние гены) нарушают экспрессию крайне консервативных у млекопитающих генов (онкогенов, генов-ингибиторов опухолевого роста, генов-блокаторов апоптоза), возникает принципиально иная форма ВПЧ-ассоциированных изменений – интросомальная, интегрированная, которая морфологически проявляет себя поражениями плоского эпителия высокой степени злокачественности (HSIL). Основной целью цервикального скрининга
LSIL &CIN I & слабая дисплазия):
Продукция вируса & Транзиентная инфекция & Койлоцитарная атипия
Цитоморфологическую LSIL основу составляют инфицированные клетки с койлоцитарной атипией.
Койлоциты – клетки плоского эпителия, содержащие в ядре и цитоплазме вирусные частицы, репликация которых, приводит к характерным цитоморфологическим изменениям, свойственным койлоцитарной атипии. Они вызваны цитопатогенным действием вируса, которое приводит к некрозу ядра и цитополазмы.
Койлоцитарная атипия является одним из важнейших прямых признаков ВПЧ-инфицирования эпителия шейки матки.
Критерии:
HSIL & CIN II, CIN III, CIS & умеренная дисплазия, тяжёлая дисплазия, cr in situ. HPV E6/E7 экспрессия & риск инвазивного рака.
Терминологическая система Бетезда объединяет все типы дисплазий после категории CIN I в единую группу атипий плоского эпителия высокой степени злокачественности (HSIL), которые представляют собой интегрированную, инрососмальную форму ВПЧ-ассоциированных поражений. Принципиально важной и наиболее значимой частью цитологической практики является дифференциальная диагностика LSIL и HSIL, которая полностью опирается на чётко определённые цитоморфологические критерии. На первый план выступают все признаки незавершённого клеточного созревания.
Критерии HSIL:
Четыре наиболее частых морфологических типа HSIL
Дисплазия с ороговением: клетки с ярко выраженной атипией, с признаками ороговения цитоплазмы (оранжевые клетки при окраске по Папаниколау) располагаются в пластах, с наслаивающимися гиперхромными ядрами. Опухолевый диатез отсутствует, что отличает эту форму HSIL от инвазивного рака. Но, с другой стороны, гипер- и паракератоз-косвенные признаки ВПЧ-инфекции, могут протекать без признаков клеточной атипии, что затрудняет дифференциальную диагностику Данной формы HSIL.
Мелкие клетки с резким дискариозом: ядра атипичных клеток чуть больше, чем у лимфоцита. Клетки располагаются разрозненно или в гиперхромных пластах, в которых достаточно трудно определимы границы между ними. Цитоплазма почти не определяется т.к. ядро занимает практически 100% клеточного объёма. Дифференциальную диагностику проводят с фолликулярным цервицитом, эндометриальным клетками и незрелой метаплазией, нейроэндокринной карциномой.
HSIL в незрелых метаплазированных клетках: клетки преимущественно располагаются по одиночке, в отличие от незрелых метаплазированных клеток, образующих небольшие пласты. Как известно, ядерно-цитоплазматическое соотношение в нормальных незрелых метаплазированных клетках приближается к 50%. Дифференциальная диагностика должна опираться на признаки атипии: аномальное распределение хроматина, неровность ядерной мембраны, плеоморфность ядер в пластах, гиперхромию ядер и гранулярный хроматин. Цитоплазма плотная, с чёткими границами, вакуолизирована.
HSIL в атрофических мазках: гиперхромные парабазальные пласты клеток, лежащие на фоне воспаления и аутолиза – это общие морфологические черты HSIL и атрофии. Для дифференциальной диагностики необходимо опираться на следующие признаки: внимание должны привлекать отдельно лежащие популяции клеток с признаками дискариоза. При наличии атрофического вагинита, при котором клетки могут быть увеличены и несколько атипичны, рекомендовано проведение короткого курса местной терапии эстрогенами и последующее котестирование, включающее цитологическое исслеование и ВПЧ-тестом.


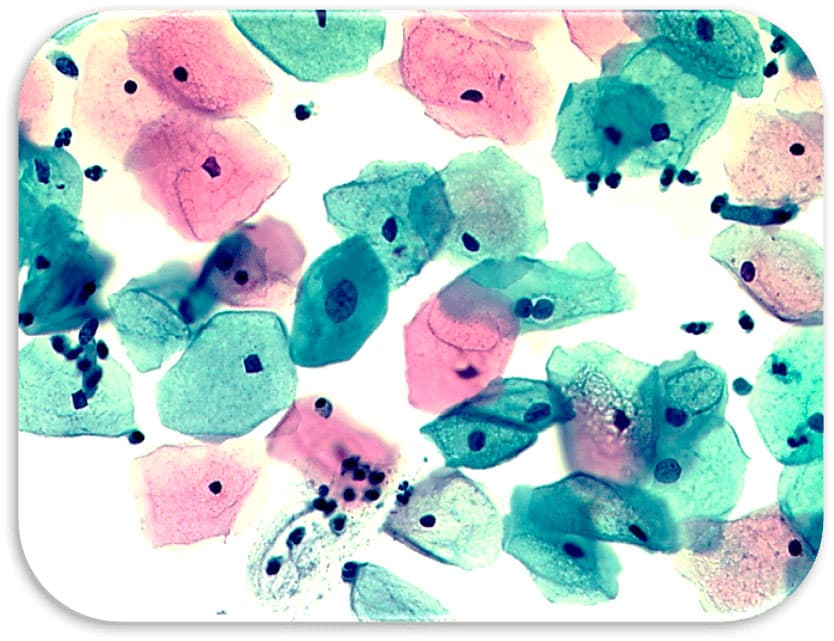
Глава 6. Атипия железистого эпителия (AGC).
Внедрение в практику Пап-теста жидкостных технологий приготовления препаратов, а также использование цитощёток Cervex-Brush Combi, захватывающих одновременно экто-эндоцервикс и зону трансформации, позволило существенно улучшить цитологическую диагностику патологии железистого эпителия, относительная доля которого в последние два десятилетия существенно возросла. (R. Nayar, David C. Wilbur.2015.).
Аденокарциномы соствляют 5-10% от всех неоплазм шейки матки. Гистологически выделяют три типа: эндоцервикальная, эндометриальная и светлоклеточная аденокарциномы. Эндоцервикальная аденокарцинома – самый распространённый и наиболее легко распознаваемый при цитологическом обследовании тип. Довольно часто она сочетается с плоскоклеточной карциномой, что свидетельствует об общности этих процессов по этиологии и патогенезу. Таким образом, наряду с плоскоклеточными неоплазмами, являются ВПЧ-ассоциированными злокачественными новообразованиями шейки матки. Достаточно долго аденокарцинома может не проявлять себя клинически, без изменений шейки матки. Цитологически выделяют три степени градации аденокарциномы, в зависимости от степени дифференцировки опухолевых клеток: высоко-, средне, и низкодифференцированная. Чем меньше дифференцировка, тем меньше злокачественные клетки напоминают нормальный эндоцервикальный эпителий.
В системе Бетезда выделена категория атипичных клеток железистого эпителия (AGC). Этот цитологический диагноз устанавливают если клеточная (ядерная) атипия превышает признаки реактивно-воспалительных изменений, но не является очевидной для постановки диагноза аденокарциномы.
| Атипия железистого эпителия: | |
| ASC-H | HPV-тест + кольпоскопия с биопсией. |
| LSIL | HPV-тест (-), повторное цитологическое обследование через 6 месяцев. |
| HSIL | HPV-тест+ кольпоскопия с биопсией. |
| Плоскоклеточная карцинома | Оперативное лечение |
| Атипия цервикальных клеток, возможно неоплазия; Эндоцервикальная аденокарцинома in situ Эндоцервикальная аденокарцинома | Кольпоскопия с конусовой радиоволновой эксцизией/гистероскопия с раздельным диагностическим выскабливанием цервикального канала и полости матки. |
| Эндометриальная аденокарцинома | Гистероскопия, раздельное диагностическое выскабливание цервикального канала и полости матки. |




Для получения профессиональной консультации обращайтесь к гинекологам нашей клиники.

























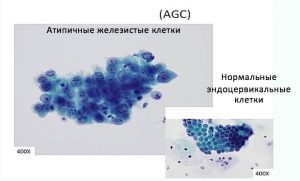 Критерии AGC:
Критерии AGC: