В результате чего развивается тканевая гипоксия
Кислородное голодание
Кислородное голодание может возникнуть как при недостаточном содержании кислорода в окружающей атмосфере, так и при некоторых патологических состояниях.
Гипоксия головного мозга наблюдается при нарушениях мозгового кровообращения, шоковых состояниях, острой сердечно-сосудистой недостаточности, полной поперечной блокаде сердца, отравлении окисью углерода и при асфиксии различного происхождения. Гипоксия головного мозга может возникать как осложнение при операциях на сердце и магистральных сосудах, а также в раннем послеоперационном периоде. При этом развиваются разнообразные неврологические синдромы и психические сдвиги, причем преобладают общемозговые симптомы, диффузное расстройство функций ЦНС.
Патогенез (что происходит?) во время Кислородного голодания:
Микроскопически может наблюдаться отек головного мозга. Ранним признаком гипоксии является нарушение микроциркуляторного русла – стазы, плазматическое пропитывание и некробиотические изменения сосудистых стенок с нарушением их проницаемости, выходом плазмы в перикапиллярное пространство. При тяжелой форме острой гипоксии рано выявляются различной степени поражения нейроцитов вплоть до необратимых. В клетках головного мозга обнаруживают вакуолизацию, хроматолиз, гиперхроматоз, кристаллические включения, пикноз, острое набухание, ишемическое и гомогенизирующее состояние нейронов, клетки-тени. Отмечаются грубые нарушения ультраструктуры ядра, его мембраны, деструкция митохондрий, осмиофилия части нервных клеток.
Выраженность изменений клеток зависит от тяжести гипоксии. В случаях тяжелой гипоксии может происходить углубление патологии клетки после устранения причины, вызвавшей гипоксию; в клетках, не имеющих признаков серьезных повреждений в течение нескольких часов, спустя 1-3 сут и позже можно обнаружить структурные изменения различной тяжести. В дальнейшем такие клетки подвергаются распаду и фагоцитозу, что приводит к образованию очагов размягчения; однако возможно и постепенное восстановление нормальной структуры клеток.
При хронической гипоксии морфологические изменения нервных клеток обычно менее выражены; глиальные клетки ЦНС при хронической гипоксии активизируются и усиленно пролиферируют.
Симптомы Кислородного голодания:
При возникновении острой кислородной недостаточности часто развивается возбуждение нервной системы, сменяющееся торможением и нарастающим угнетением ее функций. Возбуждение сопровождается двигательным беспокойством, эйфорией, учащением сердцебиения и дыхания, бледностью кожных покровов, появлением холодного пота на лице и конечностях. Вслед за более или менее длительным периодом возбуждения (а нередко и без него) развиваются явления угнетения с возникновением потемнения в глазах (после предшествовавшего «мелькания» перед глазами), головокружения, сонливости, общей заторможенности, оглушенности, с постепенным угнетением сознания.
Растормаживание и индукционное усиление деятельности подкорковых образований сопровождаются беспорядочной двигательной активностью, судорожными сокращениями мышц, общими тоническими и клоническими судорогами. Этот период обычно бывает кратковременным. Дальнейшее распространение торможения сопровождается изменением безусловных рефлексов: выпадают сначала кожные рефлексы (брюшные, подошвенные, кремастерные), затем надкостничные (запястно-лучевые, надбровные) и, наконец, сухожильные, которые вначале резко усиливаются, а потом угасают, обычно сначала на верхних, а затем на нижних конечностях. Далее выпадают зрачковые и корнеальные рефлексы. Однако последовательность исчезновения рефлексов не всегда бывает одинаковой; отмечаются случаи длительного сохранения отдельных рефлексов при отсутствии остальных. Двигательные расстройства характеризуются развитием спастического паралича с повышением тонуса мышц, рефлексов, появлением патологических и защитных рефлексов, а затем тонус мышц снижается, рефлексы угасают. При быстром развитии глубокого кислородного голодания уже через несколько десятков секунд происходит потеря сознания, а спустя 1-2 мин развивается кома. Вследствие гипоксии мозга могут развиваться следующие неврологические синдромы.
• Коматозные состояния (в зависимости от распространенности угнетения функций мозга
и уровня регуляции сохранившихся функций):
а) состояние декортикации (подкорковая кома); б) переднестволовая (диэнцефально-мезэнцефальная), или «гиперактивная», кома;
в) заднестволовая, или «вялая», кома; г) терминальная (запредельная) кома.
• Состояния частичного нарушения сознания: а) сопор; б) оглушение; в) сомноленция.
• Синдромы диффузного органического поражения: а) тяжелая постгипоксическая
энцефалопатия (с мнестическими, зрительными, мозжечковыми, стриарными расстройствами);
б) умеренно выраженная постгипоксическая энцефалопатия.
• Астенические состояния (постгипоксическая астения с явлениями гипо- и гиперстении).
Перечисленные синдромы могут быть фазами проявления последствий гипоксии мозга.
В основе наиболее тяжелой степени коматозного состояния (запредельная кома) лежит угнетение функций центральной нервной системы, клинически проявляющееся арефлексией, гипотонией мышц, отсутствием электрической активности мозга («молчание»), расстройствами дыхания. Сохраняются деятельность сердца, автоматическая деятельность других органов за счет периферической вегетативной регуляции.
С частичным восстановлением функций подкорковых узлов связаны особенности подкорковой комы, или состояния декортикации. Клиническая картина ее характеризуется выраженными симптомами орального автоматизма (иногда сосательными и жевательными движениями), усилением деятельности подкорковых рефлекторных уровней – стволовых, спинальных, периферических, вегетативных. Сухожильные рефлексы повышены, кожные – угнетены, вызываются стопные и кистев ые патологические рефлексы. Явления раздражения проявляются хореиформными и атетоидными гиперкинезами, миоклоническими подергиваниями в отдельных мышечных группах. На ЭЭГ определяются диффузные медленные волны.
По мере восстановления сознания у больных возникает состояние оглушения. Более глубокое оглушение определяется как сопор, легкие степени оглушения постепенно сменяются сомноленцией, что соответствует восстановлению функций коры головного мозга. При этом признаки восстановления сочетаются с симптомами выпадения и раздражения. Особенности клиники в большей степени определяются состоянием лимбико-ретикулярного комплекса.
При сопорозных состояниях имеются лишь самые элементарные реакции на внешние раздражения. На ЭЭГ обычно доминируют медленные волны. Оглушение сопровождается затруднением понимания больным сложных фраз, ограничением способности произвольных движений, затруднением запоминания. Больные обычно лежат неподвижно. На фоне оглушения иногда возникают сноподобные (онейроидные) состояния. При сомнолентных состояниях больных можно легко вывести из дремотного состояния, они адекватно отвечают на вопросы, но крайне быстро устают. На фоне состояния оглушения выявляются мнестические, гностические, праксические нарушения, симптомы поражения мозжечка и экстрапирамидной системы, а также другие органические симптомы. Такие нарушения определяются как постгипоксическая энцефалопатия, которая характериз уется преи мущественно выраженными расстройствами сознания, памяти, агнозиями, апраксиями, речевыми нарушениями (в форме афазий, дизартрии или мутизма), мозжечковыми симптомами, стриарными гиперкинезами, диффузными очаговыми органическими симптомами. В дальнейшем при восстановлении функций (иногда далеко не полном) долго сохраняются неврастеноподобные симптомы, характерные для постгипоксической астении. В основе этих состояний лежит ослабление тормозного процесса с развитием раздражительной слабости, повышенной возбудимости, бессонницы, снижением внимания и памяти (гиперстеническая форма) либо ослабление и тормозного, и возбудительного процессов, сопровождающееся вялостью, сонливостью, обшей заторможенностью (гипостеническая форма).
Лечение Кислородного голодания:
Противогипоксические средства весьма перспективны, но пока применяются главным образом в эксперименте. Большого внимания заслуживают попытки создания новых хинонов (на основе ортобензохинона). Защитными свойствами обладают препараты типа гутимина, оксибутирата натрия, а также средства из группы ноотропов.
К каким докторам следует обращаться если у Вас Кислородное голодание:
Механизмы гипоксии
Noreen R. Henig, David J. Pierson
Статья опубликована в журнале
Respiratory Care Clinics of North America
Volume 6, Number 4, December 2000
Четырьмя основными механизмами гипоксемии, которые необходимо запомнить каждому студенту медику являются низкий уровень кислорода, гиповентиляция, нарушение соотношения перфузии–вентиляции, сброс крови «справа налево». Если запомнить этот список и понять сами механизмы, то каждый может быстро и легко выявить причину гипоксии у пациента.
Человеческий организм является аэробным. Это значит, что все процессы клеточного метаболизма зависят от уровня молекул кислорода, которые поддерживают основные функции организма. Несмотря на то, что организму необходим кислород, клинически определить субоптимальные потребности очень тяжело и невозможно подсчитать. У пациентов с недостаточной оксигенацией могут наблюдаться цианоз, одышка, сердцебиение, потеря сознания, парестезии, усиление диуреза, гипотермия или боль. pH крови может быть понижен, а уровень лактата повышен в результате анаэробного метаболизма. Все или ни одного из этих признаков могут присутствовать, однако это дело лечащего врача подозревать гипоксию и выявлять ее причину.
В этой статье авторы обсуждают определение гипоксемии, обозревают анатомию легочной системы и этапы доставки кислорода и описывают четыре основные причины гипоксемии с примерами из практики. В заключении будет описан пятый механизм гипоксии, который у человека встречается очень редко. Вследствие того, что поместить кислород в кровоток человека это еще только полдела, авторы описали еще и механизм гипоксии тканей при адекватном обмене кислорода в легких.
Гипоксемия против гипоксии
Гипоксемия – это состояние, при котором парциальное давление кислорода в артериальной крови (РаО2) меньше нормального (менее 60 мм рт. ст.). Если пациент, дышит кислородом, но РаО2 у него ниже, чем ожидается, то необходимо исключить гипоксемию, даже если уровень РаО2 выше 60 мм рт. ст. Гипоксемия возникает вследствие непопадания кислорода в кровь. Гипоксия тканей возникает вследствие того, что клеткам не хватает кислорода для выполнения функции метаболизма. Хотя гипоксемия (слишком маленькое поступление кислорода в кровь) обычно является причиной гипоксии тканей, существуют другие состояния, которые прерывают поступление кислорода в кровь и приводят к гипоксии.
Для того чтобы понять обстоятельства, которые приводят к гипоксемии или гипоксии, необходимо представить путь, который проходят молекулы кислорода из воздуха в ткани, где они используются как топливо для клеток. Во время спонтанного дыхания мозг генерирует сигнал, который ведет к сокращению диафрагмы и расширению грудной клетки. При этом создается отрицательное давление в грудной полости, вследствие чего воздух проникает по дыхательным путям в альвеолы. Молекулы кислорода диффундируют через стенку альвеол в капилляры. В крови большинство кислорода переносится гемоглобином в эритроцитах, в то время как небольшой процент растворяется в плазме. Кровь перекачивается через легкие из правого желудочка сердца и после этого возвращается в левое предсердие и желудочек для того, чтобы оттуда разойтись по телу. По ходу того, как артерии разделяются на более мелкие капилляры, кислород освобождается из гемоглобина и поступает в ткани для питания клеток. Углекислый газ, который является продуктом клеточного метаболизма, диффундирует из тканей в капилляры и проходит по венозной системе в правое сердце. Кровь, насыщенная углекислым газом, проходит в легкие. Таким образом, углекислый газ может диффундировать через альвеолярно–капиллярный барьер, чтобы выйти из организма во время выдоха.
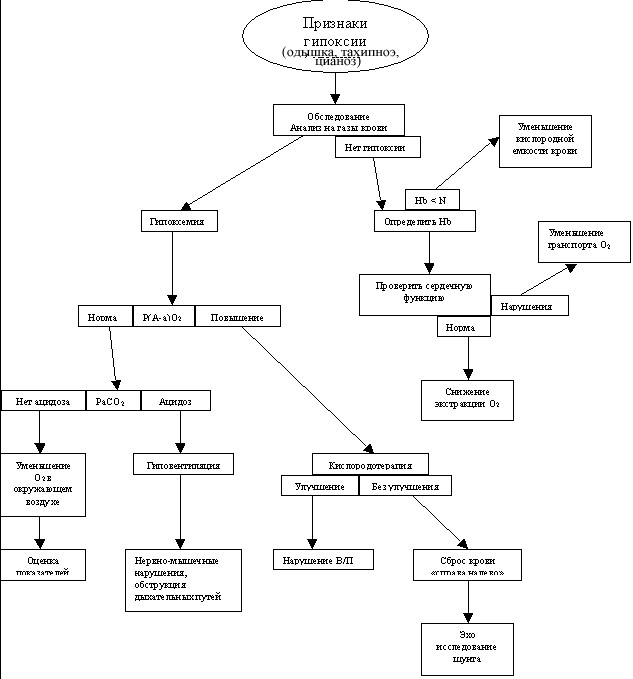 |
| Рисунок 1. |
Таблица 1. Механизмы гипоксии
Гипоксемия с нормальным Р(А-а)О2
Гипоксемия с увеличением Р(А-а)О2
Гипоксия тканей без гипоксемии
Механизмы гипоксемии
Уменьшение кислорода в окружающем воздухе
Неадекватный транспорт кислорода
Если кислород попал в кровь и связался с гемоглобином, то доставка кислорода к тканям начинает зависеть от сердечного выброса. Отношение сердечного выброса (Qt) и транспорта кислорода (DO2) показано в таблице 2. Уменьшение сердечного выброса может привести к внутренней сердечной дисфункции или внешним сердечным нарушениям. В результате уменьшения или нарушения сердечного выброса развивается гипоксия тканей.
Внутренняя сердечная дисфункция
Первичные заболевания сердца зачастую возникают вследствие патологии коронарных сосудов и ишемической кардиомиопатии. Однако гипертензия, патология клапанов сердца, нарушения ритма и кардиомиопатии неишемической этиологии (алкоголь, вирус) также играют большую роль в дисфункции сердца. У пациентов с признаками гипоксии, при нормальном анализе крови на содержание кислорода, сердечная дисфункция является наиболее частой причиной данного состояния. Хотя при сердечной дисфункции чаще всего пациента госпитализируют, скрытые заболевания сердца часто обостряют основную причину заболевания. Сепсис может ухудшить тканевую гипоксию, связанную с гипотонией. Пациентам необходимо выполнить эхокардиографию, коронарную ангиографию, провести функциональные исследования, такие как стресс тест при подозрении на первичную патологию сердца.
Внешние сердечные нарушения
Неадекватная периферическая экстракция кислорода
Даже если кислород полностью связался с гемоглобином и был доставлен к тканям, то существует два обстоятельства, при которых нарушается утилизация кислорода клетками. Первым является тот факт, что кислород может быть сильно связан с гемоглобином, что препятствует переходу в ткани. Вторым является обстоятельство, при котором происходит интоксикация митохондрий, с помощью которых в клетке происходят процессы метаболизма.
Сродство гемоглобина к кислороду
Сродство гемоглобина к кислороду определяется по форме и позиции кривой диссоциации оксигемоглобина (рис. 6).
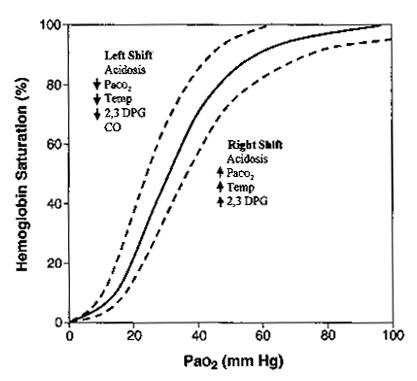 |
| Рисунок 6. Кривая диссоциации гемоглобина. Данная кривая показывает взаимоотношение РаО2 (по горизонтальной оси) с сатурацией гемоглобина (вертикальная ось). Существуют несколько факторов, которые влияют на способность гемоглобина связываться с кислородом. Кривая будет смещаться вправо, указывая на уменьшение связывания кислорода в легких или облегчение отдачи кислорода тканям. Данная картина встречается при ацидозе, гиперкапнии, гипертермии, повышения 2,3-дифосфоглицерата (2,3-ДФГ). Кривая будет отклоняться влево, увеличивая насыщение кислорода в легких и уменьшая отдачу кислорода тканям. Это встречается при алкалозе, гипокапнии, гипотермии, уменьшении 2,3-ДФГ, отравлении угарным газом. |
Когда кривая смещается вправо, сродство снижается и кислорода на грамм гемоглобина становится меньше, хотя на периферии кислород отсоединяется более легко. Когда кривая смещается влево и кверху сродство к кислороду увеличивается. Больше кислорода захватывается в легких где показатель РаО2 высокий, но на уровне тканей, где РаО2 низкий количество доступного кислорода снижается. Алкалоз, гипотермия, гипокапния, уменьшение 2,3-ДФГ приводят к сдвигу кривой влево. При переливании цельной крови происходит уменьшение 2,3-ДФГ, тем самым выражается вредное действие массивных гемотрансфузий. Так как 2,3-ДФГ вырабатывается эритроцитами, эффект обычно кратковременный. Угарный газ не сдвигает кривую влево, но занимает гемоглобиновые мостики и тем самым приводит к гипоксии.
Интоксикация митохондрий
Заключение
Существует большое количество заболеваний, которые могут закончиться гипоксемией. Гипоксемия возникает вследствие одного из этих факторов: снижение кислорода в окружающем воздухе, гиповентиляции, нарушения В/П, сброса крови «справа налево». При обследовании пациента необходимо установить действительно ли у него есть гипоксемия и если это так то необходимо определить Р(А-а)О2. Таким образом, определив газовый состав крови можно провести дифференциальный диагноз и правильно оценить ситуацию. Важно также запомнить, что при подключении более одного механизма необходимо снова и снова оценивать состояние пациента.
В результате чего развивается тканевая гипоксия
10.1. Классификация гипоксических состояний
Гипоксия – типовой патологический процесс, характеризующийся снижением содержания кислорода в крови (гипоксемией) и тканях, развитием комплекса вторичных неспецифических метаболических и функциональных расстройств, а также реакцией адаптации.
Первая классификация гипоксических состояний была предложена Баркрофтом (1925), а затем дополнена и усовершенствована И.Р. Петровым (1949). Классификация И.Р. Петрова используется и в наше время. Согласно этой классификации различают гипоксии экзогенного и эндогенного происхождения.
В основе гипоксии экзогенного происхождения лежит недостаток кислорода во вдыхаемом воздухе, в связи с чем выделяют нормобарическую и гипобарическую гипоксию. К гипоксиям эндогенного происхождения относятся следующие типы:
а) дыхательная (респираторная); б) сердечно-сосудистая (циркуляторная); в) гемическая (кровяная); г) тканевая (гистотоксическая); д) смешанная.
По течению различают:
• молниеносную (в течение нескольких секунд, например, при разгерметизации летательных аппаратов на большой высоте);
• острую (которая развивается через несколько минут или в пределах часа в результате острой кровопотери, острой сердечной или дыхательной недостаточности, при отравлении угарным газом, цианидами, при шоке, коллапсе);
• подострую (она формируется в течение нескольких часов при попадании в организм метгемоглобинообразователей, таких как нитраты, бензол, а в ряде случаев в результате медленно нарастающей дыхательной или сердечной недостаточности;
• хроническую гипоксию, которая возникает при дыхательной и сердечной недостаточности и других формах патологии, а также при хронической анемии, пребывании в шахтах, колодцах, при работе в водолазных и защитных костюмах.
а) местную (локальную) гипоксию, развивающуюся при ишемии, венозной гиперемии, престазе и стазе в зоне воспаления;
б) общую (системную) гипоксию, которая наблюдается при гиповолемии, сердечной недостаточности, шоке, коллапсе, ДВС-синдроме, анемиях.
Известно, что наиболее устойчивыми к гипоксии являются кости, хрящи и сухожилия, которые сохраняют нормальную структуру и жизнеспособность в течение многих часов при полном прекращении снабжения кислородом. Поперечно-полосатые мышцы выдерживают гипоксию в течение 2 часов; почки, печень – 20-30 минут. Наиболее чувствительна к гипоксии кора головного мозга.
10.2. Общая характеристика этиологических и патогенетических факторов гипоксий экзогенного и эндогенного происхождения
Экзогенный тип гипоксии развивается при уменьшении парциального давления кислорода в воздухе, поступающем в организм. При нормальном барометрическом давлении говорят о нормобарической экзогенной гипоксии (примером может служить нахождение в замкнутых помещениях малого объема). При снижении барометрического давления развивается гипобарическая экзогенная гипоксия (последнее наблюдается при подъеме на высоту, где РО2 воздуха снижено примерно до 100 мм рт. ст. Установлено, что при снижении РО2 до 50 мм рт. ст. возникают тяжелые расстройства, несовместимые с жизнью).
В ответ на изменение показателей газового состава крови (гипоксемию и гиперкапнию) возбуждаются хеморецепторы аорты, каротидных клубочков, центральные хеморецепторы, что вызывает стимуляцию бульбарного дыхательного центра, развитие тахи- и гиперпное, газового алкалоза, увеличение числа функционирующих альвеол.
Эндогенные гипоксические состояния являются в большинстве случаев результатом патологических процессов и болезней, приводящих к нарушению газообмена в легких, недостаточному транспорту кислорода к органам или к нарушению его утилизации тканями.
Дыхательная (респираторная) гипоксия
Респираторная гипоксия возникает вследствие недостаточности газообмена в легких, которая может быть обусловлена следующими причинами: альвеолярной гиповентиляцией, сниженной перфузией кровью легких, нарушением диффузии кислорода через аэрогематический барьер, и соответственно, нарушением вентиляционно-перфузионного соотношения. Патогенетическую основу дыхательной гипоксии составляют снижение содержания оксигемоглобина, повышение концентрации восстановленного гемоглобина, гиперкапния и газовый ацидоз.
Гиповентиляция легких является результатом действия ряда патогенетических факторов:
а) нарушения биомеханических свойств дыхательного аппарата при обструктивных и рестриктивных формах патологии;
б) расстройств нервной и гуморальной регуляции вентиляции легких;
в) снижения перфузии легких кровью и нарушения диффузии О2 через аэрогематический барьер;
г) избыточного внутри- и внелегочного шунтирования венозной крови.
Циркуляторная (сердечно-сосудистая, гемодинамическая) гипоксия развивается при локальных, региональных и системных нарушениях гемодинамики. В зависимости от механизмов развития циркуляторной гипоксии можно выделить ишемическую и застойную формы. В основе циркуляторной гипоксии может лежать абсолютная недостаточность кровообращения или относительная при резком возрастании потребности тканей в кислородном обеспечении (при стрессорных ситуациях).
Генерализованная циркуляторная гипоксия возникает при сердечной недостаточности, шоке, коллапсе, обезвоживании организма, ДВС-синд-роме и т.д., причем, если нарушения гемодинамики возникают в большом круге кровообращения, насыщение крови кислородом в легких может быть нормальным, а нарушается его доставка к тканям в связи с развитием венозной гиперемии и застойных явлений в большом круге кровообращения. При нарушениях гемодинамики в сосудах малого круга кровообращения страдает оксигенация артериальной крови. Локальная циркуляторная гипоксия возникает в зоне тромбоза, эмболии, ишемии, венозной гиперемии в тех или иных органах и тканях.
Особое место занимает гипоксия, связанная с нарушением транспорта кислорода в клетки при снижении проницаемости мембран для О2. Последнее наблюдается при интерстициальном отеке легких, внутриклеточной гипергидратации.
Для циркуляторной гипоксии характерны: снижение РаО2, увеличение утилизации О2 тканями вследствие замедления кровотока и активации системы цитохром, возрастание уровня ионов водорода и углекислого газа в тканях. Нарушение газового состава крови приводит к рефлекторной активации дыхательного центра, развитию гиперпноэ, увеличению скорости диссоциации оксигемоглобина в тканях.
Гемический (кровяной) тип гипоксии возникает в результате уменьшения эффективной кислородной емкости крови и, следовательно, ее кислород транспортирующей функции. Транспорт кислорода от легких к тканям почти полностью осуществляется при участии Hb. Главными звеньями снижения кислородной емкости крови являются:
1) уменьшение содержания Нb в единице объема крови и в полном объеме, например, при выраженных анемиях, обусловленных нарушением костно-мозгового кроветворения различного генеза, при постгеморрагических и гемолитической анемиях.
2) нарушение транспортных свойств Нb, которое может быть обусловлено либо снижением способности Нb эритроцитов связывать кислород в капиллярах легких, либо транспортировать и отдавать оптимальное количество его в тканях, что наблюдается при наследственных и приобретенных гемоглобинопатиях.
Достаточно часто гемическая гипоксия наблюдается при отравлении окисью углерода («угарным газом»), так как окись углерода обладает чрезвычайно высоким сродством к гемоглобину, почти в 300 раз превосходя сродство к нему кислорода. При взаимодействии окиси углерода с гемоглобином крови образуется карбоксигемоглобин, лишенный способности транспортировать и отдавать кислород.
Окись углерода содержится в высокой концентрации в выхлопных газах двигателей внутреннего сгорания, в бытовом газе и т.д.
Выраженные нарушения жизнедеятельности организма развиваются при увеличении содержания в крови НbСО до 50% (от общей концентрации гемоглобина). Повышение его уровня до 70-75 % приводит к тяжелой гипоксемии и летальному исходу.
Карбоксигемоглобин имеет ярко-красный цвет, поэтому при его избыточном образовании в организме кожа и слизистые становятся красными. Устранение СО из вдыхаемого воздуха приводит к диссоциации НbСО, но этот процесс протекает медленно и занимает несколько часов.
Воздействие на организм ряда химических соединений (нитратов, нитритов, окисла азота, бензола, некоторых токсинов инфекционного происхождения, лекарственных средств: феназепама, амидопирина, сульфаниламидов, продуктов ПОЛ и т.д.) приводит к образованию метгемоглобина, который не способен переносить кислород, так как содержит окисную форму железа (Fe3+).
Окисная форма Fe3+ обычно находится в связи с гидроксилом (ОН-). МетНb имеет темно-коричневую окраску и, именно этот оттенок приобретают кровь и ткани организма. Процесс образования метНb носит обратимый характер, однако его восстановление в нормальный гемоглобин происходит относительно медленно (в течение нескольких часов), когда железо Нb вновь переходит в закисную форму. Образование метгемоглобина не только снижает кислородную емкость крови, но и уменьшает способность активного оксигемоглобина диссоциировать с отдачей кислорода тканям.
Тканевая (гистотоксическая) гипоксия развивается вследствие нарушения способности клеток поглощать кислород (при нормальной его доставке к клетке) или в связи с уменьшением эффективности биологического окисления в результате разобщения окисления и фосфорилирования.
Развитие тканевой гипоксии связывают со следующими патогенетическими факторами:
1. Нарушением активности ферментов биологического окисления в процессе:
а) специфического связывания активных центров фермента, например, цианидами и некоторыми антибиотиками;
б) связывания SН-групп белковой части фермента ионами тяжелых металлов (Аg2+, Нg2+, Сu2+), в результате чего образуются неактивные формы фермента;
в) конкурентного блокирования активного центра фермента веществами, имеющими структурную аналогию с естественным субстратом реакции (оксалаты, малонаты).
2. Нарушением синтеза ферментов, которое может возникать при дефиците витаминов В1 (тиамина), ВЗ (РР), никотиновой кислоты и др., а также при кахексии различного происхождения.
3. Отклонениями от оптимума физико-химических параметров внутренней среды организма: рН, температуры, концентрации электролитов и др. Эти изменения возникают при разнообразных заболеваниях и патологических состояниях (гипотермиях и гипертермиях, недостаточности почек, сердца и печени, анемиях) и снижают эффективность биологического окисления.
4. Дезинтеграцией биологических мембран, обусловленной воздействием патогенных факторов инфекционной и неинфекционной природы, сопровождающейся снижением степени сопряжения окисления и фосфорилирования, подавлением образования макроэргических соединений в дыхательной цепи. Способностью разобщать окислительное фосфорилирование и дыхание в митохондриях обладают: избыток ионов Н+ и Са2+, свободных жирных кислот, адреналина, тироксина и трийодтиронина, некоторых лекарственных веществ (дикумарина, грамицидина и др.). В этих условиях увеличиваются расход кислорода тканями. В случаях набухания митохондрий, разобщения окислительного фосфорилирования и дыхания большая часть энергии трансформируется в тепло и не используется для ресинтеза макроергов. Эффективность биологического окисления снижается.