для чего гликоген в печени
Гликоген
Содержание
Гликоген в организме [ править | править код ]
Гликоген — это сложный углевод, который состоит из соединенных в цепочку молекул глюкозы. После приема пищи в кровь начинает поступать большое количество глюкозы и организм человека запасает излишки этой глюкозы в виде гликогена. Когда уровень глюкозы в крови начинает снижаться (например при выполнении физических упражнений), организм с помощью ферментов расщепляет гликоген, в результате чего уровень глюкозы остается в норме и органы (в том числе, мышцы во время тренировки) получают достаточное ее количество для производства энергии.
Гликоген откладывается главным образом в печени и мышцах. Общий запас гликогена в печени и мышцах взрослого человека составляет 300-400 г («Физиология человека» А.С. Солодков, Е.Б. Сологуб). В бодибилдинге имеет значение только тот гликоген, который содержится в мышечной ткани.
При выполнении силовых упражнений (бодибилдинг, пауэрлифтинг) общая усталость наступает в связи с истощением запасов гликогена, поэтому за 2 часа до тренировки рекомендуется съедать богатую углеводами пищу, чтобы восполнить запасы гликогена.
Биохимия и физиология [ править | править код ]
С химической точки зрения гликоген (C6H10O5)n представляет собой полисахарид, образованный остатками глюкозы, связанными α-1→4 связями (α-1→6 в местах разветвления); основной запасной углевод человека и животных. Гликоген (также иногда называемый животным крахмалом, несмотря на неточность этого термина) является основной формой хранения глюкозы в животных клетках. Откладывается в виде гранул в цитоплазме во многих типах клеток (главным образом печени и мышц). Гликоген образует энергетический резерв, который может быть быстро мобилизован при необходимости восполнить внезапный недостаток глюкозы. Гликогеновый запас, однако, не столь ёмок в калориях на грамм, как запас триглицеридов (жиров). Только гликоген, запасённый в клетках печени (гепатоциты) может быть переработан в глюкозу для питания всего организма. Содержание гликогена в печени при увеличении его синтеза может составить 5-6% от массы печени. [1] Общая масса гликогена в печени может достигать 100—120 граммов у взрослых. В мышцах гликоген перерабатывается в глюкозу исключительно для локального потребления и накапливается в гораздо меньших концентрациях (не более 1 % от общей массы мышц), в то же время его общий мышечный запас может превышать запас, накопленный в гепатоцитах. Небольшое количество гликогена обнаружено в почках, и ещё меньшее — в определённых видах клеток мозга (глиальных) и белых кровяных клетках.
В качестве запасного углевода гликоген присутствует также в клетках грибов.
Метаболизм гликогена [ править | править код ]
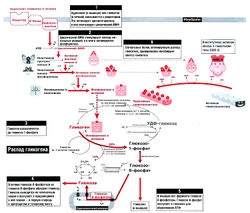
При недостатке в организме глюкозы гликоген под воздействием ферментов расщепляется до глюкозы, которая поступает в кровь. Регуляция синтеза и распада гликогена осуществляется нервной системой и гормонами. Наследственные дефекты ферментов, участвующих в синтезе или расщеплении гликогена, приводят к развитию редких патологических синдромов — гликогенозов.
Регуляция распада гликогена [ править | править код ]
Распад гликогена в мышцах инициирует адреналин, который связывается со своим рецептором и активирует аденилатциклазу. Аденилатциклаза начинает синтезировать циклический АМФ. Циклический АМФ запускает целый каскад реакций, которые в конечном итоге приводят к активации фосфорилазы. Гликогенфосфорилаза катализирует распад гликогена. В печени распад гликогена стимулируется глюкагоном. Этот гормон секретируют а-клетки поджелудочной железы при голодании.
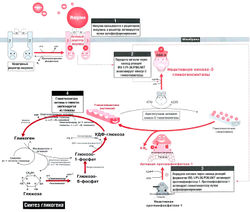
Регуляция синтеза гликогена [ править | править код ]
Синтез гликогена инициируется после связывания инсулина со своим рецептором. При этом происходит аутофосфорилирование остатков тирозина в рецепторе инсулина. Запускается каскад реакций, в которых поочередно активируются следующие сигнальные белки: субстрат-1 инсулинового рецептора, фосфоинозитол-3-киназа, фосфоинозитол-зависимая киназа-1, протеинкиназа АКТ. В конечном итоге ингибируется киназа-3 гликогенсинтазы. При голодании киназа-3 гликогенсинтетазы активна и инактивируется только на короткое время после приема пищи, в ответ на сигнал инсулина. Она ингибирует гликогенсинтазу путем фосфорилирования, не позволяя ей синтезировать гликоген. Во время приема пищи инсулин активирует каскад реакций, в результате которого ингибируется киназа-3 гликогенсинтазы и активируется протеинфосфатаза-1. Протеинфосфатаза-1 дефосфорилирует гликогенсинтазу, и последняя начинает синтезировать гликоген из глюкозы.
Протеинтирозинфосфатаза и ее ингибиторы
Как только прием пищи заканчивается, протеинтирозинфосфатаза блокирует действие инсулина. Она дефосфорилирует остатки тирозина в рецепторе инсулина, и рецептор переходит в неактивную форму. У больных диабетом II типа активность протеинтирозинфосфатазы чрезмерно повышена, что приводит к блокированию сигнала инсулина, и клетки оказываются невосприимчивы к инсулину. В настоящее время проводятся исследования, направленные на создание ингибиторов протеинфосфатазы, с помощью которых станет возможным разработать новые методы лечения в лечении диабета II типа.
Восполнение запасов гликогена [ править | править код ]
Большинство зарубежных специалистов [2] [3] [4] [5] [6] акцентирует внимание на необходимости возмещения гликогена как главного источника энергии для обеспечения мышечной активности. Повторные нагрузки, отмечается в этих работах, могут вызывать глубокое истощение запасов гликогена в мышцах и печени и отрицательно сказываться на результативности спортсменов. Пища с высоким содержанием углеводов увеличивает запас гликогена, энергетический потенциал мышц и улучшает общую работоспособность. Большая часть калорий в день (60-70%), по наблюдениям В. Shadgan, должна приходиться на углеводы, которые обеспечивают хлеб, крупы, зерновые культуры, овощи и фрукты.
Основные закономерности метаболических процессов в организме человека. Часть 2.
Рассматривая обмен веществ в условиях нормального функционирования организма, следует остановиться на безусловно взаимосвязанных, но в то же время достаточно специфичных составляющих метаболизма, а именно на углеводном, белковом, липидном и водно-электролитном обмене.
Очевидно, что основная роль углеводов в метаболизме определяется их энергетической функцией. Именно глюкоза крови вследствие наличия простого и быстрого пути гликолитической диссимиляции и последующего окисления в цикле трикарбоновых кислот, а также возможности максимально быстрого извлечения ее из депо гликогена, обеспечивающей экстренную мобилизацию энергетических ресурсов, является наиболее востребованным источником энергии в организме. Использование циркулирующей в плазме глюкозы разными органами неодинаково: мозг задерживает 12% глюкозы, кишечник— 9%, мышцы — 7%, почки — 5%. При этом уровень глюкозы плазмы крови является одной из важнейших гомеостатических констант организма, составляя 3, 3—5, 5 ммоль/л. Как известно снижение уровня глюкозы ниже допустимого передела имеет своим незамедлительным следствием дискоординацию деятельности ЦНС, проявляющуюся соответствующей клинической симптоматикой: головной мозг содержит небольшие резервы углеводов и нуждается в постоянном поступлении глюкозы, поскольку энергетические расходы мозга покрываются исключительно за счет углеводов. Глюкоза в тканях мозга преимущественно окисляется, а небольшая часть ее превращается в молочную кислоту.
При полном отсутствии углеводов в пище они образуются в организме из продуктов трансформации жиров и белков. В печени возможно новообразование углеводов как из собственных продуктов их распада (пировиноградной или молочной кислоты), так и из продуктов диссимиляции жиров и белков (кетокислот и аминокислот), что обозначается как глюконеогенез. В результате трансформации аминокислот образуется пировиноградная кислота, при окислении жирных кислот — ацетилкоэнзим А, который может превращаться в пировиноградную кислоту — предшественник глюкозы. Это наиболее важный общий путь биосинтеза углеводов. Между двумя основными источниками энергии — углеводами и жирами — существует тесная физиологическая взаимосвязь. Повышение содержания глюкозы в крови увеличивает биосинтез триглицеридов и уменьшает распад жиров в жировой ткани. Поступление в кровь свободных жирных кислот уменьшается. В случае возникновения гипогликемии процесс синтеза триглицеридов тормозится, ускоряется распад жиров и в кровь в большом количестве поступают свободные жирные кислоты. Гликогенез, гликогенолиз и глюконеогенез являются тесно взаимосвязанными процессами, обеспечивающими оптимальный уровень глюкозы крови сообразно степени функционального напряжения организма.
Центральным звеном регуляции углеводного и других видов обмена и местом формирования сигналов, управляющих уровнем глюкозы, является гипоталамус. Отсюда регулирующие влияния реализуются вегетативными нервами и гуморальным путем, включающим эндокринные железы. Единственным гормоном, снижающим уровень гликемии, является инсулин — гормон, вырабатываемый β-клетками островков Ланхгерганса. Снижение гликемии происходит за счет усиления инсулином синтеза гликогена в печени и мышцах и повышения потребления глюкозы тканями организма. Увеличение уровня глюкозы в крови возникает при действии нескольких гормонов. Это глюкагон, продуцируемый α-клетками островков Ланхгерганса, адреналин — гормон мозгового слоя надпочечников, глюкокортикоиды — гормоны коркового слоя надпочечников, соматотропный гормон гипофиза, тироксин и трийодтиронин — гормоны щитовидной железы. Данные гормоны в связи с однонаправленностью их влияния на углеводный обмен и функциональным антагонизмом по отношению к эффектам инсулина часто объединяют понятием «контринсулярные гормоны».
Таким образом биологическая роль углеводов для организма человека определяется прежде всего их энергетической функцией. Обладая энергетической ценностью в 16, 7 кДж (4, 0 ккал) на 1 грамм вещества, углеводы являются основным источником энергии для всех клеток организма, при этом выполняя еще пластическую и опорную функции. Суточная потребность взрослого человека в углеводах составляет около 500 г.
— пластическая (структурная) функция заключается в том, что белки являются главной составной частью всех клеточных и межклеточных структур тканей;
— ферментная (каталитическая, энзимная) функция состоит в обеспечении всех химических реакций, протекающих в ходе обмена веществ в организме (дыхание, пищеварение, выделение), деятельностью ферментов, являющихся по своей структуре белками;
— транспортная функция белков заключается в их способности к соединению с целым рядом метаболитов и переносе последних в связанном состоянии в межтканевой жидкости и плазме крови к области их утилизации;
— защитная функция белков проявляется реализацией иммунного ответа образованием иммуноглобулинов (антител) и системы комплемента при поступлении в организм чужеродного белка, а также способностью к непосредственному связыванию экзогенных токсинов; белки системы гемостаза обеспечивают свертывание крови и остановку кровотечения при повреждении кровеносных сосудов;
— регуляторная функция, направленная на сохранение гомеостаза с поддержанием биологических констатнт организма, реализуется буферными свойствами молекулы протеинов, белковой структурой клеточных рецепторов, активируемых в свою очередь регуляторными полипептидами и гормонами, также имеющими белковую структуру;
— двигательная функция, обеспечивается взаимодействием сократительных белков мышечной ткани актина и миозина;
— энергетическая роль белков состоит в обеспечении организма энергией, образующейся при диссимиляции белковых молекул; при окислении 1 г белка в среднем освобождается энергия, равная 16, 7 кДж (4, 0 ккал).
При катаболизме почти все природные аминокислоты сначала передают аминогруппу на а-кетоглутарат в реакции трансаминирования с образованием глутамата и соответствующей кетокислоты. Затем глутамат подвергается прямому окислительному дезаминированию под действием глутаматдегидрогеназы, в результате чего получаются а-кетоглутарат и аммиак. При необходимости синтеза аминокислот и наличии необходимых а-кетокислот обе стадии непрямого дезаминирования протекают в обратном направлении. В результате восстановительного аминирования а-кетоглутарата образуется глутамат, который вступает в трансаминирование с соответствующей а-кетокислотой, что приводит к синтезу новой аминокислоты. В случае использования белков в качестве источника энергии большинство аминокислот окисляются в конечном счёте через цикл лимонной кислоты до углекислого газа и воды. Прежде, чем эти вещества вовлекаются в заключительный этап катаболизма, их углеродный скелет превращается в двухуглеродный фрагмент в форме ацетил-КоА. Именно в этой форме большая часть молекул аминокислот включается в цикл лимонной кислоты.
Таблица 1. 1. Аминокислоты, входящие в состав белков человека.
1. Незаменимые
2. Частично заменимые
3. Условно заменимые
4. Заменимые
Таблица 1. 2. Классификация липидов организма человека.
1. Гликолипиды.
Содержат углеводный компонент.
2. Жиры.
3. Минорные липиды.
4. Стероиды.
А. Стерины (спирты).
Наиболее важен холестерин.
В. Стериды.
Эфиры стеринов и высших жирных кислот. Наиболее распространены эфиры холестерина.
5. Фосфолипипы.
Одним из продуктов катаболизма жиров, имеющем важное значения для метаболизма в целом являются кетоновые тела. Кетоновые тела — группа органических соединений, являющихся промежуточными продуктами жирового, углеводного и белкового обменов. К кетоновым телам относят β-оксимасляную и ацетоуксусную кислоты и ацетон, имеющие сходное строение и способные к взаимопревращениям. Главным путем синтеза кетоновых тел, происходящего в основном в печени, считается реакция конденсации между двумя молекулами ацетил-КоА, образовавшегося при β-окислении жирных кислот или при окислительном декарбоксилировании пирувата (пировиноградной кислоты) в процессе обмена глюкозы и ряда аминокислот. Данный путь синтеза кетоновых тел более других зависит от характера питания и в большей степени страдает при патологических нарушениях обмена веществ. Из печени кетоновые тела поступают в кровь и с нею во все остальные органы и ткани, где они включаются в универсальный энергообразующий цикл — цикл трикарбоновых кислот, в котором окисляются до углекислоты и воды. Кетоновые тела используются также для синтеза холестерина, высших жирных кислот, фосфолипидов и заменимых аминокислот. При голодании, однообразном безуглеводистом питании и при недостаточной секреции инсулина использование ацетил-КоА в цикле трикарбоновых кислот подавляется, так как все метаболически доступные ресурсы организма превращаются в глюкозу крови. В этих условиях увеличивается синтез кетоновых тел. Следует подчеркнуть важную роль кетоновых тел в поддержании энергетического баланса. Кетоновые тела – поставщики «топлива» для мышц, почек и действуют, возможно, как часть регуляторного механизма с обратной связью, предотвращая чрезвычайную мобилизацию жирных кислот из жировых депо. Печень в этом смысле является исключением, она не использует кетоновые тела в качестве энергетического материала.
Процесс образования, отложения и мобилизации из депо жира регулируется нервной и эндокринной системами, а также тканевыми механизмами и тесно связаны с углеводным обменом. Так, повышение концентрации глюкозы в крови уменьшает распад триглицеридов и активизирует их синтез. Понижение концентрации глюкозы в крови, наоборот, тормозит синтез триглицеридов и усиливает их расщепление. Таким образом, взаимосвязь жирового и углеводного обменов направлена на обеспечение энергетических потребностей организма. При избытке углеводов в пище триглицериды депонируются в жировой ткани, при нехватке углеводов происходит расщепление триглицеридов с образованием неэтерифицнрованных жирных кислот, служащих источником энергии. В обмене жиров одна из важнейших ролей принадлежит печени. Печень — основной орган, в котором происходит образование кетоновых тел (бета-оксимасляная, ацетоуксусная кислоты, ацетон), используемых как альтернативный глюкозе источник энергии.
Как указывалось выше метаболизм жиров контролируется нервной и эндокринной системами. Мобилизация жиров из депо происходит под влиянием гормонов мозгового слоя надпочечников — адреналина и норадреналина. Соматотропный гормон гипофиза также обладает жиромобилизирующим действием. Аналогично действует тироксин — гормон щитовидной железы. Тормозят мобилизацию жира глюкокортикоиды — гормоны коркового слоя надпочечника, вероятно, вследствие того, что они несколько повышают уровень глюкозы в крови. Действие инсулина связано с повышением активности внутриклеточной фосфодиэстеразы, что приводит к снижению концентрации цАМФ и угнетению липолиза. Таким образом, инсулин усиливает синтез жира и уменьшает скорость его мобилизации. Имеются данные, свидетельствующие о возможности прямых нервных влияний на обмен жиров. Симпатические влияния тормозят синтез триглицеридов и усиливают их распад. Парасимпатические влияния, напротив, способствуют отложению жира в депо.
Статья добавлена 31 мая 2016 г.
Что такое гликоген, как он влияет на наши тренировки и можно ли увеличить его запасы в организме?
Гликоген – это полисахарид (длинная цепочка углеводов), который хранится в печени и скелетных мышцах и является источником глюкозы в периоды мышечной активности или отсутствия пищи.
В 1920-х годах стало очевидно, что углеводы выступают важным источником топлива для тренировки мышц. Чуть позже было доказано, что концентрация глюкозы в крови связана с утомляемостью во время марафонского бега, и что увеличение потребления углеводов перед забегом и питание по ходу дистанции предотвращали слабость и утомляемость.
Несмотря на эти наблюдения и гораздо более раннее открытие гликогена в 1858 году, связь между содержанием углеводов в рационе, уровнем полисахаридов в мышцах и способностью выполнять больше физической работы подтвердилась лишь в 1960-х годах, когда группа скандинавских ученых воспользовалась методом мышечной биопсии (отсечение небольшого образца ткани для изучения), чтобы установить, что содержание мышечного гликогена оказывает значительное влияние на работоспособность.
Роль гликогена в организме
Способность спортсменов тренироваться день за днем в значительной степени зависит от адекватного восполнения запасов гликогена в организме – процесса, который требует потребления достаточного количества углеводов с пищей и адекватного времени отдыха. Попытка новичков тренироваться несколько раз в день и последующее чувство усталости в том числе связано с исчерпаемостью запасов гликогена, которые дают нам необходимую энергию в процессе тренировок.
При планировании тренировочного процесса важно учитывать не только сами тренировки, но и сбалансированное питание и отдых. Также необходимо понимать, как конкретный вид спорта расходует запасы энергии.
Например, спорт на выносливость (бег, велоспорт, плавание, лыжи) выжигает значительные запасы углеводов и требует особого внимания к правильному питанию после тренировок, особенно длительных и интенсивных.
Где накапливается гликоген и как восполнить его запасы
Гликоген преимущественно накапливается в печени и скелетных мышцах. При этом данные депо (совокупный объем накопленных полисахаридов) выполняют разные функции и по разному питают организм.
Гликоген печени в основном поставляет глюкозу в кровоток во время периодов голодания, а тот, что хранится в скелетных мышцах, обеспечивает глюкозой мышечные волокна во время физической нагрузки. Следовательно, его содержание в печени уменьшается, когда вы долго не употребляете углеводы, а в мышцах концентрация полисахаридов падает после продолжительных и интенсивных тренировок.
Гликоген в печени преимущественно восстанавливается сразу после приема пищи. Этот процесс называется прямым синтезом гликогена.
С мышцами все немного сложнее. Сразу после физической нагрузки мышечные волокна, которые были задействованы в работе, метаболически подготавливаются к быстрому гликогенезу (процессу синтеза полисахаридов из глюкозы). Проще говоря, использование гликогена во время упражнений запускает его синтез в период восстановления.
Когда после тренировки углеводы попадают в организм с пищей, отработавшие на полную мышцы начинают усиленно поглощать глюкозу из еды, заполняя гликогеновые депо. Эта повышенная чувствительность может длиться до 48 часов. Именно поэтому важно после изматывающей тренировки сразу съесть что-то с высоким содержанием углеводов.
Особенно важно правильное питание во время многодневных соревнований, например, в велогонках. Если у спортсмена есть хотя бы 6 часов отдыха между этапами, то употребление углеводов из расчета 1-1,2 г на килограмм веса в час позволит восполнить до 80% опустевших депо к старту следующего отрезка гонки.
Признаки и причины низкого уровня гликогена
Низкий уровень полисахаридов в организме будет выражаться в быстрой утомляемости при выполнении физических упражнений и умственной работе. Решить эту проблему поможет питание, богатое углеводами, и отдых.
Также встречаются метаболические заболевания – гликогенозы, 1 случай на 100-500 тысяч новорожденных. Эти нарушения обмена веществ вызваны дефицитом ферментов, влияющих на синтез гликогена в мышцах и клетках печени. Они проявляются в виде быстрой мышечной утомляемости, судорог при занятиях спортом и даже миопатии (поражениях мышц и нервов).
Можно ли повысить запасы гликогена и как?
Физические упражнения способствуют накоплению гликогена после тренировок. В задействованных в ходе занятий мышцах содержание полисахаридов во время восстановления быстро увеличивается, достигая со временем более высокого уровня, чем до начала тренировок (эффект суперкомпенсации). Соответственно, у регулярно тренирующихся людей запасы гликогена в организме будут выше, чем у нетренированных.
Важно понимать, что продукты питания сами по себе не повышают запасы гликогена, а лишь способствуют его более быстрому восполнению. Именно поэтому для регулярно тренирующихся или занятых физическим трудом людей важно контролировать достаточное содержание углеводов в рационе.
Какие продукты рекомендовано есть?
В первые часы после тренировки употребление продуктов с высоким гликемическим индексом (ГИ), например, сладостей, выпечки, риса или картофеля может ускорить восстановление гликогена в мышцах.
Также в двух исследованиях было доказано, что при недостатке углеводов в рационе прием дополнительных 0,3-0,4 г протеина на килограмм массы тела ускорял восполнение полисахаридов. В некоторых публикациях можно найти доказательства того, что прием креатина положительно влияет на синтез гликогена в мышцах в период отдыха после тренировок.
Еще один важный момент: учитывайте, что избыточное употребление углеводов не ускоряет процесс расширения гликогеновых депо у тренирующихся. Также длительное потребление большого количества углеводов не увеличивает содержание полисахаридов в скелетных мышцах у нетренированных людей. Питайтесь сбалансировано в соответствии с вашими тренировкам.